L-赖氨酸 | 56-87-1
物质功能分类
中文名称
L-赖氨酸
中文别名
赖氨酸;2,6二氨基己酸;(S)-2,6-二氨基己酸;L-已氨酸;L-2,6-二氨基已酸,L-已氨酸,L-松氨酸;L-2,6-二氨基己酸;L-(+)-赖氨酸;L-赖氨酸碱;L-己氨酸;L-松氨酸
英文名称
L-lysine
英文别名
lysine;Lys;L-Lys;K;(2S)-2,6-diaminohexanoic acid;(2S)-6-amino-2-azaniumylhexanoate
CAS
56-87-1
化学式
C6H14N2O2
mdl
——
分子量
146.189
InChiKey
KDXKERNSBIXSRK-YFKPBYRVSA-N
BEILSTEIN
——
EINECS
——
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
物化性质
-
熔点:215 °C (dec.)(lit.)
-
比旋光度:D20 +14.6° (c = 6.5); D23 +25.9° (c = 2 in 6.0N HCl)
-
沸点:265.81°C (rough estimate)
-
密度:1.1360 (rough estimate)
-
溶解度:在水中的溶解度0.1 g/mL,澄清,无色
-
LogP:-3.05
-
物理描述:Solid
-
颜色/状态:Needles from water, hexagonal plates from dilute alcohol
-
味道:Sweet/bitter
-
蒸汽压力:5.28X10+9 mm Hg at 25 °C /extrapolated/
-
亨利常数:Henry's Law constant = 3.59X10-13 atm-cu m/mol at 25 °C (est)
-
旋光度:Specific optical rotation: +14.6 at 20 °C/D (c = 6.5); +25.9 at 23 °C/D (c = 2 in 6.0N HCl)
-
分解:When heated to decomposition it emits toxic fumes of /nitric oxide/.
-
解离常数:3.12 (at 0 °C)
-
碰撞截面:130.7 Ų [M+H]+ [CCS Type: DT, Method: single field calibrated with Agilent tune mix (Agilent)]
-
稳定性/保质期:
存在于烟叶中。
计算性质
-
辛醇/水分配系数(LogP):-3
-
重原子数:10
-
可旋转键数:5
-
环数:0.0
-
sp3杂化的碳原子比例:0.83
-
拓扑面积:89.3
-
氢给体数:3
-
氢受体数:4
ADMET
代谢
肝脏的
Hepatic
来源:DrugBank
代谢
Like other amino acids, the metabolism of free lysine follows two principal paths: protein synthesis and oxidative catabolism. It is required for biosynthesis of such substances as carnitine, collage, and elastin.
来源:Hazardous Substances Data Bank (HSDB)
代谢
Oxidative deamination or transamination of l-lysine /yields/ alpha-keto-epsilon-aminocaproic acid; decarboxylation of l-lysine /yields/ cadaverine. /From table/
来源:Hazardous Substances Data Bank (HSDB)
代谢
一旦氨基酸脱氨产物进入三羧酸循环(也称为柠檬酸循环或克雷布斯循环)或糖酵解途径,它们的碳骨架也可用于生物合成途径,特别是用于葡萄糖和脂肪的生成。氨基酸的碳骨架是形成葡萄糖还是脂肪取决于其进入这两个途径的点。如果它们作为乙酰辅酶A进入,那么只能形成脂肪或酮体。然而,其他氨基酸的碳骨架可以以这样的方式进入途径,即它们的碳可用于糖异生。这是将氨基酸经典营养描述为生酮或生糖(即能够产生酮体[或脂肪]或葡萄糖)的基础。一些氨基酸在降解时产生这两种产物,因此被认为是既生酮又生糖的。/氨基酸/
Once the amino acid deamination products enter the tricarboxylic acid (TCA) cycle (also known as the citric acid cycle or Krebs cycle) or the glycolytic pathway, their carbon skeletons are also available for use in biosynthetic pathways, particularly for glucose and fat. Whether glucose or fat is formed from the carbon skeleton of an amino acid depends on its point of entry into these two pathways. If they enter as acetyl-CoA, then only fat or ketone bodies can be formed. The carbon skeletons of other amino acids can, however, enter the pathways in such a way that their carbons can be used for gluconeogenesis. This is the basis for the classical nutritional description of amino acids as either ketogenic or glucogenic (ie, able to give rise to either ketones [or fat] or glucose). Some amino acids produce both products upon degradation and so are considered both ketogenic and glucogenic. /Amino acids/
来源:Hazardous Substances Data Bank (HSDB)
代谢
在慢性低血糖期间和恢复到正常血糖水平后,胎儿绵羊的赖氨酸代谢率与正常、同龄正常血糖对照组胎儿的结果进行了比较,以解释蛋白质代谢对低葡萄糖浓度的适应性反应。限制母体向胎儿的葡萄糖供应降低了胎儿(脐带)葡萄糖(42%)和乳酸(36%)的净摄取率,导致胎儿赖氨酸代谢的补偿性改变。与正常血糖对照组胎儿相比,低血糖组胎儿的血浆赖氨酸浓度高出1.9倍,但胎儿(脐带)赖氨酸摄取率没有差异。在低血糖组胎儿中,赖氨酸处置率也高于对照组胎儿,这是由于赖氨酸回流到胎盘和胎儿组织的速率更高。赖氨酸脱羧产生CO2的排放率在低血糖组胎儿中是对照组胎儿的2.4倍,这表明在慢性低血糖期间赖氨酸的氧化代谢速率更高。尽管低血糖组和对照组之间胎儿蛋白质积累或合成速率没有差异,但在低血糖组胎儿中蛋白质分解速率显著增加(p < 0.05),这表明每个速率都有小的变化。这一点得到了肌肉特异性泛素连接酶的升高和4E-BP1浓度的增加的支持。慢性低血糖后的正常血糖恢复使所有通量正常化,实际上降低了与对照组胎儿相比的赖氨酸脱羧化速率(p < 0.05)。这些结果表明,慢性低血糖增加了净蛋白质分解和赖氨酸氧化代谢,两者都导致胎儿生长速率随时间减慢。此外,5天的正常血糖校正使赖氨酸通量恢复正常,并导致赖氨酸氧化的过度校正。
... Rates of lysine metabolism in fetal sheep during chronic hypoglycemia and following euglycemic recovery /were compared with/ results with normal, age-matched euglycemic control fetuses to explain the adaptive response of protein metabolism to low glucose concentrations. Restriction of the maternal glucose supply to the fetus lowered the net rates of fetal (umbilical) glucose (42%) and lactate (36%) uptake, causing compensatory alterations in fetal lysine metabolism. The plasma lysine concentration was 1.9-fold greater in hypoglycemic compared with control fetuses, but the rate of fetal (umbilical) lysine uptake was not different. In the hypoglycemic fetuses, the lysine disposal rate also was higher than in control fetuses due to greater rates of lysine flux back into the placenta and into fetal tissue. The rate of CO2 excretion from lysine decarboxylation was 2.4-fold higher in hypoglycemic than control fetuses, indicating greater rates of lysine oxidative metabolism during chronic hypoglycemia. No differences were detected for rates of fetal protein accretion or synthesis between hypoglycemic and control groups, although there was a significant increase in the rate of protein breakdown (p < 0.05) in the hypoglycemic fetuses, indicating small changes in each rate. This was supported by elevated muscle specific ubiquitin ligases and greater concentrations of 4E-BP1. Euglycemic recovery after chronic hypoglycemia normalized all fluxes and actually lowered the rate of lysine decarboxylation compared with control fetuses (p < 0.05). These results indicate that chronic hypoglycemia increases net protein breakdown and lysine oxidative metabolism, both of which contribute to slower rates of fetal growth over time. Furthermore, euglycemic correction for 5 days returns lysine fluxes to normal and causes an overcorrection of lysine oxidation.
来源:Hazardous Substances Data Bank (HSDB)
毒理性
单纯疱疹病毒的蛋白质富含L-精氨酸,组织培养研究显示,当组织培养介质中L-精氨酸与L-赖氨酸的氨基酸比例较高时,能增强病毒的复制。当L-赖氨酸与L-精氨酸的比例较高时,已发现单纯疱疹病毒的复制和细胞病理效应受到抑制。L-赖氨酸可能有助于从小肠吸收钙。
Proteins of the herpes simplex virus are rich in L-arginine, and tissue culture studies indicate an enhancing effect on viral replication when the amino acid ratio of L-arginine to L-lysine is high in the tissue culture media. When the ratio of L-lysine to L-arginine is high, viral replication and the cytopathogenicity of herpes simplex virus have been found to be inhibited. L-lysine may facilitate the absorption of calcium from the small intestine.
来源:Toxin and Toxin Target Database (T3DB)
毒理性
对人类不具有致癌性(未被国际癌症研究机构IARC列名)。
No indication of carcinogenicity to humans (not listed by IARC).
来源:Toxin and Toxin Target Database (T3DB)
毒理性
Chronically high levels of lysine are associated with at least 5 inborn errors of metabolism including: D-2-Hydroxyglutaric Aciduria, Familial Hyperlysinemia I, Hyperlysinemia II, Pyruvate carboxylase deficiency and Saccharopinuria.
来源:Toxin and Toxin Target Database (T3DB)
毒理性
从小肠腔通过主动运输过程被吸收进入肠细胞
Absorbed from the lumen of the small intestine into the enterocytes by an active transport process
来源:Toxin and Toxin Target Database (T3DB)
毒理性
赖氨酸以10毫摩尔/千克的剂量给予小鼠,持续1到10天,显著增加了由60毫克/千克戊四唑(PTZ)引起的阵挛性和强直性癫痫发作的潜伏期。在第1天,阵挛性和强直性癫痫发作的潜伏期分别从160.4 ± 26.3秒和828.6 ± 230.8秒增加到286.1 ± 103.3秒和982.3 ± 98.6秒。随着额外赖氨酸的治疗,阵挛性和强直性癫痫发作的潜伏期稳步增加,而存活率没有显著变化。在第10天,抗惊厥效果达到最高水平,阻止了强直性发作,存活率为100%,没有产生耐受性。急性赖氨酸显著增加了85.8 ± 5.24秒到128.2 ± 9.0秒的平均阵挛潜伏期和由80毫克/千克PTZ引起的平均强直性发作从287.2 ± 58.7秒到313.5 ± 42.2秒。在治疗第10天,赖氨酸的抗惊厥效果最高,阵挛性和强直性潜伏期分别比对照组显著增加了155%和184%。在治疗15天和20天后,阵挛性和强直性癫痫发作的潜伏期和存活率降低,提示产生了耐受性...
Lysine 10 mmol/kq given to mice for 1 to 10 days significantly increased clonic and tonic seizure latencies caused by 60 mg/kg pentylenetetrazol (PTZ). On day 1 the clonic and tonic seizure latencies were increased from 160.4 +/- 26.3 and 828.6 +/- 230.8 s to 286.1 +/- 103.3 and 982.3 +/- 98.6 respectively. Both clonic and tonic seizure latencies increased steadily with additional L-lysine treatment without significant change in survival rate. On day 10, the anticonvulsant effect reached its highest level with a block of tonic seizures and survival rate of 100% without tolerance developing. Acute L-lysine significantly increased the mean clonic latency from 85.8 +/- 5.24 to 128.2 +/- 9.0 s and the mean tonic seizure from 287.2 +/- 58.7 to 313.5 +/- 42.2 s with 80 mg/kg of PTZ. On day 10 of treatment, the anticonvulsant effect of L-lysine was highest, with a significant incr of 155 and 184% in clonic and tonic latencies over control, respectively. After 15 and 20 day treatment, clonic and tonic seizure latencies and survival rate decreased, suggesting development of tolerance ...
来源:Hazardous Substances Data Bank (HSDB)
吸收、分配和排泄
从小肠腔通过主动运输过程被吸收进入肠细胞
Absorbed from the lumen of the small intestine into the enterocytes by an active transport process
来源:DrugBank
吸收、分配和排泄
尽管溶解在体液中的游离氨基酸仅占全身氨基酸总量的一小部分,但它们对于身体蛋白质的营养和代谢控制非常重要。尽管血浆室最容易被取样,但大多数氨基酸在组织细胞内池中的浓度更高。通常,大中性氨基酸,如亮氨酸和苯丙氨酸,基本上与血浆处于平衡状态。其他的氨基酸,特别是谷氨酰胺、谷氨酸和甘氨酸,在细胞内池中的浓度比血浆中高10到50倍。饮食变化或病理状态可能导致血浆和组织池中个别游离氨基酸浓度发生显著变化。/氨基酸/
Although the free amino acids dissolved in the body fluids are only a very small proportion of the body's total mass of amino acids, they are very important for the nutritional and metabolic control of the body's proteins. ... Although the plasma compartment is most easily sampled, the concentration of most amino acids is higher in tissue intracellular pools. Typically, large neutral amino acids, such as leucine and phenylalanine, are essentially in equilibrium with the plasma. Others, notably glutamine, glutamic acid, and glycine, are 10- to 50-fold more concentrated in the intracellular pool. Dietary variations or pathological conditions can result in substantial changes in the concentrations of the individual free amino acids in both the plasma and tissue pools. /Amino acids/
来源:Hazardous Substances Data Bank (HSDB)
吸收、分配和排泄
摄入后,蛋白质在胃中被胃酸变性,同时被胃蛋白酶分解成更小的肽。这种酶在进食时由于胃酸增加而被激活。然后,蛋白质和肽进入小肠,在那里肽键被多种酶水解。这些特定于肽键的酶来自胰腺,包括胰蛋白酶、胰凝乳蛋白酶、弹性蛋白酶和羧肽酶。随后,由自由氨基酸和短肽组成的混合物通过多种载体系统被运输到粘膜细胞中,这些载体系统专门用于特定氨基酸和二肽和三肽,每种系统只限于一定范围的肽底物。吸收的肽在细胞内水解后,自由氨基酸通过粘膜细胞中的其他特定载体系统分泌到门静脉血液中,或者进一步在细胞内代谢。吸收的氨基酸进入肝脏,其中一部分被摄取和使用;其余的通过进入全身循环,被外周组织利用。/氨基酸/
After ingestion, proteins are denatured by the acid in the stomach, where they are also cleaved into smaller peptides by the enzyme pepsin, which is activated by the increase in stomach acidity that occurs on feeding. The proteins and peptides then pass into the small intestine, where the peptide bonds are hydrolyzed by a variety of enzymes. These bond-specific enzymes originate in the pancreas and include trypsin, chymotrypsins, elastase, and carboxypeptidases. The resultant mixture of free amino acids and small peptides is then transported into the mucosal cells by a number of carrier systems for specific amino acids and for di- and tri-peptides, each specific for a limited range of peptide substrates. After intracellular hydrolysis of the absorbed peptides, the free amino acids are then secreted into the portal blood by other specific carrier systems in the mucosal cell or are further metabolized within the cell itself. Absorbed amino acids pass into the liver, where a portion of the amino acids are taken up and used; the remainder pass through into the systemic circulation and are utilized by the peripheral tissues. /Amino acids/
来源:Hazardous Substances Data Bank (HSDB)
吸收、分配和排泄
蛋白质分泌到肠道的现象即使在没有蛋白质摄入的情况下也会持续,而粪便中的氮损失(即以细菌形式在粪便中损失的氮)可能占必需氮损失量的25%。在这种情况下,作为蛋白水解酶的组成部分和脱落的粘膜细胞分泌到肠道的氨基酸,是维持肠道细菌生物量的唯一氨基酸来源。 ... 完整氨基酸的其它损失途径是通过尿液以及皮肤和头发的脱落。与上述损失相比,这些损失虽然较小,但仍然可能对需求估计产生重大影响,特别是在疾病状态下。 /氨基酸/
Protein secretion into the intestine continues even under conditions of protein-free feeding, and fecal nitrogen losses (ie, nitrogen lost as bacteria in the feces) may account for 25% of the obligatory loss of nitrogen. Under this dietary circumstance, the amino acids secreted into the intestine as components of proteolytic enzymes and from sloughed mucosal cells are the only sources of amino acids for the maintenance of the intestinal bacterial biomass. ... Other routes of loss of intact amino acids are via the urine and through skin and hair loss. These losses are small by comparison with those described above, but nonetheless may have a significant impact on estimates of requirements, especially in disease states. /Amino acids/
来源:Hazardous Substances Data Bank (HSDB)
吸收、分配和排泄
一个健康的成年人每天通过尿液排出大约11到15克的氮,这通常是在摄入70到100克蛋白质的情况下发生的,大部分以尿素的形式排出,还有少量的氨、尿酸、肌酐和一些游离氨基酸。这些都是蛋白质代谢的最终产物,尿素和氨来自于氨基酸的部分氧化。尿酸和肌酐也是间接来源于氨基酸。将氮从各个氨基酸中移除并转化为可以通过肾脏排出的形式,可以被认为是一个两步过程。第一步通常通过两种类型的酶促反应之一进行:转氨作用或脱氨作用。转氨作用是一个可逆反应,使用葡萄糖代谢的酮酸中间体(例如,丙酮酸、草酰乙酸和α-酮戊二酸)作为氨基酸氮的受体。大多数氨基酸可以参与这些反应,结果它们的氨基酸氮转移到了只有三种氨基酸:丙氨酸来自丙酮酸,天冬氨酸来自草酰乙酸,谷氨酸来自α-酮戊二酸。与许多氨基酸不同,支链氨基酸的转氨作用发生在全身,特别是在骨骼肌中。在这里,氨基酸氮的主要受体是丙氨酸和谷氨酰胺(分别来自丙酮酸和谷氨酸),然后它们进入血液循环。这些作为将氮从外周(骨骼肌)输送到肠道和肝脏的重要载体。在小肠中,谷氨酰胺被提取并代谢成氨、丙氨酸和瓜氨酸,然后通过门静脉系统输送到肝脏。氮也通过脱氨反应从氨基酸中移除,从而形成氨。许多氨基酸可以被脱氨,直接(组氨酸)、通过脱水(丝氨酸、苏氨酸)、通过嘌呤核苷酸循环(天冬氨酸)或通过氧化脱氨(谷氨酸)... 谷氨酸还形成于精氨酸和赖氨酸的特定降解途径中。因此,任何氨基酸的氮都可以转移到尿素合成的两个前体中,即氨和天冬氨酸。/氨基酸/
About 11 to 15 g of nitrogen are excreted each day in the urine of a healthy adult consuming 70 to 100 g of protein, mostly in the form of urea, with smaller contributions from ammonia, uric acid, creatinine, and some free amino acids. These are the end products of protein metabolism, with urea and ammonia arising from the partial oxidation of amino acids. Uric acid and creatinine are indirectly derived from amino acids as well. The removal of nitrogen from the individual amino acids and its conversion to a form that can be excreted by the kidney can be considered as a two-part process. The first step usually takes place by one of two types of enzymatic reactions: transamination or deamination. Transamination is a reversible reaction that uses ketoacid intermediates of glucose metabolism (e.g., pyruvate, oxaloacetate, and alpha-ketoglutarate) as recipients of the amino nitrogen. Most amino acids can take part in these reactions, with the result that their amino nitrogen is transferred to just three amino acids: alanine from pyruvate, aspartate from oxaloacetate, and glutamate from alpha-ketoglutarate. Unlike many amino acids, branched-chain amino acid transamination occurs throughout the body, particularly in skeletal muscle. Here the main recipients of amino nitrogen are alanine and glutamine (from pyruvate and glutamate, respectively), which then pass into the circulation. These serve as important carriers of nitrogen from the periphery (skeletal muscle) to the intestine and liver. In the small intestine, glutamine is extracted and metabolized to ammonia, alanine, and citrulline, which are then conveyed to the liver via the portal circulation. Nitrogen is also removed from amino acids by deamination reactions, which result in the formation of ammonia. A number of amino acids can be deaminated, either directly (histidine), by dehydration (serine, threonine), by way of the purine nucleotide cycle (aspartate), or by oxidative deamination (glutamate). ... Glutamate is also formed in the specific degradation pathways of arginine and lysine. Thus, nitrogen from any amino acid can be funneled into the two precursors of urea synthesis, ammonia and aspartate. /Amino acids/
来源:Hazardous Substances Data Bank (HSDB)
安全信息
-
TSCA:Yes
-
危险品标志:Xi
-
安全说明:S24/25
-
WGK Germany:3
-
海关编码:2922411000
-
危险品运输编号:NONH for all modes of transport
-
RTECS号:OL5540000
-
危险性防范说明:P261,P305+P351+P338
-
危险性描述:H315,H319,H335
-
储存条件:本品应密封在0℃以下的干燥环境中保存。
SDS
1.1 产品标识符
: L-赖氨酸
产品名称
1.2 鉴别的其他方法
无数据资料
1.3 有关的确定了的物质或混合物的用途和建议不适合的用途
仅供科研用途,不作为药物、家庭备用药或其它用途。
模块 2. 危险性概述
2.1 GHS分类
根据化学品全球统一分类与标签制度(GHS)的规定,不是危险物质或混合物。
2.3 其它危害物 - 无
模块 3. 成分/组成信息
3.1 物 质
: C6H14N2O2
分子式
: 146.19 g/mol
分子量
无
模块 4. 急救措施
4.1 必要的急救措施描述
吸入
如果吸入,请将患者移到新鲜空气处。 如果停止了呼吸,给于人工呼吸。
皮肤接触
用肥皂和大量的水冲洗。
眼睛接触
用水冲洗眼睛作为预防措施。
食入
切勿给失去知觉者从嘴里喂食任何东西。 用水漱口。
4.2 主要症状和影响,急性和迟发效应
据我们所知,此化学,物理和毒性性质尚未经完整的研究。
4.3 及时的医疗处理和所需的特殊处理的说明和指示
无数据资料
模块 5. 消防措施
5.1 灭火介质
灭火方法及灭火剂
用水雾,耐醇泡沫,干粉或二氧化碳灭火。
5.2 源于此物质或混合物的特别的危害
碳氧化物, 氮氧化物
5.3 给消防员的建议
如必要的话,戴自给式呼吸器去救火。
5.4 进一步信息
无数据资料
模块 6. 泄露应急处理
6.1 人员的预防,防护设备和紧急处理程序
防止粉尘的生成。 防止吸入蒸汽、气雾或气体。
6.2 环境保护措施
不要让产物进入下水道。
6.3 抑制和清除溢出物的方法和材料
扫掉和铲掉。 存放进适当的闭口容器中待处理。
6.4 参考其他部分
丢弃处理请参阅第13节。
模块 7. 操作处置与储存
7.1 安全操作的注意事项
在有粉尘生成的地方,提供合适的排风设备。
7.2 安全储存的条件,包括任何不兼容性
贮存在阴凉处。 容器保持紧闭,储存在干燥通风处。
强烈地吸湿
7.3 特定用途
无数据资料
模块 8. 接触控制和个体防护
8.1 容许浓度
最高容许浓度
没有已知的国家规定的暴露极限。
8.2 暴露控制
适当的技术控制
常规的工业卫生操作。
个体防护设备
眼/面保护
请使用经官方标准如NIOSH (美国) 或 EN 166(欧盟) 检测与批准的设备防护眼部。
皮肤保护
戴手套取 手套在使用前必须受检查。
请使用合适的方法脱除手套(不要接触手套外部表面),避免任何皮肤部位接触此产品.
使用后请将被污染过的手套根据相关法律法规和有效的实验室规章程序谨慎处理. 请清洗并吹干双手
所选择的保护手套必须符合EU的89/686/EEC规定和从它衍生出来的EN 376标准。
身体保护
根据危险物质的类型,浓度和量,以及特定的工作场所来选择人体保护措施。,
防护设备的类型必须根据特定工作场所中的危险物的浓度和含量来选择。
呼吸系统防护
不需要保护呼吸。如需防护粉尘损害,请使用N95型(US)或P1型(EN 143)防尘面具。
呼吸器使用经过测试并通过政府标准如NIOSH(US)或CEN(EU)的呼吸器和零件。
模块 9. 理化特性
9.1 基本的理化特性的信息
a) 外观与性状
形状: 固体
b) 气味
无数据资料
c) 气味阈值
无数据资料
d) pH值
无数据资料
e) 熔点/凝固点
215 °C - 加热时分解。
f) 起始沸点和沸程
无数据资料
g) 闪点
无数据资料
h) 蒸发速率
无数据资料
i) 易燃性(固体,气体)
无数据资料
j) 高的/低的燃烧性或爆炸性限度 无数据资料
k) 蒸汽压
无数据资料
l) 蒸汽密度
无数据资料
m) 相对密度
无数据资料
n) 水溶性
无数据资料
o) n-辛醇/水分配系数
无数据资料
p) 自燃温度
无数据资料
q) 分解温度
无数据资料
r) 粘度
无数据资料
模块 10. 稳定性和反应活性
10.1 反应性
无数据资料
10.2 稳定性
无数据资料
10.3 危险反应的可能性
无数据资料
10.4 应避免的条件
无数据资料
10.5 不兼容的材料
强氧化剂
10.6 危险的分解产物
其它分解产物 - 无数据资料
模块 11. 毒理学资料
11.1 毒理学影响的信息
急性毒性
无数据资料
皮肤刺激或腐蚀
无数据资料
眼睛刺激或腐蚀
无数据资料
呼吸道或皮肤过敏
无数据资料
生殖细胞突变性
无数据资料
致癌性
IARC:
此产品中没有大于或等于 0。1%含量的组分被 IARC鉴别为可能的或肯定的人类致癌物。
生殖毒性
无数据资料
特异性靶器官系统毒性(一次接触)
无数据资料
特异性靶器官系统毒性(反复接触)
无数据资料
吸入危险
无数据资料
潜在的健康影响
吸入 吸入可能有害。 可能引起呼吸道刺激。
摄入 如服入是有害的。
皮肤 如果通过皮肤吸收可能是有害的。 可能引起皮肤刺激。
眼睛 可能引起眼睛刺激。
接触后的征兆和症状
据我们所知,此化学,物理和毒性性质尚未经完整的研究。
附加说明
化学物质毒性作用登记: OL5540000
模块 12. 生态学资料
12.1 生态毒性
无数据资料
12.2 持久存留性和降解性
无数据资料
12.3 潜在的生物蓄积性
无数据资料
12.4 土壤中的迁移性
无数据资料
12.5 PBT 和 vPvB的结果评价
无数据资料
12.6 其它不利的影响
无数据资料
模块 13. 废弃处置
13.1 废物处理方法
产品
将剩余的和未回收的溶液交给处理公司。
受污染的容器和包装
作为未用过的产品弃置。
模块 14. 运输信息
14.1 联合国危险货物编号
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.2 联合国(UN)规定的名称
欧洲陆运危规: 非危险货物
国际海运危规: 非危险货物
国际空运危规: 非危险货物
14.3 运输危险类别
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.4 包裹组
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.5 环境危险
欧洲陆运危规: 否 国际海运危规 海运污染物: 否 国际空运危规: 否
14.6 对使用者的特别提醒
无数据资料
模块 15 - 法规信息
N/A
模块16 - 其他信息
N/A
: L-赖氨酸
产品名称
1.2 鉴别的其他方法
无数据资料
1.3 有关的确定了的物质或混合物的用途和建议不适合的用途
仅供科研用途,不作为药物、家庭备用药或其它用途。
模块 2. 危险性概述
2.1 GHS分类
根据化学品全球统一分类与标签制度(GHS)的规定,不是危险物质或混合物。
2.3 其它危害物 - 无
模块 3. 成分/组成信息
3.1 物 质
: C6H14N2O2
分子式
: 146.19 g/mol
分子量
无
模块 4. 急救措施
4.1 必要的急救措施描述
吸入
如果吸入,请将患者移到新鲜空气处。 如果停止了呼吸,给于人工呼吸。
皮肤接触
用肥皂和大量的水冲洗。
眼睛接触
用水冲洗眼睛作为预防措施。
食入
切勿给失去知觉者从嘴里喂食任何东西。 用水漱口。
4.2 主要症状和影响,急性和迟发效应
据我们所知,此化学,物理和毒性性质尚未经完整的研究。
4.3 及时的医疗处理和所需的特殊处理的说明和指示
无数据资料
模块 5. 消防措施
5.1 灭火介质
灭火方法及灭火剂
用水雾,耐醇泡沫,干粉或二氧化碳灭火。
5.2 源于此物质或混合物的特别的危害
碳氧化物, 氮氧化物
5.3 给消防员的建议
如必要的话,戴自给式呼吸器去救火。
5.4 进一步信息
无数据资料
模块 6. 泄露应急处理
6.1 人员的预防,防护设备和紧急处理程序
防止粉尘的生成。 防止吸入蒸汽、气雾或气体。
6.2 环境保护措施
不要让产物进入下水道。
6.3 抑制和清除溢出物的方法和材料
扫掉和铲掉。 存放进适当的闭口容器中待处理。
6.4 参考其他部分
丢弃处理请参阅第13节。
模块 7. 操作处置与储存
7.1 安全操作的注意事项
在有粉尘生成的地方,提供合适的排风设备。
7.2 安全储存的条件,包括任何不兼容性
贮存在阴凉处。 容器保持紧闭,储存在干燥通风处。
强烈地吸湿
7.3 特定用途
无数据资料
模块 8. 接触控制和个体防护
8.1 容许浓度
最高容许浓度
没有已知的国家规定的暴露极限。
8.2 暴露控制
适当的技术控制
常规的工业卫生操作。
个体防护设备
眼/面保护
请使用经官方标准如NIOSH (美国) 或 EN 166(欧盟) 检测与批准的设备防护眼部。
皮肤保护
戴手套取 手套在使用前必须受检查。
请使用合适的方法脱除手套(不要接触手套外部表面),避免任何皮肤部位接触此产品.
使用后请将被污染过的手套根据相关法律法规和有效的实验室规章程序谨慎处理. 请清洗并吹干双手
所选择的保护手套必须符合EU的89/686/EEC规定和从它衍生出来的EN 376标准。
身体保护
根据危险物质的类型,浓度和量,以及特定的工作场所来选择人体保护措施。,
防护设备的类型必须根据特定工作场所中的危险物的浓度和含量来选择。
呼吸系统防护
不需要保护呼吸。如需防护粉尘损害,请使用N95型(US)或P1型(EN 143)防尘面具。
呼吸器使用经过测试并通过政府标准如NIOSH(US)或CEN(EU)的呼吸器和零件。
模块 9. 理化特性
9.1 基本的理化特性的信息
a) 外观与性状
形状: 固体
b) 气味
无数据资料
c) 气味阈值
无数据资料
d) pH值
无数据资料
e) 熔点/凝固点
215 °C - 加热时分解。
f) 起始沸点和沸程
无数据资料
g) 闪点
无数据资料
h) 蒸发速率
无数据资料
i) 易燃性(固体,气体)
无数据资料
j) 高的/低的燃烧性或爆炸性限度 无数据资料
k) 蒸汽压
无数据资料
l) 蒸汽密度
无数据资料
m) 相对密度
无数据资料
n) 水溶性
无数据资料
o) n-辛醇/水分配系数
无数据资料
p) 自燃温度
无数据资料
q) 分解温度
无数据资料
r) 粘度
无数据资料
模块 10. 稳定性和反应活性
10.1 反应性
无数据资料
10.2 稳定性
无数据资料
10.3 危险反应的可能性
无数据资料
10.4 应避免的条件
无数据资料
10.5 不兼容的材料
强氧化剂
10.6 危险的分解产物
其它分解产物 - 无数据资料
模块 11. 毒理学资料
11.1 毒理学影响的信息
急性毒性
无数据资料
皮肤刺激或腐蚀
无数据资料
眼睛刺激或腐蚀
无数据资料
呼吸道或皮肤过敏
无数据资料
生殖细胞突变性
无数据资料
致癌性
IARC:
此产品中没有大于或等于 0。1%含量的组分被 IARC鉴别为可能的或肯定的人类致癌物。
生殖毒性
无数据资料
特异性靶器官系统毒性(一次接触)
无数据资料
特异性靶器官系统毒性(反复接触)
无数据资料
吸入危险
无数据资料
潜在的健康影响
吸入 吸入可能有害。 可能引起呼吸道刺激。
摄入 如服入是有害的。
皮肤 如果通过皮肤吸收可能是有害的。 可能引起皮肤刺激。
眼睛 可能引起眼睛刺激。
接触后的征兆和症状
据我们所知,此化学,物理和毒性性质尚未经完整的研究。
附加说明
化学物质毒性作用登记: OL5540000
模块 12. 生态学资料
12.1 生态毒性
无数据资料
12.2 持久存留性和降解性
无数据资料
12.3 潜在的生物蓄积性
无数据资料
12.4 土壤中的迁移性
无数据资料
12.5 PBT 和 vPvB的结果评价
无数据资料
12.6 其它不利的影响
无数据资料
模块 13. 废弃处置
13.1 废物处理方法
产品
将剩余的和未回收的溶液交给处理公司。
受污染的容器和包装
作为未用过的产品弃置。
模块 14. 运输信息
14.1 联合国危险货物编号
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.2 联合国(UN)规定的名称
欧洲陆运危规: 非危险货物
国际海运危规: 非危险货物
国际空运危规: 非危险货物
14.3 运输危险类别
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.4 包裹组
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.5 环境危险
欧洲陆运危规: 否 国际海运危规 海运污染物: 否 国际空运危规: 否
14.6 对使用者的特别提醒
无数据资料
模块 15 - 法规信息
N/A
模块16 - 其他信息
N/A
制备方法与用途
性状
赖氨酸呈现白色粉末状态。
简介赖氨酸是人体必需氨基酸之一,有助于促进人体发育、增强免疫功能,并提高中枢神经组织的功能。它是一种碱性必需氨基酸。由于谷物食品中赖氨酸含量较低且容易在加工过程中被破坏而缺乏,因此被称为第一限制性氨基酸。
用途 制备游离L-赖氨酸固体的制备过程如下:取1.00千克L-赖氨酸盐酸盐,加入5.0升纯化水搅拌溶解,澄清后将溶液缓慢注入7.20千克活化的强酸性阳离子交换树脂柱上。用纯化水冲洗约2-3小时直至中性和无氯离子(通过硝酸银和广泛pH试纸检测)。再以11.1升5%氨水冲洗树脂柱,同样缓慢冲洗2-3小时并监测pH值大于10时开始收集碱性洗脱液。继续此过程直至pH值减小到约10停止收集。将收集的溶液在60℃(-0.10~-0.08Mpa)条件下减压浓缩,直到无液滴滴出为止。继续浓缩至变成白色固体。加入8升无水乙醇进行打浆析晶操作3小时,直至所有固体析出。离心过滤收集固体,直至无液滴流出。将滤饼铺在搪瓷托盘上,在60±5℃(-0.08~-0.1Mpa)条件下真空干燥8小时后冷却至室温,密封袋密封保存,最终得到776克游离L-赖氨酸固体,收率96.95%。
食品添加剂最大允许使用量及残留标准L-赖氨酸作为食品用香料时,各香料成分不得超过在GB 2760中的最大允许使用量和最大允许残留量。实际应用中应遵循相关法规要求。
化学性质L-赖氨酸是一种白色或近白色的自由流动结晶性粉末,几乎无气味。熔点为238℃。它具有游离氨基而容易发黄变质并带有刺激性腥味,但L-赖氨酸盐酸盐相对稳定不易潮解。
用途 生产方法通常以L-赖氨酸盐酸盐供应市场。通过红血球为原料制备时,将其悬浮于硫酸溶液中,并用氢氧化钙沉淀、水洗后苦味酸溶解结晶获得产品。也可以通过发酵法生产,包括两步法和一步法。合成法则有己内酰胺或糠醛为原料的两种方法。
用途- 作为食品强化剂及营养增补剂。
- 改善某些药物性能,提高药效。
上下游信息
-
上游原料
中文名称 英文名称 CAS号 化学式 分子量 DL-赖氨酸 2,6-diaminocaproic acid —— C6H14N2O2 146.189 D-赖氨酸 D-lysine 923-27-3 C6H14N2O2 146.189 —— (2R,6S)-2,6-diaminoheptanedioic acid —— C7H14N2O4 190.199 2,6-二氨基庚二酸 2,6-diaminopimelic acid 583-93-7 C7H14N2O4 190.199 (6S,2S)-二氨基庚二酸 (S,S)-2,6-diaminopimelic acid 14289-34-0 C7H14N2O4 190.199 —— 6,6-Dimethyl lysine —— C8H18N2O2 174.24 L-2-氨基己二酸 L-homoglutamic acid 1118-90-7 C6H11NO4 161.158 DL-a-氨基己二酸 (R,S)-2-aminoadipic acid 542-32-5 C6H11NO4 161.158 N-ε-羧甲基-L-赖氨酸 N6-carboxymethyllysine 5746-04-3 C8H16N2O4 204.226 L-鸟氨酸 L-ornithine 70-26-8 C5H12N2O2 132.162 D-鸟氨酸 D-ornithine 348-66-3 C5H12N2O2 132.162 L-赖氨酸乙酯 L-Lysine ethyl ester 4117-33-3 C8H18N2O2 174.243 DL-亮氨酸 LEUCINE 328-39-2 C6H13NO2 131.175 L-亮氨酸 L-leucine 61-90-5 C6H13NO2 131.175 (2S)-2-氨基-6-[(2-羟基-1-甲基-2-氧代-乙基)氨基]己酸 Nε-(carboxyethyl)lysine 5746-03-2 C9H18N2O4 218.253 L-谷氨酸 L-glutamic acid 56-86-0 C5H9NO4 147.131 L-赖氨酸正丙酯 L-lysine n-propyl ester 57590-09-7 C9H20N2O2 188.27 —— isoleucine 443-79-8 C6H13NO2 131.175 L-异亮氨酸 L-isoleucine 73-32-5 C6H13NO2 131.175 D-异亮氨酸 D-Isoleucine 319-78-8 C6H13NO2 131.175 L-谷氨酰胺 L-glutamine 56-85-9 C5H10N2O3 146.146 - 1
- 2
- 3
-
下游产品
中文名称 英文名称 CAS号 化学式 分子量 DL-赖氨酸 2,6-diaminocaproic acid —— C6H14N2O2 146.189 (2S)-2-氨基-6-甲基氨基己酸 Nε-Monomethyl-L-lysin 1188-07-4 C7H16N2O2 160.216 —— N6-hydroxy-L-lysine —— C6H14N2O3 162.189 L-6-羟基正亮氨酸 (S)-2-amino-6-hydroxyhexanoic acid 6033-32-5 C6H13NO3 147.174 N6,N6-二甲基-L-赖氨酸 Nε,Nε-dimethyl-L-lysine 2259-86-1 C8H18N2O2 174.243 Nε-甲酰基-L-赖氨酸 N(ε)-Formyl-L-lysin 1190-48-3 C7H14N2O3 174.2 —— deoxyhypusine 82543-85-9 C10H23N3O2 217.312 L-2-氨基己二酸 L-homoglutamic acid 1118-90-7 C6H11NO4 161.158 L-赖氨酸甲酯 L-LysOMe 687-64-9 C7H16N2O2 160.216 —— (2S,5S)-5-hydroxylysine 18899-29-1 C6H14N2O3 162.189 赤藓-5-羟基-L-赖氨酸 (5R)-5-hydroxy-L-lysine 1190-94-9 C6H14N2O3 162.189 高精氨酸 L-homoarginine 156-86-5 C7H16N4O2 188.23 N-ε-羧甲基-L-赖氨酸 N6-carboxymethyllysine 5746-04-3 C8H16N2O4 204.226 N-EPSILON-乙酰-L-赖胺基乙酸 H-Lys(acetyl)-OH 692-04-6 C8H16N2O3 188.227 L-鸟氨酸 L-ornithine 70-26-8 C5H12N2O2 132.162 —— 5-bromolysine —— C6H13BrN2O2 225.085 —— 4-hydroxylysine 15574-69-3 C6H14N2O3 162.189 —— (2S,4S)-2,6-diamino-4-hydroxyhexanoic acid —— C6H14N2O3 162.189 —— (4R)-4-hydroxy-L-lysine 60594-62-9 C6H14N2O3 162.189 —— L-Lys(n-PrCO) —— C10H20N2O3 216.28 —— threo-γ-Chlor-lysin = L-(+)-4-Chlor-2,6-diamino-capronsaeure —— C6H13ClN2O2 180.634 —— 4-chloro-L-lysine —— C6H13ClN2O2 180.634 —— Lysine(butyryl)-oh (H-L-Lys(Butanoyl)-OH) —— C11H22N2O3 230.307 —— Nε-monohexanoyl-L-lysine 30664-73-4 C12H24N2O3 244.334 L-赖氨酸乙酯 L-Lysine ethyl ester 4117-33-3 C8H18N2O2 174.243 L-亮氨酸 L-leucine 61-90-5 C6H13NO2 131.175 D-亮氨酸 (R)-leucine 328-38-1 C6H13NO2 131.175 —— (2S,3S)-3-hydroxylysine 1613640-71-3 C6H14N2O3 162.189 —— Nε-acryloyl-L-lysine 48065-82-3 C9H16N2O3 200.238 (2S)-2-氨基-6-[(2-羟基-1-甲基-2-氧代-乙基)氨基]己酸 Nε-(carboxyethyl)lysine 5746-03-2 C9H18N2O4 218.253 —— L-NMMHA 75830-53-4 C8H18N4O2 202.257 N6-(2-碘乙酰基)-L-赖氨酸 (+)-S-2-amino-6-iodoacetamidohexanoic acid 90764-56-0 C8H15IN2O3 314.123 —— β-lysine 504-21-2 C6H14N2O2 146.189 —— (R)-β-lysine 51703-81-2 C6H14N2O2 146.189 —— Nα-formyl-L-lysine 19729-28-3 C7H14N2O3 174.2 N6-(1-氧代十六烷基)-L-赖氨酸 palmitoyl-(S)-lysine 59012-43-0 C22H44N2O3 384.603 N6-(1-氧代辛基)-L-赖氨酸 Nε-octanoyl-L-lysine 23735-96-8 C14H28N2O3 272.388 N-(十二酰基)赖氨酸 Nε-lauroyl-L-lysine 52315-75-0 C18H36N2O3 328.495 DL-谷氨酸 Glutamic acid 617-65-2 C5H9NO4 147.131 L-谷氨酸 L-glutamic acid 56-86-0 C5H9NO4 147.131 Nα,Nα,Nε,Nε-四甲基赖氨酸 Nα,Nα,Nε,Nε-tetramethyllysine 92175-43-4 C10H22N2O2 202.297 L-赖氨酸正丙酯 L-lysine n-propyl ester 57590-09-7 C9H20N2O2 188.27 N-epsilon磷酰赖氨酸 ε-phospholysine 14721-74-5 C6H15N2O5P 226.169 —— (2S)-2-amino-6-(pent-4-enamido)hexanoic acid 1378237-14-9 C11H20N2O3 228.291 —— L-lysine 21653-99-6 C6H14N2O 130.19 L-赖氨酸正丁酯 L-lysine n-butyl ester 2885-12-3 C10H22N2O2 202.297 —— N6-(1-imino-3-butenyl)-L-lysine —— C10H19N3O2 213.28 L-异亮氨酸 L-isoleucine 73-32-5 C6H13NO2 131.175 来沙尔 S-lysinol 12772-68-8 C6H16N2O 132.206 —— (S)-2,6-Diamino-hexanoic acid octyl ester 16011-73-7 C14H30N2O2 258.404 —— n6-(2-Chloroethylcarbamoyl)lysine 14851-86-6 C9H18ClN3O3 251.713 六氢吡啶-alpha-羧酸 Pipecolic Acid 535-75-1 C6H11NO2 129.159 L-哌啶-2-甲酸 pipecolinic acid 3105-95-1 C6H11NO2 129.159 D-哌啶-2-甲酸 (R)-(+)-pipecolic acid 1723-00-8 C6H11NO2 129.159 —— ε-N-oxalyllysine 5238-83-5 C8H14N2O5 218.21 L-谷氨酰胺 L-glutamine 56-85-9 C5H10N2O3 146.146 三氟乙酰赖氨酸 (S)-6-trifluoroacetylamino-2-aminohexanoic acid 10009-20-8 C8H13F3N2O3 242.198 (+/-)-2-氨基-7-膦酰庚酸 AP-7 85797-13-3 C7H16NO5P 225.181 —— Nε-(Trichloroacetyl)-L-lysine —— C8H13Cl3N2O3 291.562 - 1
- 2
- 3
- 4
- 5
- 6
反应信息
-
作为反应物:描述:L-赖氨酸 在 sodium azide 、 ammonium iron(II) sulfate hexahydrate 、 氧气 、 HalB from Streptomyces wuyuanensis 、 sodium α-ketoglutarate 、 sodium ascorbate 作用下, 以 aq. acetate buffer 为溶剂, 反应 1.0h, 生成 5-azidolysine参考文献:名称:[EN] METHODS FOR SELECTIVELY MODIFYING AMINO ACIDS AND PRODUCTS MADE THEREBY
[FR] PROCÉDÉS DE MODIFICATION SÉLECTIVE D'ACIDES AMINÉS ET PRODUITS FABRIQUÉS PAR CEUX-CI摘要:本文披露了一种选择性替代化合物中与碳原子结合的氢(例如,脂肪族亚甲基基团的氢)的方法,包括在BesD卤素酶存在的情况下将化合物与取代基接触。公开号:WO2021007127A1 -
作为产物:参考文献:名称:手性氨基酸与 (S)-(-)-1-苯基乙磺酸的非对映异构盐的光学分辨率、表征和 X 射线晶体结构摘要:10 种 DL-氨基酸 (AA),包括中性和碱性氨基酸,以及一种亚氨基酸,通过它们与 (-)-1-苯基乙磺酸的非对映异构盐的分级结晶进行光学拆分,无需衍生为它们的共价化合物各种溶剂中的酸 (PES)。对拆分过程中形成的几对非对映体结晶盐进行了 DSC 和光谱分析,结果表明拆分成功的原因是溶解度较高的 D-AA·(-)-PES 和溶解度较低的L-AA·(-)-PES。通过比较 D- 和 L-HPG·(-)-PES 的 X 射线晶体结构,探索了对最成功解析的物质 DL-p-羟基苯基甘氨酸 (HPG) 盐的手性识别。DOI:10.1246/bcsj.67.3012
-
作为试剂:参考文献:名称:A green method for the self-aldol condensation of aldehydes using lysine摘要:在特定乳液条件下,通过赖氨酸的催化作用,在水或无溶剂体系中,方便地实现了醛的自缩合,获得了良好产率的α-支链α,β-不饱和醛。DOI:10.1039/b918349c
文献信息
-
Champacyclin, a New Cyclic Octapeptide from Streptomyces Strain C42 Isolated from the Baltic Sea作者:Alexander Pesic、Heike Baumann、Katrin Kleinschmidt、Paul Ensle、Jutta Wiese、Roderich Süssmuth、Johannes ImhoffDOI:10.3390/md11124834日期:——champacyclin (1a) present in all three strains. Herein, we report on the isolation, structure elucidation and determination of the absolute stereochemistry of this isoleucine/leucine (Ile/Leu = Xle) rich cyclic octapeptide champacyclin (1a). As 2D nuclear magnetic resonance (NMR) spectroscopy could not fully resolve the structure of (1a), additional information on sequence and configuration of stereocenters从哥特兰深海(波罗的海)、乌拉尼亚盆地(地中海东部)和基尔湾(波罗的海)的海洋沉积物中分离出新的 Streptomyces champavatii 分离株。这些分离株产生了几种寡肽次生代谢物,包括所有三种菌株中都存在的新八肽尚帕环素 (1a)。在此,我们报告了这种富含异亮氨酸/亮氨酸 (Ile/Leu = Xle) 的环状八肽香槟环素 (1a) 的绝对立体化学的分离、结构解析和测定。由于二维核磁共振 (NMR) 光谱无法完全解析 (1a) 的结构,因此通过多级质谱 (MSn) 研究、氨基酸分析、部分水解和随后的对映体分析采用气相色谱正化学电离/电子轰击质谱 (GC-PCI/EI-MS),并与参考二肽进行比较。与选择性侧链环化衍生物 (2) 相比,通过固相肽合成 (SPPS) 证明了 (1a) 的头对尾环化。尚帕环素 (1a) 可能由非核糖体肽合成酶 (NRPS) 合成,因为其 (D)-氨基
-
[EN] NOVEL COMPOUNDS, THEIR PREPARATION AND USE<br/>[FR] NOUVEAUX COMPOSES, LEUR PREPARATION ET LEUR UTILISATION申请人:NOVO NORDISK AS公开号:WO2005105736A1公开(公告)日:2005-11-10Novel compounds of the general formula (I), the use of these compounds as phar- maceutical compositions, pharmaceutical compositions comprising the compounds and methods of treatment employing these compounds and compositions. The present compounds may be useful in the treatment and/or prevention of conditions mediated by Peroxisome Proliferator-Activated Receptors (PPAR), in particular the PPARδ suptype.
-
[EN] A CONJUGATE OF A TUBULYSIN ANALOG WITH BRANCHED LINKERS<br/>[FR] CONJUGUÉ D'UN ANALOGUE DE TUBULYSINE AVEC DES LIEURS RAMIFIÉS申请人:HANGZHOU DAC BIOTECH CO LTD公开号:WO2019127607A1公开(公告)日:2019-07-04The present invention relates to the conjugation of a tubulysin analog compound to a cell-binding molecule with branched/side-chain linkers for having better delivery of the conjugate compound and targeted treatment of abnormal cells. It also relates to a branched-linkage method of conjugation of a tubulysin analog molecule to a cell-binding ligand, as well as methods of using the conjugate in targeted treatment of cancer, infection and autoimmune disease.本发明涉及将一种管腔霉素类似物化合物与具有分支/侧链连接物的细胞结合分子结合,以实现结合物的更好传递和靶向治疗异常细胞。它还涉及一种将管腔霉素类似物分子与细胞结合配体结合的分支连接方法,以及在靶向治疗癌症、感染和自身免疫疾病中使用结合物的方法。
-
Synthèse d'analogues structuraux de l'élédoïsine. 1<sup>re</sup>partie: Préparation des produits intermédiaires作者:Ed. Sandrin、R. A. BoissonnasDOI:10.1002/hlca.19630460518日期:——The preparation of new dipeptides and tripeptides, which are useful intermediates in the synthesis of Eledoisin analogues, is described.描述了新的二肽和三肽的制备,它们是Eledoisin类似物合成中的有用中间体。
-
Enantioselective Enzymatic Cleavage of N-Benzyloxycarbonyl Groups作者:Ramesh N. Patel、Venkata Nanduri、David Brzozowski、Clyde McNamee、Amit BanerjeeDOI:10.1002/adsc.200303038日期:2003.6A new enzymatic process for the enantioselective cleavage of N-benzyloxycarbonyl (Cbz) groups from protected amino acids and related compounds has been developed. The Cbz-deprotecting enzyme was isolated from cell extracts of Sphingomonas paucimobilis SC 16113 and purified to homogeneity. The purified protein has a molecular weight of 155,000 daltons and a subunit size of 44,000 daltons.
表征谱图
-
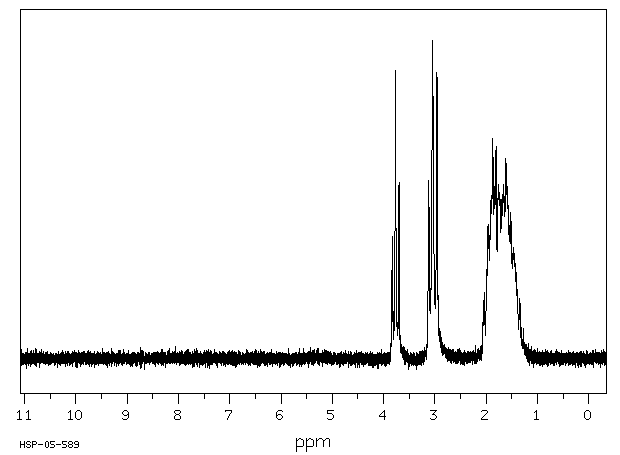
氢谱1HNMR
-
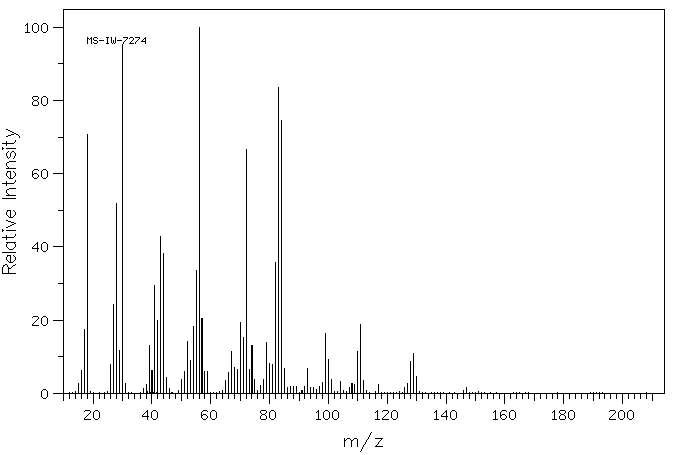
质谱MS
-
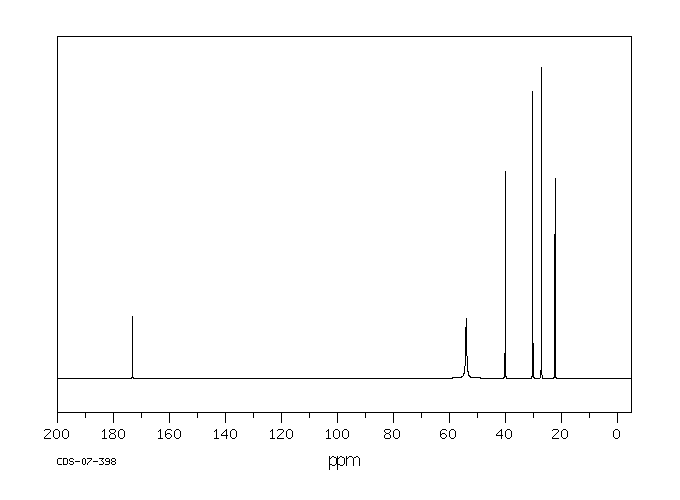
碳谱13CNMR
-
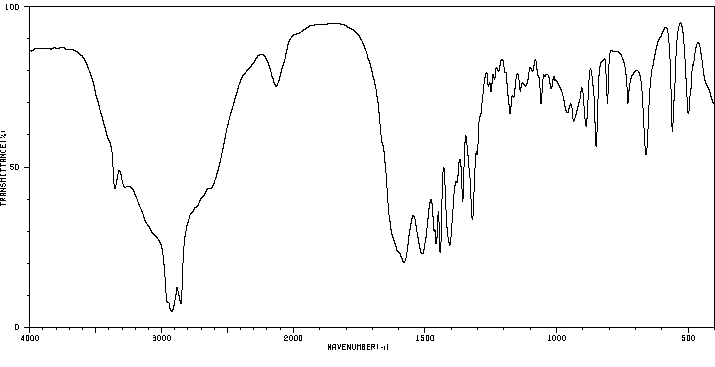
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息
同类化合物
(甲基3-(二甲基氨基)-2-苯基-2H-azirene-2-羧酸乙酯)
(±)-盐酸氯吡格雷
(±)-丙酰肉碱氯化物
(d(CH2)51,Tyr(Me)2,Arg8)-血管加压素
(S)-(+)-α-氨基-4-羧基-2-甲基苯乙酸
(S)-阿拉考特盐酸盐
(S)-赖诺普利-d5钠
(S)-2-氨基-5-氧代己酸,氢溴酸盐
(S)-2-[[[(1R,2R)-2-[[[3,5-双(叔丁基)-2-羟基苯基]亚甲基]氨基]环己基]硫脲基]-N-苄基-N,3,3-三甲基丁酰胺
(S)-2-[3-[(1R,2R)-2-(二丙基氨基)环己基]硫脲基]-N-异丙基-3,3-二甲基丁酰胺
(S)-1-(4-氨基氧基乙酰胺基苄基)乙二胺四乙酸
(S)-1-[N-[3-苯基-1-[(苯基甲氧基)羰基]丙基]-L-丙氨酰基]-L-脯氨酸
(R)-乙基N-甲酰基-N-(1-苯乙基)甘氨酸
(R)-丙酰肉碱-d3氯化物
(R)-4-N-Cbz-哌嗪-2-甲酸甲酯
(R)-3-氨基-2-苄基丙酸盐酸盐
(R)-1-(3-溴-2-甲基-1-氧丙基)-L-脯氨酸
(N-[(苄氧基)羰基]丙氨酰-N〜5〜-(diaminomethylidene)鸟氨酸)
(6-氯-2-吲哚基甲基)乙酰氨基丙二酸二乙酯
(4R)-N-亚硝基噻唑烷-4-羧酸
(3R)-1-噻-4-氮杂螺[4.4]壬烷-3-羧酸
(3-硝基-1H-1,2,4-三唑-1-基)乙酸乙酯
(2S,4R)-Boc-4-环己基-吡咯烷-2-羧酸
(2S,3S,5S)-2-氨基-3-羟基-1,6-二苯己烷-5-N-氨基甲酰基-L-缬氨酸
(2S,3S)-3-((S)-1-((1-(4-氟苯基)-1H-1,2,3-三唑-4-基)-甲基氨基)-1-氧-3-(噻唑-4-基)丙-2-基氨基甲酰基)-环氧乙烷-2-羧酸
(2S)-2,6-二氨基-N-[4-(5-氟-1,3-苯并噻唑-2-基)-2-甲基苯基]己酰胺二盐酸盐
(2S)-2-氨基-N,3,3-三甲基-N-(苯甲基)丁酰胺
(2S)-2-氨基-3-甲基-N-2-吡啶基丁酰胺
(2S)-2-氨基-3,3-二甲基-N-(苯基甲基)丁酰胺,
(2S)-2-氨基-3,3-二甲基-N-2-吡啶基丁酰胺
(2S,4R)-1-((S)-2-氨基-3,3-二甲基丁酰基)-4-羟基-N-(4-(4-甲基噻唑-5-基)苄基)吡咯烷-2-甲酰胺盐酸盐
(2R,3'S)苯那普利叔丁基酯d5
(2R)-2-氨基-3,3-二甲基-N-(苯甲基)丁酰胺
(2-氯丙烯基)草酰氯
(1S,3S,5S)-2-Boc-2-氮杂双环[3.1.0]己烷-3-羧酸
(1R,5R,6R)-5-(1-乙基丙氧基)-7-氧杂双环[4.1.0]庚-3-烯-3-羧酸乙基酯
(1R,4R,5S,6R)-4-氨基-2-氧杂双环[3.1.0]己烷-4,6-二羧酸
齐特巴坦
齐德巴坦钠盐
齐墩果-12-烯-28-酸,2,3-二羟基-,苯基甲基酯,(2a,3a)-
齐墩果-12-烯-28-酸,2,3-二羟基-,羧基甲基酯,(2a,3b)-(9CI)
黄酮-8-乙酸二甲氨基乙基酯
黄荧菌素
黄体生成激素释放激素(1-6)
黄体生成激素释放激素 (1-5) 酰肼
黄体瑞林
麦醇溶蛋白
麦角硫因
麦芽聚糖六乙酸酯
麦根酸