去氧鬼臼毒素 | 19186-35-7
分子结构分类
中文名称
去氧鬼臼毒素
中文别名
去氧鬼臼脂素
英文名称
deoxypodophyllotoxin
英文别名
(-)-Deoxypodophyllotoxin;5R-5,8,8a,9-tetrahydro-5-(3,4,5-dimethoxyphenyl)furan(3',4':6,7)naphtho-[2,3-d]-1,3-dioxole-6(5aH)-one;4'-demethyldesoxypodophyllotoxin;(−)-deoxypodophyllotoxin;(-)-desoxypodophyllotoxin;(5R,5aR,8aR)-5-(3,4,5-trimethoxyphenyl)-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[5,6-f][1,3]benzodioxol-6-one
CAS
19186-35-7
化学式
C22H22O7
mdl
——
分子量
398.412
InChiKey
ZGLXUQQMLLIKAN-SVIJTADQSA-N
BEILSTEIN
——
EINECS
——
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
物化性质
-
溶解度:溶于氯仿、二氯甲烷、乙酸乙酯、DMSO、丙酮等。
-
沸点:564.5±50.0 °C(Predicted)
-
密度:1.304±0.06 g/cm3(Predicted)
-
熔点:168 °C
计算性质
-
辛醇/水分配系数(LogP):3.1
-
重原子数:29
-
可旋转键数:4
-
环数:5.0
-
sp3杂化的碳原子比例:0.41
-
拓扑面积:72.4
-
氢给体数:0
-
氢受体数:7
ADMET
代谢
去氧鬼臼毒素已知的人体代谢物包括6,7-二羟基-4-(3,4,5-三甲氧基苯基)-3a,4,9,9a-四氢-1H-苯并[f][2]苯并呋喃-3-酮,5-(4-羟基-3,5-二甲氧基苯基)-5a,8,8a,9-四氢-5H-[2]苯并呋喃[5,6-f][1,3]苯并二氧杂环戊-6-酮,以及5-羟基-9-(3,4,5-三甲氧基苯基)-5a,6,8a,9-四氢-5H-[2]苯并呋喃[5,6-f][1,3]苯并二氧杂环戊-8-酮。
Deoxypodophyllotoxin has known human metabolites that include 6,7-Dihydroxy-4-(3,4,5-trimethoxyphenyl)-3a,4,9,9a-tetrahydro-1H-benzo[f][2]benzofuran-3-one, 5-(4-Hydroxy-3,5-dimethoxyphenyl)-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[5,6-f][1,3]benzodioxol-6-one, and 5-hydroxy-9-(3,4,5-trimethoxyphenyl)-5a,6,8a,9-tetrahydro-5H-[2]benzofuro[5,6-f][1,3]benzodioxol-8-one.
来源:NORMAN Suspect List Exchange
安全信息
-
储存条件:存储条件:2-8℃,干燥且密封。
SDS
制备方法与用途
生物活性 Deoxypodophyllotoxin(DPT),鬼臼毒素的一种衍生物,是一种木酚素。它从Sinopodophyllexandrum的根茎中分离得到,并展现出强效的抗有丝分裂和抗病毒特性。作为一种靶向微管的药物,Deoxypodophyllotoxin不仅是有效的抗有丝分裂剂,还能作为血管生成抑制剂,在肿瘤学领域发挥重要作用。研究表明,该化合物能诱导细胞自噬(autophagy)和细胞凋亡(apoPTosis),并引起DRG神经元细胞内Ca2+浓度增加。
体外研究 Deoxypodophyllotoxin(浓度为25-75 nM;作用时间为6-48小时)显著增加了早期凋亡细胞的比例,从2.05%分别增长到24小时后的5.62%和48小时后的18.49%。此外,在SGC-7901细胞中,该化合物以时间和剂量依赖的方式导致G2/M期细胞周期阻滞,并显著下调了Cdc2和Cdc25C的表达水平,同时在6小时内上调cyclin B1表达,随后抑制了PARP、Bcl-2及caspase-3活性。
凋亡分析
- 细胞系:SGC-7901细胞
- 浓度:25, 50, 75 nM
- 培养时间:6, 12, 24, 48小时
- 结果:诱导SGC-7901细胞凋亡
细胞周期分析
- 细胞系:SGC-7901细胞
- 浓度:25, 50, 75 nM
- 培养时间:6, 12, 24, 48小时
- 结果:诱导SGC-7901细胞G2/M期阻滞
Western Blot分析
- 细胞系:SGC-7901细胞
- 浓度:25, 50, 75 nM
- 培养时间:6, 12, 24, 48小时
- 结果:改变了cyclin B1、Cdc2、Cdc25C、p-PARP、Bcl-2及p-caspase-3蛋白的表达水平
体内研究 Deoxypodophyllotoxin(静脉注射;剂量分别为5、10和20 mg/kg;每周三次,共28天)表现出剂量依赖性的肿瘤抑制作用。在裸鼠异种移植模型中,用SGC-7901细胞构建的胃癌肿瘤生长分别被抑制了22.19%、47.91%及50.93%。
实验结果
- 动物模型:裸鼠异种移植模型(使用SGC-7901细胞)
- 剂量:5, 10, 和20 mg/kg
- 给药方式:静脉注射;剂量分别为5、10和20 mg/kg,每周三次,共28天
- 结果:抑制了胃癌肿瘤的生长
化学性质 无色棱柱状结晶(无水乙醇中),可溶于甲醇、乙醇及DMSO等有机溶剂。该化合物来源于桃儿七Sinopodophyllexandrum和八角莲Dysosma versipellis 的根茎。
用途 去氧鬼臼毒素具有抗肿瘤活性。
上下游信息
-
上游原料
中文名称 英文名称 CAS号 化学式 分子量 —— deoxypicropodophyllin 24150-39-8 C22H22O7 398.412 —— (5R,5aR,8aR)-5-(3,4,5-trimethoxyphenyl)-5,5a,8a,9-tetrahydro-[2]benzofuro[5,6-f][1,3]benzodioxole-6,8-dione 160869-33-0 C22H20O8 412.396 —— 6,7-demethylenedeoxypodophyllotoxin 1173-42-8 C21H22O7 386.401 —— (5R,6R,7R)-5-(3,4,5-trimethoxyphenyl)-5,6,7,8-tetrahydrobenzo[f][1,3]benzodioxole-6,7-dicarboxylic acid 160823-61-0 C22H22O9 430.411 鬼臼脂毒酮 podophyllotoxone 477-49-6 C22H20O8 412.396 鬼臼毒素 podofilox 518-28-5 C22H22O8 414.412 —— bis[(1S)-2-methoxy-2-oxo-1-phenylethyl] (5R,6R,7R)-5-(3,4,5-trimethoxyphenyl)-5,6,7,8-tetrahydrobenzo[f][1,3]benzodioxole-6,7-dicarboxylate 160823-59-6 C40H38O13 726.734 —— bis[(1S)-2-methoxy-2-oxo-1-phenylethyl] (5R,6S,7R)-5-hydroxy-5-(3,4,5-trimethoxyphenyl)-7,8-dihydro-6H-benzo[f][1,3]benzodioxole-6,7-dicarboxylate 160823-58-5 C40H38O14 742.733 Yatein; (-)-反式-3-(3,4-亚甲基二氧基苄基)-2-(3,4,5-三甲氧基苄基)丁内酯 yatein 40456-50-6 C22H24O7 400.428 —— rac-4-{benzo[d][1,3]dioxol-5-yl(hydroxy)methyl}-3-(3,4,5-trimethoxybenzyl)dihydrofuran-2(3H)-one —— C22H24O8 416.428 —— (+)-γ-Apopicropodophyllin 668-01-9 C22H20O7 396.397 —— 1-(3',4',5'-trimethoxyphenyl)-1,2-dihydro-4,5-methylenedioxybenzocyclobuten-1-ol 134454-88-9 C18H18O6 330.337 - 1
- 2
-
下游产品
中文名称 英文名称 CAS号 化学式 分子量 —— deoxypicropodophyllin 24150-39-8 C22H22O7 398.412 4 ’-去甲去氧鬼臼毒素 4'-demethyl-4-deoxypodophyllotoxin 3590-93-0 C21H20O7 384.386 —— 3',4'-didemethyl-1-desoxypodophyllotoxin —— C20H18O7 370.359 —— 6,7-demethylenedeoxypodophyllotoxin 1173-42-8 C21H22O7 386.401 —— (3aS,4R,9aR)-6,7-dihydroxy-4-(3,4,5-trimethoxyphenyl)-3a,4,9,9a-tetrahydro-1H-benzo[f][2]benzofuran-3-one 3590-88-3 C21H22O7 386.401 —— desoxypodophyllinic acid ethyl ester 78215-95-9 C24H28O8 444.482 —— Desoxypodophyllinsaeure-methylester 1643-12-5 C23H26O8 430.455 —— deoxypicropodophyllinic acid methyl ester 140147-76-8 C23H26O8 430.455 —— 4'-demethyl-6,7-demethylenedesoxypodophyllotoxin —— C20H20O7 372.375 —— methyl (5R,6S,7R)-7-formyl-5-(3,4,5-trimethoxyphenyl)-5,6,7,8-tetrahydrobenzo[f][1,3]benzodioxole-6-carboxylate 171483-28-6 C23H24O8 428.439 —— ethyl (5R,6R,7R)-7-(methoxymethoxymethyl)-5-(3,4,5-trimethoxyphenyl)-5,6,7,8-tetrahydrobenzo[f][1,3]benzodioxole-6-carboxylate 514223-12-2 C26H32O9 488.535 —— 4'-demethyl-4'-O-benzyl-1-desoxypodophyllotoxin —— C28H26O7 474.51 —— deoxypicropodophyllic acid 1254-07-5 C22H24O8 416.428 —— [4-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-2,6-dimethoxyphenyl] N-ethylcarbamate 13091-61-7 C24H25NO8 455.464 盾叶鬼臼素 β-peltatin 518-29-6 C22H22O8 414.412 —— [4-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-2,6-dimethoxyphenyl] (Z)-octadec-11-enoate —— C39H52O8 648.837 —— 4'-O-trans-11-eicosenoyl-4'-demethyldeoxypodophyllotoxin —— C41H56O8 676.891 —— 4'-O-all-cis-5,8,11,14-eicosatetraenoyl-4'-demethyldeoxypodophyllotoxin —— C41H50O8 670.843 —— 4'-O-all-cis-11,14-eicosadienoyl-4'-demethyldeoxypodophyllotoxin —— C41H54O8 674.875 —— 4'-O-(diethylphosphoryl)-4'-demethyl-1-desoxypodophyllotoxin —— C25H29O10P 520.473 —— deoxyanhydro-4-isopodophyllol 321747-09-5 C22H24O6 384.429 6,8-二溴-4-氧代-4H-1-苯并吡喃-3-甲醛 9-deoxyanhydropodophyllol 25088-82-8 C22H24O6 384.429 —— 2-(4-deoxyl-4'-demethylpodophyllotoxinoxy)-N-phenylacetamide —— C29H27NO8 517.535 —— 4'-demethyl-4'-O-tert-butyldimethylsilyl-1-desoxypodophyllotoxin —— C27H34O7Si 498.648 —— 4'-demethyl-4-deoxypodophyllotoxin 4'-(4-methylpiperazine) carbamate 1308813-80-0 C27H30N2O8 510.544 —— 2-(4-deoxyl-4'-demethylpodophyllotoxinoxy)-N-(p-methoxyphenyl)acetamide —— C30H29NO9 547.562 —— 2-(4-deoxyl-4'-demethylpodophyllotoxinoxy)-N-(o-methylphenyl)acetamide —— C30H29NO8 531.562 鬼臼脂毒酮 podophyllotoxone 477-49-6 C22H20O8 412.396 (5R)-5,8,8ab,9-四氢-5b-(3,4,5-三甲氧基苯基)呋喃并[3',4':6,7]萘并[2,3-d]-1,3-二氧杂环戊烯-6(5abH),9-二酮 (5aR,8aS,9R)-9-(3,4,5-trimethoxyphenyl)-5a,6,8a,9-tetrahydrofuro[3',4':6,7]naphtho[2,3-d][1,3]dioxole-5,8-dione 477-48-5 C22H20O8 412.396 —— 2-(4-deoxyl-4'-demethylpodophyllotoxinoxy)-N-(m-fluorophenyl)acetamide —— C29H26FNO8 535.526 —— [(5R,6R,7R)-7-(methoxymethoxymethyl)-5-(3,4,5-trimethoxyphenyl)-5,6,7,8-tetrahydrobenzo[f][1,3]benzodioxol-6-yl]methanol 514223-09-7 C24H30O8 446.497 —— 2-(4-deoxyl-4'-demethylpodophyllotoxinoxy)-N-(m-chlorophenyl)acetamide —— C29H26ClNO8 551.98 5,8,8a,9-四氢-9-羟基-5-(3,4,5-三甲氧基苯基)-(5R,5aR,8aR,9S)-呋喃并[3',4':6,7]萘并[2,3-d]-1,3-二氧杂环戊烯-6(5aH)-酮 epipodophyllotoxin 4375-07-9 C22H22O8 414.412 鬼臼毒素 podofilox 518-28-5 C22H22O8 414.412 —— (6R,7R,8R)-6-(methoxymethoxymethyl)-7-methyl-8-(3,4,5-trimethoxyphenyl)-5,6,7,8-tetrahydrobenzo[f][1,3]benzodioxole 514223-13-3 C24H30O7 430.498 —— 9-deoxypodophyllol 31104-02-6 C22H26O7 402.444 —— 2-(4-deoxyl-4'-demethylpodophyllotoxinoxy)-N-(o-chlorophenyl)acetamide —— C29H26ClNO8 551.98 —— [(6R,7R,8R)-7-methyl-8-(3,4,5-trimethoxyphenyl)-5,6,7,8-tetrahydrobenzo[f][1,3]benzodioxol-6-yl]methanol 514223-14-4 C22H26O6 386.445 —— 1-bromo-desoxypodophyllotoxin —— C22H21BrO7 477.309 —— 1α-bromo-desoxypodophyllotoxin 106636-74-2 C22H21BrO7 477.309 —— 4β-bromo-4-desoxypodophyllotoxin 106636-74-2 C22H21BrO7 477.309 —— 6,7-O-Demethylen-epipodophyllotoxin 1174-96-5 C21H22O8 402.401 —— 2'-bromodeoxypodophyllotoxin 93108-13-5 C22H21BrO7 477.309 (3aR,4S,9R,9aR)-4,6,7-三羟基-9-(4-羟基-3,5-二甲氧苯基)-3a,4,9,9a-四氢萘并[2,3-c]呋喃-1(3H)-酮 6,7-O,O-demethylene-4'-O-demethylepipodophyllotoxin 138456-91-4 C20H20O8 388.374 —— 2-(4-deoxyl-4'-demethylpodophyllotoxinoxy)-N-(m-nitrophenyl)acetamide —— C29H26N2O10 562.533 —— 4'-demethyl-4-deoxypodophyllotoxin 4'-(4-p-hydroxyphenylpiperazine) carbamate 1308813-86-6 C32H32N2O9 588.614 —— 2-(4-deoxyl-4'-demethylpodophyllotoxinoxy)-N-(2-chloro-6-methylphenyl)acetamide —— C30H28ClNO8 566.007 —— 4'-demethyl-4-deoxypodophyllotoxin 4'-(4-p-fluorophenylpiperazine) carbamate 1308813-82-2 C32H31FN2O8 590.605 —— 2-(4-deoxyl-4'-demethylpodophyllotoxinoxy)-N-(o-nitrophenyl)acetamide —— C29H26N2O10 562.533 —— [(5R,6R,7R)-7-(methoxymethoxymethyl)-5-(3,4,5-trimethoxyphenyl)-5,6,7,8-tetrahydrobenzo[f][1,3]benzodioxol-6-yl]methyl methanesulfonate 514223-10-0 C25H32O10S 524.589 —— 4'-demethyl-4-deoxypodophyllotoxin 4'-(4-p-nitrophenylpiperazine) carbamate 1308813-81-1 C32H31N3O10 617.612 —— 6,7-demethylene-1-O-ethyl-1-epipodophyllotoxin —— C23H26O8 430.455 —— 6,7-demethylene-4'-demethyl-1-O-ethyl-1-epipodophyllotoxin —— C22H24O8 416.428 —— (5R,5aR,8aR)-5-(4-methoxyphenazin-2-yl)-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[5,6-f][1,3]benzodioxol-6-one 1445712-09-3 C26H20N2O5 440.455 (5R,5aR,8aR,9R)-9-羟基-10-甲氧基-5-(3,4,5-三甲氧基苯基)-5a,8,8a,9-四氢-5H-异苯并呋喃并[6,5-f][1,3]苯并二氧戊环-6-酮 5-methoxypodophyllotoxin 128443-52-7 C23H24O9 444.438 —— (5R,5aR,8aR)-5-(8-amino-4-methoxyphenazin-2-yl)-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[5,6-f][1,3]benzodioxol-6-one 1445712-13-9 C26H21N3O5 455.47 —— (5R,5aR,8aR)-5-(7-amino-4-methoxyphenazin-2-yl)-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[5,6-f][1,3]benzodioxol-6-one 1445712-12-8 C26H21N3O5 455.47 —— [4-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-2,6-dimethoxyphenyl] N-[(2S)-4-methylsulfanyl-1-[4-(4-nitrophenyl)piperazin-1-yl]-1-oxobutan-2-yl]carbamate 1308813-91-3 C37H40N4O11S 748.811 —— [4-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-2,6-dimethoxyphenyl] N-[(2R)-4-methylsulfanyl-1-[4-(4-nitrophenyl)piperazin-1-yl]-1-oxobutan-2-yl]carbamate 1308813-92-4 C37H40N4O11S 748.811 —— N-[8-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-6-methoxyphenazin-2-yl]acetamide 1445712-23-1 C28H23N3O6 497.507 —— N-[7-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-9-methoxyphenazin-2-yl]acetamide 1445712-14-0 C28H23N3O6 497.507 —— [4-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-2,6-dimethoxyphenyl] N-[(2S)-1-[4-(4-nitrophenyl)piperazin-1-yl]-1-oxo-3-phenylpropan-2-yl]carbamate 1308813-89-9 C41H40N4O11 764.789 —— [4-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-2,6-dimethoxyphenyl] N-[(2R)-1-[4-(4-nitrophenyl)piperazin-1-yl]-1-oxo-3-phenylpropan-2-yl]carbamate 1308813-90-2 C41H40N4O11 764.789 —— N-[8-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-6-methoxyphenazin-2-yl]-2-chloroacetamide 1445712-24-2 C28H22ClN3O6 531.952 —— N-[7-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-9-methoxyphenazin-2-yl]-2-chloroacetamide 1445712-15-1 C28H22ClN3O6 531.952 —— N-[8-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-6-methoxyphenazin-2-yl]propanamide 1445712-25-3 C29H25N3O6 511.534 —— N-[7-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-9-methoxyphenazin-2-yl]propanamide 1445712-16-2 C29H25N3O6 511.534 —— (5R,5aR,8aR)-5-(4-methoxy-8-nitrophenazin-2-yl)-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[5,6-f][1,3]benzodioxol-6-one 1445712-11-7 C26H19N3O7 485.453 —— (5R,5aR,8aR)-5-(4-methoxy-7-nitrophenazin-2-yl)-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[5,6-f][1,3]benzodioxol-6-one 1445712-10-6 C26H19N3O7 485.453 —— N-[8-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-6-methoxyphenazin-2-yl]heptanamide 1445712-27-5 C33H33N3O6 567.642 —— N-[7-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-9-methoxyphenazin-2-yl]heptanamide 1445712-17-3 C33H33N3O6 567.642 —— N-[8-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-6-methoxyphenazin-2-yl]-2-methylprop-2-enamide 1445712-26-4 C30H25N3O6 523.545 —— [(1S,12R,15R)-1-(3,4,5-trimethoxyphenyl)-5,7,14-trioxatetracyclo[10.2.1.02,10.04,8]pentadeca-2,4(8),9-trien-15-yl]methanol 321747-15-3 C22H24O7 400.428 —— N-[8-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-6-methoxyphenazin-2-yl]benzamide 1445712-28-6 C33H25N3O6 559.578 —— N-[7-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-9-methoxyphenazin-2-yl]benzamide 1445712-18-4 C33H25N3O6 559.578 —— N-[8-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-6-methoxyphenazin-2-yl]-4-methoxybenzamide 1445712-32-2 C34H27N3O7 589.604 —— N-[7-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-9-methoxyphenazin-2-yl]-4-methoxybenzamide 1445712-21-9 C34H27N3O7 589.604 —— N-[8-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-6-methoxyphenazin-2-yl]-3-methoxybenzamide 1445712-31-1 C34H27N3O7 589.604 —— N-[7-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-9-methoxyphenazin-2-yl]-3-methoxybenzamide 1445712-20-8 C34H27N3O7 589.604 —— N-[8-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-6-methoxyphenazin-2-yl]-3,4-dimethoxybenzamide 1445712-33-3 C35H29N3O8 619.631 —— N-[7-[(5R,5aR,8aR)-6-oxo-5a,8,8a,9-tetrahydro-5H-[2]benzofuro[6,5-f][1,3]benzodioxol-5-yl]-9-methoxyphenazin-2-yl]-3,4-dimethoxybenzamide 1445712-22-0 C35H29N3O8 619.631 —— 5-methoxypodophyllotoxin-4-O-β-D-glucoside 119188-52-2 C29H34O14 606.581 - 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
反应信息
-
作为反应物:描述:去氧鬼臼毒素 在 lead(IV) acetate 作用下, 以 溶剂黄146 为溶剂, 反应 3.0h, 以15 mg的产率得到6,7-demethylenedeoxypodophyllotoxin参考文献:名称:Isolation of 6,7-Demethylenedesoxypodophyllotoxin from Hernandia ovigera.摘要:从台湾采集的 Hernandia ovigera L.(Hernandiaceae)种子中分离出了 6,7-Demethylenedesoxypodophyllotoxin(1)以及几种已知的木脂素。这是首次在天然来源中发现 1 的实例。此外,还通过二维 H-C 相关光谱(COSY)和 H-C 长程 COSY 技术,确定了从该植物中分离出的几种豆荚毒素类似物的 13C 核磁共振信号的分配。DOI:10.1248/cpb.40.1318
-
作为产物:描述:Yatein; (-)-反式-3-(3,4-亚甲基二氧基苄基)-2-(3,4,5-三甲氧基苄基)丁内酯 在 ferrous(II) sulfate heptahydrate 、 ATGGGCAGCACCGCGCCGCTGCGTTTCCCGGTTATCGATTTGAGCATGAAGAACCTGAAACCTGGAACCACATCATGGAACAGCGTACGCACTCAGGTGCGTGAAGCTTTGGAAGAATATGGTTGCTTTGAAGCCGTTATTGATGCGGTTTCCCCAGAGTTGCAAAAAGCTGTCTGCAACAAGGGGCACGAACTGTTAAATTTACCGCTGGAGACCAAGATGCTTAATGGTAATAAGCCGGAGTACGATGGATTTACATCAATCCCGAACCTTAACGAAGGTATGGGTGTTGGCCGCATCACTGACTTAGAGAAGGTCGAACGTTTCACTAATCTGATGTGGCCTGAGGGGAACAAGGATTTTTGCGAAACAGTTTACTCCTATGGTAAGCGCATGGCAGAGGTTGACCATATTCTGAAGATGATGGTATTCGAATCTTTTGGTATGGAGAAACATTTTGACTCCTTCTGCGAAAGTACAAATTACTTGCTGCATTTCATGCGCTATCAACAACCCGGCAAAGACGGTCGCTCTCCCGCATTGAGTTTACACAAAGATAAATCTATCCTTACGATCGTCAACCAAAACGATGTAAAAGGACTGGAGTTCGAAACAAAGGATGGCGAATGGATTTTGCCAACAGCCGATAACCACATCGTATTACTTGGAGATTGCTTCATGGCTTGGAGTAACGGTCGCCTGCACTCTCCACTGCACCGTGTGACATTAGTGGCAAATCAGGCACGTTTGAGTACCTCCTCATTTAGCTTCCCAAAAGATATTATTGAGACACCGGCGGAATTGGTGGACGAGGAACATCCGCTTTTATTCAATCCCTTCGAGATCACCGAGCTTTTAGCCTACTGTTTTACAAAAGAAGGAGCCAAGGCGGTTTGCGATTTAAAGCAGTATAAAGCGTACACTGGAGCATGA 、 disodium α-ketoglutarate 、 维生素 C 作用下, 以 二甲基亚砜 为溶剂, 反应 20.0h, 以95%的产率得到去氧鬼臼毒素参考文献:名称:(-)-鬼臼毒素和相关芳基四氢木素木质素的不对称化学酶法合成。摘要:(-)-鬼臼毒素是最有效的微管解聚剂之一,在抗肿瘤药物的发现中起着重要的先导化合物的作用。这里报道的是(-)-鬼臼毒素和相关芳基四氢木脂素的短促化学酶法全合成。这种方法的关键是使用酶促氧化性C-C偶联反应以非对映选择性的方式构建天然产物的四环核。该策略允许以克级获得(-)-脱氧鬼臼毒素,并且很容易适应相关芳基四氢木脂素的制备。DOI:10.1002/anie.201904102
文献信息
-
[EN] SUBSTITUTED BENZYLAMINE COMPOUNDS, THEIR USE IN MEDICINE, AND IN PARTICULAR THE TREATMENT OF HEPATITIS C VIRUS (HCV) INFECTION<br/>[FR] COMPOSÉS DE BENZYLAMINE SUBSTITUÉS, LEUR UTILISATION EN MÉDECINE, EN PARTICULIER DANS LE TRAITEMENT D'UNE INFECTION PAR LE VIRUS DE L'HÉPATITE C (VHC)申请人:ASTEX THERAPEUTICS LTD公开号:WO2013064538A1公开(公告)日:2013-05-10The invention provides compounds of the formula (I): or a salt, N-oxide or tautomer thereof, wherein A is CH, CF or nitrogen; E is CH, CF or nitrogen; and R0 is hydrogen or C1-2 alkyl; R1a is selected from CONH2; CO2H; an optionally substituted acyclic C1-8 hydrocarbon group; and an optionally substituted monocyclic carbocyclic or heterocyclic group of 3 to 7 ring members, of which 0, 1, 2, 3 or 4 are heteroatom ring members selected from O, N and S; R2 is selected from hydrogen and a group R2a; R2a is selected from an optionally substituted acyclic d-8 hydrocarbon group; an optionally substituted monocyclic carbocyclic or heterocyclic group of 3 to 7 ring members, of which 0, 1 or 2 ring members are heteroatom ring members selected from O, N and S; and an optionally substituted bicyclic heterocyclic group of 9 or 10 ring members, of which 1 or 2 ring members are nitrogen atoms; wherein at least one of R1 and R2 is other than hydrogen; R3 is an optionally substituted 3- to 10-membered monocyclic or bicyclic carbocyclic or heterocyclic ring containing 0, 1, 2 or 3 heteroatom ring members selected from N, O and S; R4a is selected from halogen; cyano; C1-4 alkyl optionally substituted with one or more fluorine atoms; C1-4 alkoxy optionally substituted with one or more fluorine atoms; hydroxy-C1-4 alkyl; and C1-2 alkoxy-C1-4 alkyl; R5 is selected from hydrogen and a substituent R5a; and R5a is selected from C1-2 alkyl optionally substituted with one or more fluorine atoms; C1-3 alkoxy optionally substituted with one or more fluorine atoms; halogen; cyclopropyl; cyano; and amino, The compounds have activity against hepatitis C virus and can be used in the prevention or treatment of hepatitis C viral infections.该发明提供了以下式(I)的化合物,或其盐、N-氧化物或互变异构体,其中A为CH、CF或氮;E为CH、CF或氮;R0为氢或C1-2烷基;R1a选自CONH2;CO2H;一个可选择取代的非环状C1-8碳氢化合物基团;以及一个可选择取代的含有3至7个环成员的单环碳环或杂环基团,其中0、1、2、3或4个是从O、N和S中选择的杂原子环成员;R2选自氢和一个基团R2a;R2a选自一个可选择取代的非环状d-8碳氢化合物基团;一个可选择取代的含有3至7个环成员的单环碳环或杂环基团,其中0、1或2个环成员是从O、N和S中选择的杂原子环成员;以及一个可选择取代的含有9或10个环成员的双环杂环基团,其中1或2个环成员是氮原子;其中R1和R2中至少一个不是氢;R3选自一个可选择取代的含有0、1、2或3个从N、O和S中选择的杂原子环成员的3至10个成员的单环或双环碳环或杂环环;R4a选自卤素;氰基;C1-4烷基,可选择取代一个或多个氟原子;C1-4烷氧基,可选择取代一个或多个氟原子;羟基-C1-4烷基;和C1-2烷氧基-C1-4烷基;R5选自氢和一个取代基R5a;R5a选自C1-2烷基,可选择取代一个或多个氟原子;C1-3烷氧基,可选择取代一个或多个氟原子;卤素;环丙基;氰基;和氨基。这些化合物对丙型肝炎病毒具有活性,并可用于预防或治疗丙型肝炎病毒感染。
-
Efficient asymmetric syntheses of naturally occurring lignan lactones using catalytic asymmetric hydrogenation as a key reaction作者:Toshiaki Morimoto、Mitsuo Chiba、Kazuo AchiwaDOI:10.1016/s0040-4020(01)80536-6日期:1993.2using the catalytic asymmetric hydrogenation of arylidenesuccinic acid monoesters with a rhodium(I) complex of a chiral bisphosphine, (4S,5S)-MOD-DIOP. Asymmetric total syntheses of some naturally occurring lignans, (+)-collinusin, (−)-deoxypodophyllotoxin, and (+)-neoisostegane, were achieved via several steps from (R)-γ-butyrolactones as key intermediates obtained by the reduction of (R)-arylmethylsuccinic
-
Interleukin-2:remodeling and glycoconjugation of interleukin-2申请人:DeFrees Shawn公开号:US20050031584A1公开(公告)日:2005-02-10The invention includes methods and compositions for remodeling a peptide molecule, including the addition or deletion of one or more glycosyl groups to a peptide, and/or the addition of a modifying group to a peptide.该发明包括重塑肽分子的方法和组合物,包括向肽分子中添加或删除一个或多个糖基团,和/或向肽分子中添加修饰基团。
-
[EN] PHARMACEUTICAL COMPOUNDS<br/>[FR] COMPOSÉS PHARMACEUTIQUES申请人:ASTEX THERAPEUTICS LTD公开号:WO2013064543A1公开(公告)日:2013-05-10The invention provides compounds that are useful in the treatment of hepatitis C virus (HCV) infections. The compounds have the formula (1): or a salt, N-oxide, tautomer or stereoisomer thereof, wherein A is CH or N; E is CH or N; R1 is selected from: an optionally substituted acyclic C1-8 hydrocarbon group wherein one carbon atom of the acyclic C1-8 hydrocarbon group may optionally be replaced by O, S, NRC, S(O) or SO2, or two adjacent carbon atoms of the acyclic d-β hydrocarbon group may optionally be replaced by CONRc, NRcCO, NRcSO2 or SO2NRc provided that in each case at least one carbon atom of the acyclic C1-8 hydrocarbon group remains; and an optionally substituted monocyclic carbocyclic or heterocyclic group of 3 to 7 ring members, of which 0, 1, 2, 3 or 4 are heteroatom ring members selected from O, N and S; R2 is hydrogen or X-R8; X is a C1-8 alkanediyl group wherein one carbon atom of the C1-8 alkanediyl group may optionally be bonded to a -CH2-CH2- moiety to form a cyclopropane-1,1-diyl group or two adjacent carbon atoms of the C1-8 alkanediyl group may optionally be bonded to a -(CH2)n moiety, where n is 1 to 5, to form a C3-7-cycloalkane-1,2-diyl group; R3 is an optionally substituted 3- to 10-membered monocyclic or bicyclic carbocyclic or heterocyclic ring containing 0-3 heteroatom ring members selected from N, O and S; R4 is hydrogen or R43 wherein R43 is halogen; cyano; C1-4 alkyl; fluoro-1.4 alkyl; C1-4 alkoxy; fluoro-C1-4 alkoxy; hydroxy-C1-4 alkyl; or C1-2 alkoxy-C1-4 alkyl; R5 is hydrogen or R53 wherein R53 is selected from C1-2 alkyl optionally substituted with fluorine; C1-3 alkoxy optionally substituted with fluorine; halogen; cyclopropyl; and cyano; R8 is hydroxy or C(=O)NR10R11; provided that when R8 is hydroxy, there are at least two carbon atoms in line between the hydroxy group and the nitrogen atom to which X is attached; R10 is hydrogen or C1-4 alkyl; and R11 is hydrogen; amino-C2-4 alkyl or hydroxy-C2-4 alkyl; but excluding the compounds 1-(3-benzoylphenyl)-ethylamine and 1-(3-furan-2-oylcarbonylphenyl)-ethylamine.该发明提供了在治疗丙型肝炎病毒(HCV)感染中有用的化合物。这些化合物的化学式为(1):或其盐、N-氧化物、互变异构体或立体异构体,其中A为CH或N;E为CH或N;R1从以下选取:一个可选择取代的非环C1-8碳氢化合物基团,其中非环C1-8碳氢化合物基团的一个碳原子可选择被O、S、NRC、S(O)或SO2取代,或者非环d-β碳氢化合物基团的两个相邻碳原子可选择被CONRc、NRcCO、NRcSO2或SO2NRc取代,但在每种情况下非环C1-8碳氢化合物基团至少保留一个碳原子;和一个可选择取代的含3至7个环成员的单环碳环或杂环基团,其中0、1、2、3或4个是O、N和S的杂原子环成员;R2为氢或X-R8;X为一个C1-8烷二基基团,其中C1-8烷二基基团的一个碳原子可选择与一个-CH2- -基团结合形成环丙烷-1,1-二基基团,或者C1-8烷二基基团的两个相邻碳原子可选择与一个-( )n基团结合,其中n为1至5,形成一个C3-7环烷-1,2-二基基团;R3为一个可选择取代的含0-3个N、O和S杂原子环成员的3至10个成员的单环或双环碳环或杂环环;R4为氢或R43,其中R43为卤素;氰基;C1-4烷基;氟代-1,4烷基;C1-4烷氧基;氟代-C1-4烷氧基;羟基-C1-4烷基;或C1-2烷氧基-C1-4烷基;R5为氢或R53,其中R53选自可选择用氟取代的C1-2烷基;可选择用氟取代的C1-3烷氧基;卤素;环丙基;和氰基;R8为羟基或C(=O)NR10R11;但当R8为羟基时,羟基与X连接的氮原子之间至少有两个碳原子;R10为氢或C1-4烷基;R11为氢;氨基-C2-4烷基或羟基-C2-4烷基;但不包括化合物1-(3-苯甲酰基苯基)-乙胺和1-(3-呋喃-2-酰基苯基)-乙胺。
-
Aryltetralin lignans from Podophyllum hexandrum and Podophyllum peltatum作者:David E. Jackson、Paul M. DewickDOI:10.1016/s0031-9422(00)82628-x日期:1984.1Abstract Roots of Podophyllum hexandrum and P. peltatum contain the same range of ten aryltetralin lignans: podophyllotoxin, 4′-demethylpodophyllotoxin, α-peltatin, β-peltatin, desoxypodophyllotoxin, podophyllotoxone, isopicropodophyllone, 4′-demethyldesoxypodophyllotoxin, 4′-demethylpodophyllotoxone and 4′-demethylisopicropodophyllone, although the relative proportions are markedly different. The latter two
表征谱图
-
氢谱1HNMR
-
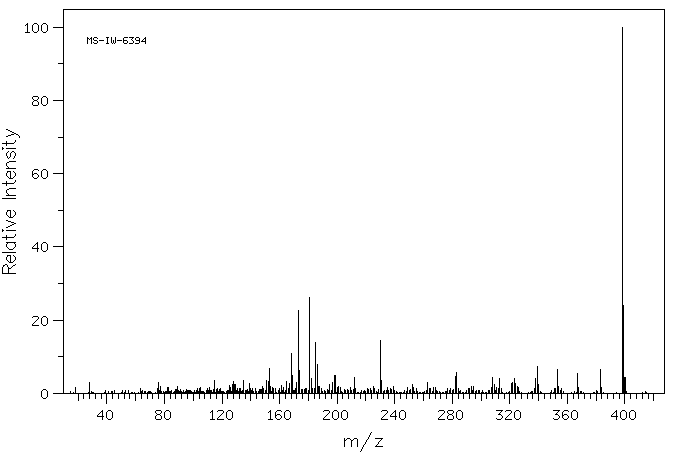
质谱MS
-
碳谱13CNMR
-
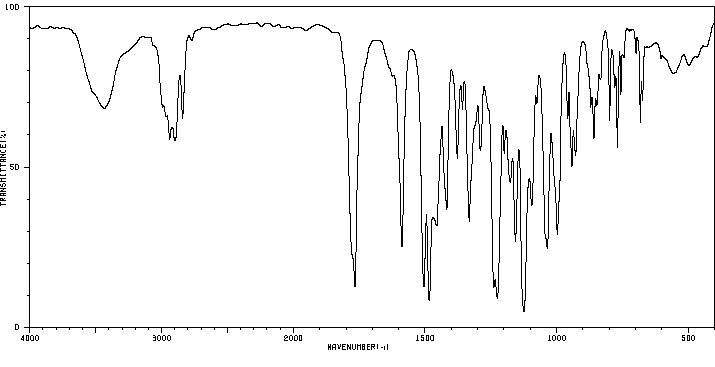
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息
同类化合物
鬼臼脂毒酮
鬼臼毒素-4-O-葡萄糖苷
鬼臼毒素
鬼臼毒素
表鬼臼毒素乙醚
苦鬼臼毒素
脱氧鬼臼毒素
磷酸依托泊甙
盾叶鬼臼素
澳白木脂素2
澳白木脂素1
替尼泊苷
托尼依托泊苷
异苦鬼臼毒素
去氧鬼臼毒素
克立米星C
依托泊苷杂质B
依托泊苷
他氟泊苷
丙氨酸,N-(羧基甲基)-(9CI)
alpha-盾叶鬼臼素
alpha-依托泊苷
alpha-依托泊苷
[(5R,5aR,8aR,9R)-9-(4-羟基-3,5-二甲氧基-苯基)-8-氧代-5a,6,8a,9-四氢-5H-异苯并呋喃并[5,6-f][1,3]苯并二氧戊环-5-基]丁酸酯
TOP-53二盐酸盐
NK-611盐酸盐
5,8,8a,9-四氢-9-羟基-5-(3,4,5-三甲氧基苯基)-(5R,5aR,8aR,9S)-呋喃并[3',4':6,7]萘并[2,3-d]-1,3-二氧杂环戊烯-6(5aH)-酮
4’-去甲鬼臼毒素
4’-去甲基表鬼臼毒素-Β-D-葡萄糖甙
4-{[(5S,5aS,8aR,9R)-9-(4-羟基-3,5-二甲氧苯基)-8-羰基-5,5a,6,8,8a,9-六氢呋喃并[3',4':6,7]萘并[2,3-d][1,3]二噁唑-5-基]氨基甲酰}苯基乙酸酯
4,6-O-苄叉-Β-D-葡萄糖甙鬼臼毒素
4'-去甲基表鬼臼毒素
4'-O-脱甲基-4-((4'-(1'-苯甲基哌啶基))氨基)-4-脱氧鬼臼毒
4 ’-去甲去氧鬼臼毒素
3-羟基-4H-吡喃-4-酮
3-氨基-N-[(5S,5aS,8aR,9R)-9-(4-羟基-3,5-二甲氧苯基)-8-羰基-5,5a,6,8,8a,9-六氢呋喃并[3',4':6,7]萘并[2,3-d][1,3]二噁唑-5-基]苯酰胺
2’-O-没食子酰基金丝桃甙
2(3H)-硫代酰苯,3-乙基二氢-3-(1-甲基乙基)-(9CI)
2'-氯依托泊苷
1-羟基-17-氧杂五环[6.6.5.0~2,7~.0~9,14~.0~15,19~]十九碳-2,4,6,9,11,13-六烯-16,18-二酮(non-preferredname)
(8aR,9S)-9-[[(2R)-7,8-二羟基-2-(2-噻吩基)-4,4a,6,7,8,8a-六氢吡喃并[5,6-d][1,3]二恶英-6-基]氧基]-5-(3,4,5-三甲氧基苯基)-5a,8,8a,9-四氢-5H-异苯并呋喃并[6,5-f][1,3]苯并二氧戊环-6-酮
(5S,5aS,8aR,9R)-5-[(4-氟苯基)氨基]-9-(4-羟基-3,5-二甲氧基-苯基)-5a,6,8a,9-四氢-5H-异苯并呋喃并[5,6-f][1,3]苯并二氧戊环-8-酮
(5S,5aR,8aR,9R)-9-(4-羟基-3,5-二甲氧基-苯基)-5-(4-羟基苯基)硫烷基-5a,6,8a,9-四氢-5H-异苯并呋喃并[5,6-f][1,3]苯并二噁唑-8-酮
(5R,5aR,8aS,9S)-9-[(4-氨基苯基)氨基]-5-(4-羟基-3,5-二甲氧苯基)-5,8,8a,9-四氢呋喃并[3',4':6,7]萘并[2,3-d][1,3]二噁唑-6(5aH)-酮盐酸(1:1)
(5R,5aR,8aR,9R)-9-羟基-10-甲氧基-5-(3,4,5-三甲氧基苯基)-5a,8,8a,9-四氢-5H-异苯并呋喃并[6,5-f][1,3]苯并二氧戊环-6-酮
(5R,5aR,8aR,9R)-9-[[(6R,7R,8R)-7,8-二羟基-2-(4-甲氧基苯基)-4,4a,6,7,8,8a-六氢吡喃并[5,6-d][1,3]二恶英-6-基]氧基]-5-(3,4,5-三甲氧基苯基)-5a,8,8a,9-四氢-5H-异苯并呋喃并[6,5-F][1,3]苯并二氧戊环-6-酮
(5R,5aR,8aR,9R)-9-[[(6R,7R,8R)-7,8-二羟基-2-(2-羟基苯基)-4,4a,6,7,8,8a-六氢吡喃并[5,6-d][1,3]二恶英-6-基]氧基]-5-(3,4,5-三甲氧基苯基)-5a,8,8a,9-四氢-5H-异苯并呋喃并[6,5-F][1,3]苯并二氧戊环-6-酮
(5R,5aR,8aR,9R)-8-羰基-9-(3,4,5-三甲氧苯基)-5,5a,6,8,8a,9-六氢呋喃并[3',4':6,7]萘并[2,3-d][1,3]二噁唑-5-基乙酸酯
(5R,5aR,8aR,9R)-5-(4-乙氧基-3,5-二甲氧基-苯基)-9-[(2R,3R,4S,5S,6R)-3,4,5-三羟基-6-(羟基甲基)四氢吡喃-2-基]氧基-5a,8,8a,9-四氢-5H-异苯并呋喃并[6,5-f][1,3]苯并二氧戊环-6-酮
(5R,5aR,8aR,9R)-5-(3,5-二甲氧基-4-丙氧基-苯基)-9-[(2R,3R,4S,5S,6R)-3,4,5-三羟基-6-(羟基甲基)四氢吡喃-2-基]氧基-5a,8,8a,9-四氢-5H-异苯并呋喃并[6,5-f][1,3]苯并二氧戊环-6-酮