盐酸胺碘酮 | 19774-82-4
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
物化性质
-
熔点:154-158°C
-
闪点:9℃
-
溶解度:易溶于可溶于氯仿、甲醇。
-
最大波长(λmax):242nm(MeOH)(lit.)
-
颜色/状态:Crystalline powder; crystals from acetone
-
稳定性/保质期:
Amiodarone Hydrochloride 0.6 mg/ml in dextrose 5% in water is stable for five days at room temperature. Solutions containing less than 0.6 mg/ml of amiodarone hydrochloride in dextrose 5% in water are unstable and should not be used.
-
解离常数:pKa = 6.56
-
碰撞截面:226.3 Ų [M+H]+ [CCS Type: TW, Method: calibrated with polyalanine and drug standards]
计算性质
-
辛醇/水分配系数(LogP):2.52
-
重原子数:32
-
可旋转键数:11
-
环数:3.0
-
sp3杂化的碳原子比例:0.4
-
拓扑面积:43.9
-
氢给体数:1
-
氢受体数:4
ADMET
安全信息
-
危险品标志:Xn
-
安全说明:S36
-
危险类别码:R20/21/22
-
WGK Germany:3
-
海关编码:2932999099
-
危险品运输编号:UN1230 - class 3 - PG 2 - Methanol, solution
-
RTECS号:OB1361000
-
危险标志:GHS07
-
危险性描述:H312,H332
-
危险性防范说明:P280
-
储存条件:2-8℃
SDS
模块 1. 化学品
1.1 产品标识符
: Amiodarone hydrochloride
产品名称
1.2 鉴别的其他方法
2-Butyl-3-benzofuranyl-4-[2-(diethylamino)ethoxy]-3,5-diiodophenyl ketonehydrochloride
1.3 有关的确定了的物质或混合物的用途和建议不适合的用途
仅用于研发。不作为药品、家庭或其它用途。
模块 2. 危险性概述
2.1 GHS-分类
急性毒性, 经口 (类别 5)
急性毒性, 吸入 (类别 4)
急性毒性, 经皮 (类别 4)
2.2 GHS 标记要素,包括预防性的陈述
象形图
警示词 警告
危险申明
H303 吞咽可能有害。
H312 皮肤接触有害。
H332 吸入有害。
警告申明
预防措施
P261 避免吸入粉尘/烟/气体/烟雾/蒸气/喷雾.
P271 只能在室外或通风良好之处使用。
P280 穿戴防护手套/ 防护服。
事故响应
P302 + P352 如果皮肤接触:用大量肥皂和水清洗。
P304 + P340 如吸入: 将患者移到新鲜空气处休息,并保持呼吸舒畅的姿势。
P312 如感觉不适,呼救中毒控制中心或医生.
P322 具体处置(见本标签上提供的急救指导)。
P363 沾污的衣服清洗后方可再用。
废弃处置
P501 将内容物/ 容器处理到得到批准的废物处理厂。
2.3 其它危害物
光敏剂
模块 3. 成分/组成信息
3.1 物 质
: 2-Butyl-3-benzofuranyl-4-[2-(diethylamino)ethoxy]-3,5-diiodophenyl
别名
ketonehydrochloride
: C25H29I2NO3 · HCl
分子式
: 681.77 g/mol
分子量
组分 浓度或浓度范围
Amiodarone hydrochloride
<=100%
化学文摘登记号(CAS 19774-82-4
No.) 243-293-2
EC-编号
模块 4. 急救措施
4.1 必要的急救措施描述
一般的建议
请教医生。 向到现场的医生出示此安全技术说明书。
吸入
如果吸入,请将患者移到新鲜空气处。 如呼吸停止,进行人工呼吸。 请教医生。
皮肤接触
用肥皂和大量的水冲洗。 请教医生。
眼睛接触
用水冲洗眼睛作为预防措施。
食入
切勿给失去知觉者通过口喂任何东西。 用水漱口。 请教医生。
4.2 主要症状和影响,急性和迟发效应
长期或频繁接触会导致:, 损伤肺, 可能发生对肝的伤害。, 对心脏有害
4.3 及时的医疗处理和所需的特殊处理的说明和指示
无数据资料
模块 5. 消防措施
5.1 灭火介质
灭火方法及灭火剂
用水雾,抗乙醇泡沫,干粉或二氧化碳灭火。
5.2 源于此物质或混合物的特别的危害
碳氧化物, 氮氧化物, 氯化氢气体, 碘化氢
5.3 给消防员的建议
如必要的话,戴自给式呼吸器去救火。
5.4 进一步信息
无数据资料
模块 6. 泄露应急处理
6.1 作业人员防护措施、防护装备和应急处置程序
使用个人防护用品。 避免粉尘生成。 避免吸入蒸气、烟雾或气体。 保证充分的通风。 避免吸入粉尘。
6.2 环境保护措施
不要让产品进入下水道。
6.3 泄漏化学品的收容、清除方法及所使用的处置材料
收集和处置时不要产生粉尘。 扫掉和铲掉。 放入合适的封闭的容器中待处理。
6.4 参考其他部分
丢弃处理请参阅第13节。
模块 7. 操作处置与储存
7.1 安全操作的注意事项
避免接触皮肤和眼睛。 避免形成粉尘和气溶胶。
在有粉尘生成的地方,提供合适的排风设备。一般性的防火保护措施。
7.2 安全储存的条件,包括任何不兼容性
贮存在阴凉处。 使容器保持密闭,储存在干燥通风处。
建议的贮存温度: 2 - 8 °C
7.3 特定用途
无数据资料
模块 8. 接触控制和个体防护
8.1 容许浓度
最高容许浓度
没有已知的国家规定的暴露极限。
8.2 暴露控制
适当的技术控制
根据良好的工业卫生和安全规范进行操作。 休息前和工作结束时洗手。
个体防护设备
眼/面保护
带有防护边罩的安全眼镜符合 EN166要求请使用经官方标准如NIOSH (美国) 或 EN 166(欧盟)
检测与批准的设备防护眼部。
皮肤保护
戴手套取 手套在使用前必须受检查。
请使用合适的方法脱除手套(不要接触手套外部表面),避免任何皮肤部位接触此产品.
使用后请将被污染过的手套根据相关法律法规和有效的实验室规章程序谨慎处理. 请清洗并吹干双手
所选择的保护手套必须符合EU的89/686/EEC规定和从它衍生出来的EN 376标准。
身体保护
全套防化学试剂工作服, 防护设备的类型必须根据特定工作场所中的危险物的浓度和数量来选择。
呼吸系统防护
如须暴露于有害环境中,请使用P95型(美国)或P1型(欧盟 英国
143)防微粒呼吸器。如需更高级别防护,请使用OV/AG/P99型(美国)或ABEK-P2型 (欧盟 英国 143)
防毒罐。
呼吸器使用经过测试并通过政府标准如NIOSH(US)或CEN(EU)的呼吸器和零件。
模块 9. 理化特性
9.1 基本的理化特性的信息
a) 外观与性状
形状: 固体
b) 气味
无数据资料
c) 气味阈值
无数据资料
d) pH值
无数据资料
e) 熔点/凝固点
无数据资料
f) 沸点、初沸点和沸程
无数据资料
g) 闪点
无数据资料
h) 蒸发速率
无数据资料
i) 易燃性(固体,气体)
无数据资料
j) 高的/低的燃烧性或爆炸性限度 无数据资料
k) 蒸气压
无数据资料
l) 蒸汽密度
无数据资料
m) 密度/相对密度
无数据资料
n) 水溶性
无数据资料
o) n-辛醇/水分配系数
无数据资料
p) 自燃温度
无数据资料
q) 分解温度
无数据资料
r) 粘度
无数据资料
模块 10. 稳定性和反应活性
10.1 反应性
无数据资料
10.2 稳定性
无数据资料
10.3 危险反应
无数据资料
10.4 应避免的条件
无数据资料
10.5 不相容的物质
强氧化剂
10.6 危险的分解产物
其它分解产物 - 无数据资料
模块 11. 毒理学资料
11.1 毒理学影响的信息
急性毒性
半数致死剂量 (LD50) 经口 - 大鼠 - > 3,000 mg/kg
皮肤刺激或腐蚀
无数据资料
眼睛刺激或腐蚀
无数据资料
呼吸道或皮肤过敏
无数据资料
生殖细胞致突变性
无数据资料
致癌性
IARC:
此产品中没有大于或等于 0。1%含量的组分被 IARC鉴别为可能的或肯定的人类致癌物。
生殖毒性
生殖毒性 - 大鼠 - 经口
对生殖的影响:胚胎植入前死亡率(例如每个雌性的植入胚胎数减少;每个黄体的植入总数。
对生殖的影响:其他生殖力相关检测。 对新生儿的影响:生长统计数据(例如体重增长的减少)。
生殖毒性 - 大鼠 - 经口
对生殖的影响:数量少(例如#每胎产仔;出生前测定)。
生殖毒性 - 大鼠 - 经口
对新生儿的影响:身体的。
特异性靶器官系统毒性(一次接触)
无数据资料
特异性靶器官系统毒性(反复接触)
无数据资料
吸入危险
无数据资料
潜在的健康影响
吸入 吸入有害。 可能引起呼吸道刺激。
摄入 如服入是有害的。
皮肤 通过皮肤吸收有害。 可能引起皮肤刺激。
眼睛 可能引起眼睛刺激。
接触后的征兆和症状
长期或频繁接触会导致:, 损伤肺, 可能发生对肝的伤害。, 对心脏有害
附加说明
化学物质毒性作用登记: OB1361000
模块 12. 生态学资料
12.1 生态毒性
无数据资料
12.2 持久性和降解性
无数据资料
12.3 潜在的生物累积性
无数据资料
12.4 土壤中的迁移性
无数据资料
12.5 PBT 和 vPvB的结果评价
无数据资料
12.6 其它不良影响
无数据资料
模块 13. 废弃处置
13.1 废物处理方法
产品
将剩余的和不可回收的溶液交给有许可证的公司处理。
联系专业的拥有废弃物处理执照的机构来处理此物质。
与易燃溶剂相溶或者相混合,在备有燃烧后处理和洗刷作用的化学焚化炉中燃烧
受污染的容器和包装
按未用产品处置。
模块 14. 运输信息
14.1 联合国危险货物编号
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.2 联合国运输名称
欧洲陆运危规: 非危险货物
国际海运危规: 非危险货物
国际空运危规: 非危险货物
14.3 运输危险类别
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.4 包裹组
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.5 环境危险
欧洲陆运危规: 否 国际海运危规 国际空运危规: 否
海洋污染物(是/否): 否
14.6 对使用者的特别提醒
无数据资料
上述信息视为正确,但不包含所有的信息,仅作为指引使用。本文件中的信息是基于我们目前所知,就正
确的安全提示来说适用于本品。该信息不代表对此产品性质的保证。
参见发票或包装条的反面。
模块 15 - 法规信息
N/A
模块16 - 其他信息
N/A
制备方法与用途
盐酸胺碘酮属于III类抗心律失常药物,能够延长心房和心室肌纤维的动作电位时程(APD),这种效果是由阻滞延迟性整流外向钾流(Ik)引起的。其中,Ik可以表现为快延迟整流(Ikr)和慢延迟整流(Iks)。胺碘酮对Ikr和Iks均有抑制作用。正常心肌细胞的3相复极电流主要由Ik和Iks混合组成,但在心动过缓时,Ikr成分增加;在心动过速时,Iks成分增加。因此,胺碘酮比纯III类药物(选择性Ikr阻断剂)更为优越,因为它具有使用依赖特性:心率加快时其抗心律失常作用增强,而心率减慢时对QT间期的影响减少。这使得它在治疗尖端扭转性室速方面表现出色。
应用盐酸胺碘酮是胺碘酮的盐酸盐形式,广泛应用于治疗和预防室性和房性心律失常。该药物具有直接扩张冠状动脉及周围血管的作用,并可影响甲状腺素代谢。
生物活性盐酸胺碘酮(AMiodarone HCl)是一种钠/钾-ATP酶抑制剂,同时也是自噬的激活剂,用于治疗各种类型的心律失常。
靶点| Target | Value |
|---|---|
| Potassium channel |
盐酸胺碘酮具有对快速钠通道和慢钙通道的抑制作用。它还表现出非竞争性抗交感神经效应,并调节甲状腺功能和磷脂代谢。该药物能够深深渗透到膜的脂质基质中,并从心脏组织非常缓慢地释放。在豚鼠乳头肌的研究中,盐酸胺碘酮(44-88 μM)抑制了Vmax而不影响静息膜电位,这种抑制作用在频率或使用依赖性方面类似于I类抗心律失常药物。在心室肌和Purkinje纤维中,该药物也在50-88 μM的浓度下抑制了去极化诱导自发动作电位(自律性异常)。
体内研究在房室结和麻醉犬中,盐酸胺碘酮(1.25-25 毫克/公斤)导致窦率下降、房室结的有效不应期延长以及频率依赖的传导延迟。在兔的心室肌细胞中,连续3-4周每天给予50毫克/公斤的药物剂量后,观察到Ikr和ito的电流密度显著下降,但ICA和IK1的密度没有受到影响。盐酸胺碘酮(AM)通过5'-脱碘(5'DI)抑制甲状腺素(T4)转化为碘甲状腺原氨酸(T3),而不影响细胞内的转换。
用途用于抗心律失常、治疗心绞痛
反应信息
-
作为反应物:描述:盐酸胺碘酮 在 mixture of recombinant P450 isoforms 、 还原型辅酶II(NADPH)四钠盐 、 magnesium chloride 作用下, 反应 0.75h, 生成 4-Hydroxyamiodarone参考文献:名称:Identifying a Selective Substrate and Inhibitor Pair for the Evaluation of CYP2J2 Activity摘要:CYP2J2 是一种花生四烯酸环氧化酶,它在阿司咪唑和依巴斯汀的首过代谢中的作用已得到公认。要全面评估 CYP2J2 在药物代谢中的作用,必须有选择性底物和强效特异性化学抑制剂。在这项研究中,我们报告了胺碘酮 4-羟基化反应,这是一种由 CYP2J2 催化的特异性反应,没有 CYP3A4 或其他药物代谢酶的参与。通过胺碘酮 4-羟化反应,可以确定 CYP2J2 的肝脏相对活性因子和系统间外推因子。胺碘酮 4-羟基化与阿司咪唑 O-脱甲基化相关,但与人体肝脏微粒体样本中 CYP2J2 蛋白含量无关。为了确定特异性 CYP2J2 抑制剂,研究人员使用特非那定和阿司咪唑作为重组 CYP2J2 的探针底物,对 138 种药物进行了筛选。42 种药物在 30 μM 的浓度下对 CYP2J2 活性的抑制率≥50%,但抑制作用依赖于底物。其中,达那唑是特非那定羟基化(IC50 = 77 nM)和阿司咪唑 O-去甲基化(K i = 20 nM)的强效抑制剂,抑制作用主要是竞争性的。达那唑抑制 CYP2C9、CYP2C8 和 CYP2D6 的 IC50 值分别为 1.44、1.95 和 2.74 μM。胺碘酮或阿司咪唑被纳入七种探针鸡尾酒中进行细胞色素 P450(P450)药物相互作用潜力筛选,阿司咪唑显示出更好的特征,因为它与其他 P450 探针没有明显的相互作用。因此,达那唑、胺碘酮和阿司咪唑将有助于确定 CYP2J2 在肝脏和肝外组织中的代谢作用。DOI:10.1124/dmd.111.043505
-
作为产物:参考文献:名称:一种制备盐酸胺碘酮的方法摘要:本发明公开一种制备盐酸胺碘酮的方法,包括:以2‑丁基苯并呋喃和对乙酰氧基苯甲醛为原料,在Lewis酸催化以及加热条件下发生aldol反应,产物在碘和碱存在的条件下同时发生羟基氧化、脱乙酰基以及碘代反应,之后产物和N,N‑二乙基氯乙胺反应、成盐,得到盐酸胺碘酮。该方法只需要催化量Lewis酸的使用,不需要强酸性氯化铝的参与,反应条件更加温和,副产物少,易于后处理,三废大大减少;整个路线的操作简单,所用试剂都便宜易得、无毒害,非常适用于工业化生产。公开号:CN113527236B
文献信息
-
[EN] REAGENTS AND PROCESS FOR DIRECT C-H FUNCTIONALIZATION<br/>[FR] RÉACTIFS ET PROCÉDÉ POUR LA FONCTIONNALISATION DIRECTE DE LA LIAISON C-H申请人:STUDIENGESELLSCHAFT KOHLE MBH公开号:WO2020094673A1公开(公告)日:2020-05-14Thianthrene derivative of the Formula (I): wherein R1 to R8 may be the same or different and are selected from hydrogen, Cl, F, a partially or fully fluorinated C1 to C6 alkyl group, and wherein n is 0 or 1, with the proviso that at least one of R1 to R8 is not hydrogen and process for C-H functionalization of aromatic compounds using this compound.
-
[EN] CHEMOKING RECEPTOR ANTAGONISTS<br/>[FR] ANTAGONISTES DES RÉCEPTEURS DE CHIMIOKINES申请人:ABBOTT LAB公开号:WO2013010453A1公开(公告)日:2013-01-24Disclosed herein are chemokine receptor antagonists of formula (I) wherein G1, X1, X2, and X3 are as defined in the specification. Compositions comprising such compounds; and methods for treating conditions and disorders using such compounds and compositions are also described.
-
Novel Tricyclic Compounds申请人:Wishart Neil公开号:US20090312338A1公开(公告)日:2009-12-17The invention provides a compound of Formula (I) pharmaceutically acceptable salts, pro-drugs, biologically active metabolites, stereoisomers and isomers thereof wherein the variable are defined herein. The compounds of the invention are useful for treating immunological and oncological conditions.这项发明提供了一个符合Formula (I)的化合物,其中包括药用盐、前药、生物活性代谢物、立体异构体和同分异构体,其中变量在此处定义。该发明的化合物对治疗免疫和肿瘤疾病有用。
-
BENZAZEPINE DERIVATIVE, PROCESS FOR PRODUCING THE SAME, AND USE申请人:Takeda Chemical Industries, Ltd.公开号:EP1422228A1公开(公告)日:2004-05-26The present invention provides a novel benzazepine derivative represented by formula : wherein, R1 is a 5- or 6-membered aromatic ring, R2 is lower alkyl group, etc., Y is an optionally substituted imino group, ring A and ring B are independently an optionally substituted aromatic ring, W is formula -W1-X2-W2- (W1 and W2 are independently S(O)m1 (m1 is 0, 1 or 2), etc., and X2 is an optionally substituted alkylene groupetc. ), a preparation method and use thereof.
-
[EN] FURO[3,2-d]PYRIMIDINE COMPOUNDS<br/>[FR] COMPOSÉS DE FURO[3,2-D]PYRIMIDINE申请人:ABBOTT LAB公开号:WO2012048222A1公开(公告)日:2012-04-12The present invention is directed to novel compounds of Formula (I), pharmaceutically acceptable salts, biologically active metabolites, pro-drugs, racemates, enantiomers, diastereomers, solvates and hydrates thereof wherein the variables are defined as herein. The compounds of Formula (I) are useful as kinase inhibitors and as such would be useful in treating certain conditions and diseases, especially inflammatory conditions and diseases and proliferative disorders and conditions, for example, cancers.
表征谱图
-
氢谱1HNMR
-
质谱MS
-
碳谱13CNMR
-
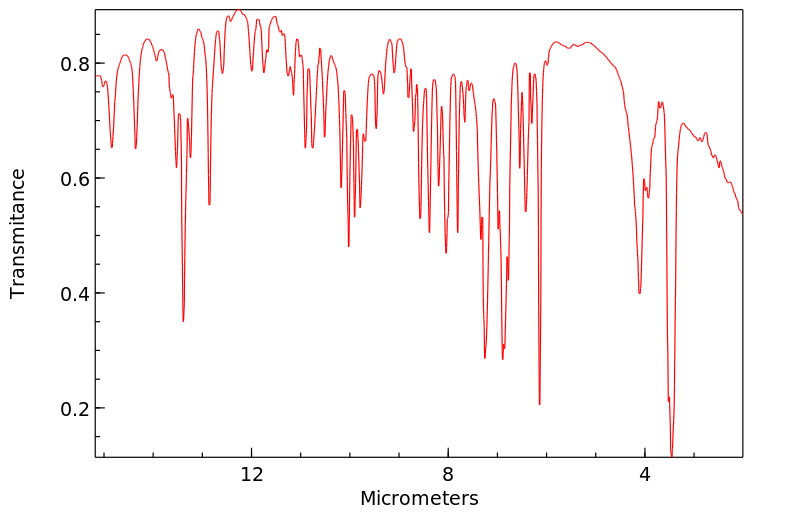
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息