次黄嘌呤 | 68-94-0
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
物化性质
-
熔点:>300 °C (lit.)
-
沸点:250.36°C (rough estimate)
-
密度:1.4295 (rough estimate)
-
溶解度:可溶于1MNaOH:25 mg/mL
-
LogP:-0.910 (est)
-
物理描述:Solid
-
水溶性:-2.29
-
碰撞截面:127.1 Ų [M+H]+ [CCS Type: DT, Method: single field calibrated with Agilent tune mix (Agilent)]
-
稳定性/保质期:
计算性质
-
辛醇/水分配系数(LogP):-1.1
-
重原子数:10
-
可旋转键数:0
-
环数:2.0
-
sp3杂化的碳原子比例:0.0
-
拓扑面积:70.1
-
氢给体数:2
-
氢受体数:2
ADMET
安全信息
-
TSCA:Yes
-
安全说明:S22,S24/25,S26,S37/39
-
危险品运输编号:NONH for all modes of transport
-
WGK Germany:3
-
海关编码:2933990090
-
危险品标志:Xn
-
危险类别码:R22,R36/37/38
-
RTECS号:UP0791000
-
危险性防范说明:P261,P305+P351+P338
-
危险性描述:H302,H315,H319,H335
-
储存条件:本品应密封、存放在阴凉干燥处。
SDS
模块 1. 化学品
1.1 产品标识符
: 次黄嘌呤
产品名称
: VetEC
1.2 鉴别的其他方法
无数据资料
1.3 有关的确定了的物质或混合物的用途和建议不适合的用途
仅供科研用途,不作为药物、家庭备用药或其它用途。
模块 2. 危险性概述
2.1 GHS分类
根据化学品全球统一分类与标签制度(GHS)的规定,不是危险物质或混合物。
2.3 其它危害物 - 无
模块 3. 成分/组成信息
3.1 物 质
: C5H4N4O
分子式
: 136.11 g/mol
分子量
无
模块 4. 急救措施
4.1 必要的急救措施描述
吸入
如果吸入,请将患者移到新鲜空气处。 如果停止了呼吸,给于人工呼吸。
皮肤接触
用肥皂和大量的水冲洗。
眼睛接触
用水冲洗眼睛作为预防措施。
食入
切勿给失去知觉者从嘴里喂食任何东西。 用水漱口。
4.2 主要症状和影响,急性和迟发效应
据我们所知,此化学,物理和毒性性质尚未经完整的研究。
4.3 及时的医疗处理和所需的特殊处理的说明和指示
无数据资料
模块 5. 消防措施
5.1 灭火介质
灭火方法及灭火剂
用水雾,耐醇泡沫,干粉或二氧化碳灭火。
5.2 源于此物质或混合物的特别的危害
碳氧化物, 氮氧化物
5.3 给消防员的建议
如必要的话,戴自给式呼吸器去救火。
5.4 进一步信息
无数据资料
模块 6. 泄露应急处理
6.1 人员的预防,防护设备和紧急处理程序
防止粉尘的生成。 防止吸入蒸汽、气雾或气体。
6.2 环境保护措施
不要让产物进入下水道。
6.3 抑制和清除溢出物的方法和材料
扫掉和铲掉。 存放进适当的闭口容器中待处理。
6.4 参考其他部分
丢弃处理请参阅第13节。
模块 7. 操作处置与储存
7.1 安全操作的注意事项
在有粉尘生成的地方,提供合适的排风设备。
7.2 安全储存的条件,包括任何不兼容性
贮存在阴凉处。 容器保持紧闭,储存在干燥通风处。
7.3 特定用途
无数据资料
模块 8. 接触控制和个体防护
8.1 容许浓度
最高容许浓度
没有已知的国家规定的暴露极限。
8.2 暴露控制
适当的技术控制
常规的工业卫生操作。
个体防护设备
眼/面保护
请使用经官方标准如NIOSH (美国) 或 EN 166(欧盟) 检测与批准的设备防护眼部。
皮肤保护
戴手套取 手套在使用前必须受检查。
请使用合适的方法脱除手套(不要接触手套外部表面),避免任何皮肤部位接触此产品.
使用后请将被污染过的手套根据相关法律法规和有效的实验室规章程序谨慎处理. 请清洗并吹干双手
所选择的保护手套必须符合EU的89/686/EEC规定和从它衍生出来的EN 376标准。
身体保护
根据危险物质的类型,浓度和量,以及特定的工作场所来选择人体保护措施。,
防护设备的类型必须根据特定工作场所中的危险物的浓度和含量来选择。
呼吸系统防护
不需要保护呼吸。如需防护粉尘损害,请使用N95型(US)或P1型(EN 143)防尘面具。
呼吸器使用经过测试并通过政府标准如NIOSH(US)或CEN(EU)的呼吸器和零件。
模块 9. 理化特性
9.1 基本的理化特性的信息
a) 外观与性状
形状: 粉末
颜色: 淡黄
b) 气味
无数据资料
c) 气味阈值
无数据资料
d) pH值
无数据资料
e) 熔点/凝固点
熔点/凝固点: > 300 °C
f) 起始沸点和沸程
无数据资料
g) 闪点
无数据资料
h) 蒸发速率
无数据资料
i) 易燃性(固体,气体)
无数据资料
j) 高的/低的燃烧性或爆炸性限度 无数据资料
k) 蒸汽压
无数据资料
l) 蒸汽密度
无数据资料
m) 相对密度
无数据资料
n) 水溶性
无数据资料
o) n-辛醇/水分配系数
无数据资料
p) 自燃温度
无数据资料
q) 分解温度
无数据资料
r) 粘度
无数据资料
模块 10. 稳定性和反应活性
10.1 反应性
无数据资料
10.2 稳定性
无数据资料
10.3 危险反应的可能性
无数据资料
10.4 应避免的条件
无数据资料
10.5 不兼容的材料
强氧化剂
10.6 危险的分解产物
模块 11. 毒理学资料
11.1 毒理学影响的信息
急性毒性
无数据资料
半数致死剂量 (LD50) 腹膜内的 - 老鼠 - 750 mg/kg
皮肤刺激或腐蚀
无数据资料
眼睛刺激或腐蚀
无数据资料
呼吸道或皮肤过敏
无数据资料
生殖细胞突变性
致癌性
IARC:
此产品中没有大于或等于 0。1%含量的组分被 IARC鉴别为可能的或肯定的人类致癌物。
生殖毒性
特异性靶器官系统毒性(一次接触)
无数据资料
特异性靶器官系统毒性(反复接触)
无数据资料
吸入危险
无数据资料
潜在的健康影响
吸入 吸入可能有害。 可能引起呼吸道刺激。
摄入 如服入是有害的。
皮肤 如果通过皮肤吸收可能是有害的。 可能引起皮肤刺激。
眼睛 可能引起眼睛刺激。
接触后的征兆和症状
据我们所知,此化学,物理和毒性性质尚未经完整的研究。
附加说明
化学物质毒性作用登记: 无数据资料
模块 12. 生态学资料
12.1 生态毒性
无数据资料
12.2 持久存留性和降解性
无数据资料
12.3 潜在的生物蓄积性
无数据资料
12.4 土壤中的迁移性
无数据资料
12.5 PBT 和 vPvB的结果评价
无数据资料
12.6 其它不利的影响
无数据资料
模块 13. 废弃处置
13.1 废物处理方法
产品
将剩余的和未回收的溶液交给处理公司。
受污染的容器和包装
作为未用过的产品弃置。
模块 14. 运输信息
14.1 联合国危险货物编号
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.2 联合国(UN)规定的名称
欧洲陆运危规: 非危险货物
国际海运危规: 非危险货物
国际空运危规: 非危险货物
14.3 运输危险类别
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.4 包裹组
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.5 环境危险
欧洲陆运危规: 否 国际海运危规 海运污染物: 否 国际空运危规: 否
14.6 对使用者的特别提醒
无数据资料
模块 15 - 法规信息
N/A
模块16 - 其他信息
N/A
制备方法与用途
次黄嘌呤是一种常见的嘌呤化合物,具有高活性的6-羟基功能团。其衍生物,如6-巯基嘌呤是重要的抗肿瘤药物和植物生长调节剂。由于嘌呤类化合物具有广泛的生物活性和应用价值,人们对于该类化合物的高效合成产生了浓厚兴趣。
次黄嘌呤与黄嘌呤一起广泛存在于动植物体中。其核苷酸肌苷酸是核酸的嘌呤核苷酸前体,并且也是咖啡因的母体。次黄嘌呤可通过腺嘌呤脱氨酶或亚硝酸的作用由腺嘌呤脱氨生成,也可通过核苷磷酸化酶使肌苷发生磷酸解而失成。
次黄嘌呤(hypoxanthine,Hx)是核苷的代谢产物,是一种重要的生物碱嘌呤,参与调节人体的一些生理机能。研究表明,Hx能促进小鼠脂肪分解,起到降低体内脂肪质量的作用。研究发现,在给药4周后,Hx给药组可以有效降低肥胖小鼠体质量、总脂肪质量和Lee's指数及脂肪系数,尤其是低剂量组与模型组的差异最为显著。
生物合成法在绝大多数微生物中,嘌呤的合成途径主要包括从头合成途径和补救途径。从头合成途径以5-磷酸核糖焦磷酸(PRPP)和谷氨酰胺为前体,经过10步反应合成次黄嘌呤核苷酸(IMP),随后IMP通过两条支路分别转化为腺苷单磷酸(AMP)和鸟苷单磷酸(GMP)。同时,IMP也可以进一步降解为次黄嘌呤。尽管从头合成途径早已探明,但该合成途径受到转录阻遏、转录衰减及底物反馈抑制等不同层面的严密调控,在天然状态下难以积累。
青岛能源所生物基材料组群赵广研究组近期在大肠杆菌内成功实现了次黄嘌呤的高效合成,并利用转录组学和荧光定量PCR技术分析了嘌呤代谢途径的合成调控机制。首先,通过解除调控蛋白PurR的转录阻遏、关键酶定点突变缓解底物反馈抑制、提高嘌呤合成前体的积累以及破坏IMP的分支代谢途径等方法,将次黄嘌呤的积累提高了近10倍。在5L发酵罐水平上,次黄嘌呤的积累达到了791.54 mg/L。然而,在次黄嘌呤发酵过程中发现副产物乙酸和黄嘌呤的显著积累。为解决这一问题,研究组发现全局调控因子ArcA在嘌呤代谢调控中具有较好的效果,乙酸副产物的积累从8.40 g/L降低至1.21 g/L,而次黄嘌呤的产量达到了1243 mg/L。
化学性质次黄嘌呤为针状结晶,熔点大于360℃。
用途次黄嘌呤可用作巯嘌呤和硫唑嘌呤的原料。同时,它还是抗恶性肿瘤药物6-巯基嘌呤(6-MP)的中间体。
生产方法通过氰乙酸乙酯与乙醇钠、硫脲经环合反应得到2-巯基-4-氨基-6-羟基嘧啶,再经过亚硝化、还原、消除和环合等步骤制得6-羟基嘌呤。
上下游信息
-
上游原料
中文名称 英文名称 CAS号 化学式 分子量 6-甲氧基嘌呤 6-methoxypurine 1074-89-1 C6H6N4O 150.14 黄嘌呤 xanthin 69-89-6 C5H4N4O2 152.112 嘌呤 purine 120-73-0 C5H4N4 120.114 2-氨基-6-甲氧基嘌呤 O6-methylguanine 20535-83-5 C6H7N5O 165.154 6-苄氧基嘌呤 6-benzyloxypurine 57500-07-9 C12H10N4O 226.238 尿酸 uric Acid 69-93-2 C5H4N4O3 168.112 —— 2,8-Dichlor-6-aethoxy-purin 5470-52-0 C7H6Cl2N4O 233.057 -
下游产品
中文名称 英文名称 CAS号 化学式 分子量 黄嘌呤 xanthin 69-89-6 C5H4N4O2 152.112 嘌呤 purine 120-73-0 C5H4N4 120.114 尿酸 uric Acid 69-93-2 C5H4N4O3 168.112 —— 6-[N-(2-Chloroethyl)-carbamoyl] oxypurine —— C8H8ClN5O2 241.637
反应信息
-
作为反应物:参考文献:名称:Means and method for the prevention and or treatment of trypanosomosis摘要:该发明提供了获得一种能够至少部分诱导锥虫生长停滞和/或细胞死亡的因子的手段和方法。该发明的手段包括可以从锥虫培养基中纯化的一个或多个因子,或者可以在化学合成或生物技术过程中生产的因子。该发明提供了用于制备治疗锥虫病的药物的方法。该发明还提供了疫苗和用于制备治疗锥虫病的疫苗的方法。公开号:EP1048728A1
-
作为产物:参考文献:名称:Sundwik, Hoppe-Seyler's Zeitschrift fur Physiologische Chemie, 1911, vol. 76, p. 487摘要:DOI:
-
作为试剂:描述:参考文献:名称:Tyrosine nitration in peptides by peroxynitrite generated in situ in a light-controlled platform: Effects of pH and thiols摘要:Peroxynitrite has been shown to play a critical role in inflammation and affords 3-nitrotyrosine as the hallmark product. The reported methods of generating this reactive nitrogen species in situ often fails to provide a high and steady flux of peroxynitrite resulting in poor yields of 3-nitrotyrosine. Herein we report a two-component peroxynitrite-generating platform in which this anion is produced in a biomimetic fashion and under the control of visible light. Incorporation of the nitric oxide- and superoxide-generating components in polymer matrices allows easy alterations of pH in the reaction wells of this platform. We have demonstrated very efficient nitration of tyrosine by peroxynitrite at different pH values and with varying concentrations of carbonate. In addition to tyrosine, a set of tyrosine-containing peptides was also studied. Presence of glutathione in the reaction wells increases the extent of tyrosine nitration in such peptide substrates presumably by raising the lifetime of nitric oxide in the reaction medium. When a cysteine residue was included in the sequence of the peptide, the extent of nitration of the tyrosine residue was found to depend on the position of the cysteine residue with respect to tyrosine. The extent of tyrosine nitration is strongly attenuated when the cysteine residue is directly adjacent to the tyrosine. This effect has been attributed to an intramolecular radical transfer mechanism. Taken together, results of this study demonstrate the potential of this light-controlled platform as a convenient bioanalytical tool in studying the reactions of peroxynitrite under widely varying conditions. (C) 2014 Elsevier Inc. All rights reserved.DOI:10.1016/j.jinorgbio.2014.04.018
文献信息
-
Thionations Using a P<sub>4</sub>S<sub>10</sub>−Pyridine Complex in Solvents Such as Acetonitrile and Dimethyl Sulfone作者:Jan Bergman、Birgitta Pettersson、Vedran Hasimbegovic、Per H. SvenssonDOI:10.1021/jo101865y日期:2011.3.18Tetraphosphorus decasulfide (P4S10) in pyridine has been used as a thionating agent for a long period of time. The moisture-sensitive reagent has now been isolated in crystalline form, and the detailed structure has been determined by X-ray crystallography. The thionating power of this storable reagent has been studied and transferred to solvents such as acetonitrile in which it has proven to be synthetically四硫化二磷(P 4 S 10)中的吡啶已长期用作硫代剂。现在已经以结晶形式分离出对水分敏感的试剂,并且已经通过X射线晶体学确定了详细的结构。已经研究了这种可储存试剂的去硫能力,并将其转移到诸如乙腈之类的溶剂中,在该溶剂中已证明其在合成上是有用的并且具有非凡的选择性。它的性能已经与所谓的Lawesson试剂(LR)进行了比较。特别有趣的是在相对较高的温度(约165°C)下以二甲基砜为溶剂进行硫磺化的结果。在这些条件下,例如,a啶酮和3-乙酰吲哚可以迅速转化为相应的亚硫代衍生物。甘氨酰甘氨酸类似地得到哌嗪去甲酮。在这些温度下 LR由于快速分解而效率低下。硫代产物通常更清洁并且更容易获得,因为在结晶试剂中,常规试剂P中始终存在杂质吡啶或LR中的4 S 10已被除去。
-
Direct <i>N</i><sup>9</sup>-arylation of purines with aryl halides作者:Anders Foller Larsen、Trond UlvenDOI:10.1039/c3cc48642g日期:——
The reported protocol is the first to be demonstrated to efficiently couple aryl halides to purines with predictable selectivity.
据报道的协议是第一个被证明能有效地将芳基卤化物与嘌呤以可预测的选择性偶联的协议。 -
Crystal and molecular structure of cis-dichloroethionineplatinum(II) and its interaction with adenine, hypoxanthine, cytosine and their nucleosides作者:Badar Taqui Khan、K. Venkatasubramanian、K. Najmuddin、S. Shamsuddin、S.M. ZakeeruddinDOI:10.1016/s0020-1693(00)85382-7日期:1991.1sulfur atoms to form a six-membered ring which adopts a skewed chair conformation. The predominant force of packing in this complex is the intermolecular hydrogen bonding between the two free carboxylic acid groups of adjacent molecules of ethionine. These are reinforced by weak NH…Cl bonds to stabilise crystal packing. Mixed ligand complexes of Pt(II)ethionine with adenine, adenosine, hypoxanthine, ionosine摘要用X射线衍射法测定了专利化合物顺式-二氯乙硫铂(II)的晶体和分子结构。该复合物在单斜空间群P 2 1 / n中具有4个分子的结晶,其晶胞尺寸为a = 7.223(1),b = 14.435(1),c = 11.012(2)A,β= 97.69(2)° 。该结构通过重原子方法求解,对于1573个观察到的反射,已将其精炼为R值为0.031。在顺式-二氯乙硫基铂(II)中,乙硫氨酸分子通过氨基氮和硫原子与铂配位,形成六元环,该环具有倾斜的椅子构象。在该络合物中的主要堆积力是相邻的乙硫氨酸分子的两个游离羧酸基团之间的分子间氢键。它们通过弱的NH…Cl键得到增强,以稳定晶体堆积。合成了Pt(II)乙硫氨酸与腺嘌呤,腺苷,次黄嘌呤,离子胞苷,胞嘧啶和胞嘧啶核苷的混合配体复合物,并通过元素分析,电导率测量,IR和1 H NMR光谱研究对其进行了表征。在腺嘌呤,腺苷,次黄嘌呤和ionosine的复合物中,配体与金属离子的结合位点为N
-
Palladium-Catalyzed Base-Selective H-D Exchange Reaction of Nucleosides in Deuterium Oxide作者:Hironao Sajiki、Hiroyoshi Esaki、Fumiyo Aoki、Tomohiro Maegawa、Kosaku HirotaDOI:10.1055/s-2005-868489日期:——We have developed an efficient and extensive deuterium incorporation method using a heterogeneous Pd/C-D 2 O-H 2 system into the base moiety of nucleosides. The results presented here provide a deuterium gas-free, totally catalytic, and post-synthetic deuterium labeling method in D 2 O media.
-
杂芳化合物及其在药物中的应用申请人:广东东阳光药业有限公司公开号:CN104744446B公开(公告)日:2019-06-25本发明提供一类杂芳化合物或其立体异构体,几何异构体,互变异构体,消旋体,氮氧化物,水合物,溶剂化物,代谢产物,代谢前体以及药学上可接受的盐或前药,用于治疗增殖性疾病。本发明还公开了含有这样的化合物的药物组合物和本发明化合物或其药物组合物在制备用于治疗增殖性疾病的药物中的用途。
表征谱图
-
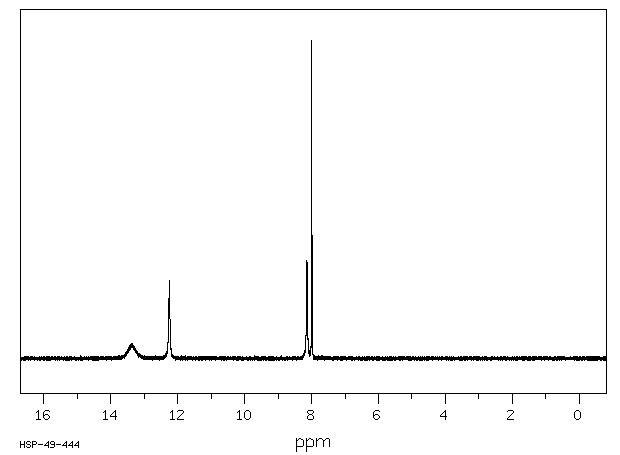
氢谱1HNMR
-
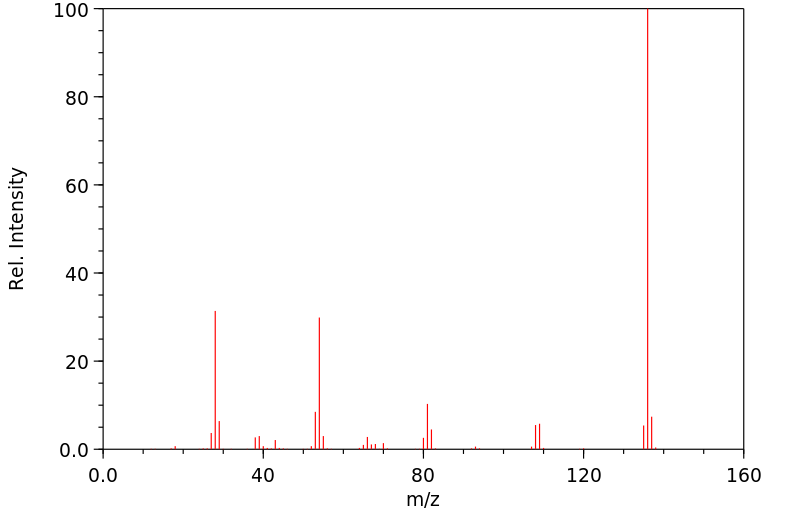
质谱MS
-
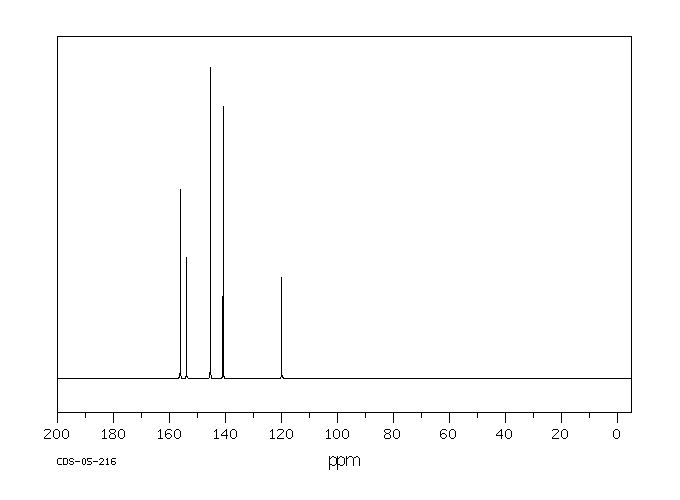
碳谱13CNMR
-
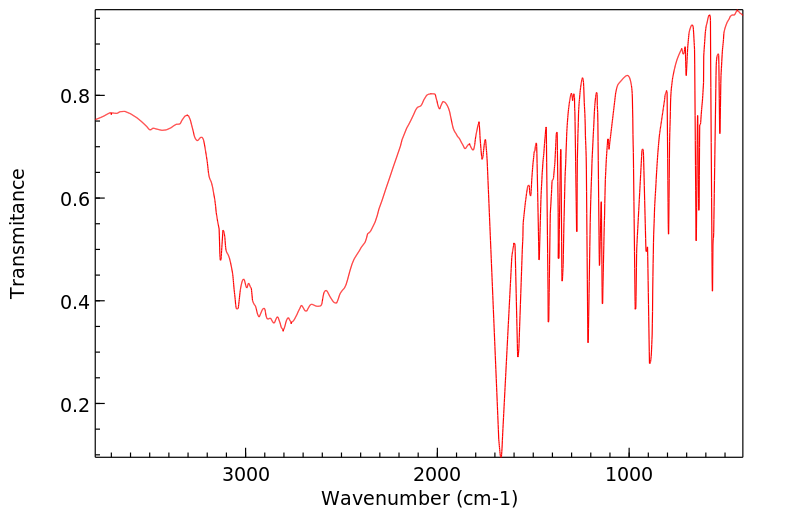
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息