L-缬氨酰基-L-酪氨酸 | 3061-91-4
中文名称
L-缬氨酰基-L-酪氨酸
中文别名
——
英文名称
L-valyl-L-tyrosine
英文别名
Val-Tyr;Val-Tyr-OH;valyl-tyrosine;valine-tyrosine;Angiotensin IV (1-2);(2S)-2-[[(2S)-2-amino-3-methylbutanoyl]amino]-3-(4-hydroxyphenyl)propanoic acid
CAS
3061-91-4
化学式
C14H20N2O4
mdl
——
分子量
280.324
InChiKey
VEYJKJORLPYVLO-RYUDHWBXSA-N
BEILSTEIN
——
EINECS
——
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
物化性质
-
熔点:245 - 248oC
-
沸点:555.1±50.0 °C(Predicted)
-
密度:1.245±0.06 g/cm3(Predicted)
-
溶解度:可溶于酸性水溶液(轻微)、DMSO(轻微、加热、超声处理)
-
物理描述:Solid
计算性质
-
辛醇/水分配系数(LogP):-1.9
-
重原子数:20
-
可旋转键数:5
-
环数:1.0
-
sp3杂化的碳原子比例:0.43
-
拓扑面积:117
-
氢给体数:3
-
氢受体数:4
安全信息
-
WGK Germany:3
-
海关编码:2924299090
-
危险性防范说明:P261,P305+P351+P338
-
危险性描述:H302,H315,H319,H335
SDS
1.1 产品标识符
: Val-Tyr
产品名称
1.2 鉴别的其他方法
无数据资料
1.3 有关的确定了的物质或混合物的用途和建议不适合的用途
仅供科研用途,不作为药物、家庭备用药或其它用途。
模块 2. 危险性概述
2.1 GHS分类
根据化学品全球统一分类与标签制度(GHS)的规定,不是危险物质或混合物。
2.3 其它危害物 - 无
模块 3. 成分/组成信息
3.1 物 质
: C14H20N2O4
分子式
: 280.32 g/mol
分子量
无
模块 4. 急救措施
4.1 必要的急救措施描述
吸入
如果吸入,请将患者移到新鲜空气处。 如果停止了呼吸,给于人工呼吸。
皮肤接触
用肥皂和大量的水冲洗。
眼睛接触
用水冲洗眼睛作为预防措施。
食入
切勿给失去知觉者从嘴里喂食任何东西。 用水漱口。
4.2 主要症状和影响,急性和迟发效应
据我们所知,此化学,物理和毒性性质尚未经完整的研究。
4.3 及时的医疗处理和所需的特殊处理的说明和指示
无数据资料
模块 5. 消防措施
5.1 灭火介质
灭火方法及灭火剂
用水雾,耐醇泡沫,干粉或二氧化碳灭火。
5.2 源于此物质或混合物的特别的危害
碳氧化物, 氮氧化物
5.3 给消防员的建议
如必要的话,戴自给式呼吸器去救火。
5.4 进一步信息
无数据资料
模块 6. 泄露应急处理
6.1 人员的预防,防护设备和紧急处理程序
防止粉尘的生成。 防止吸入蒸汽、气雾或气体。
6.2 环境保护措施
不要让产物进入下水道。
6.3 抑制和清除溢出物的方法和材料
扫掉和铲掉。 存放进适当的闭口容器中待处理。
6.4 参考其他部分
丢弃处理请参阅第13节。
模块 7. 操作处置与储存
7.1 安全操作的注意事项
在有粉尘生成的地方,提供合适的排风设备。一般性的防火保护措施。
7.2 安全储存的条件,包括任何不兼容性
贮存在阴凉处。 容器保持紧闭,储存在干燥通风处。
建议的贮存温度: -20 °C
7.3 特定用途
无数据资料
模块 8. 接触控制和个体防护
8.1 容许浓度
最高容许浓度
没有已知的国家规定的暴露极限。
8.2 暴露控制
适当的技术控制
常规的工业卫生操作。
个体防护设备
眼/面保护
请使用经官方标准如NIOSH (美国) 或 EN 166(欧盟) 检测与批准的设备防护眼部。
皮肤保护
戴手套取 手套在使用前必须受检查。
请使用合适的方法脱除手套(不要接触手套外部表面),避免任何皮肤部位接触此产品.
使用后请将被污染过的手套根据相关法律法规和有效的实验室规章程序谨慎处理. 请清洗并吹干双手
所选择的保护手套必须符合EU的89/686/EEC规定和从它衍生出来的EN 376标准。
身体保护
根据危险物质的类型,浓度和量,以及特定的工作场所来选择人体保护措施。,
防护设备的类型必须根据特定工作场所中的危险物的浓度和含量来选择。
呼吸系统防护
不需要保护呼吸。如需防护粉尘损害,请使用N95型(US)或P1型(EN 143)防尘面具。
呼吸器使用经过测试并通过政府标准如NIOSH(US)或CEN(EU)的呼吸器和零件。
模块 9. 理化特性
9.1 基本的理化特性的信息
a) 外观与性状
形状: 固体
b) 气味
无数据资料
c) 气味阈值
无数据资料
d) pH值
无数据资料
e) 熔点/凝固点
无数据资料
f) 起始沸点和沸程
无数据资料
g) 闪点
无数据资料
h) 蒸发速率
无数据资料
i) 易燃性(固体,气体)
无数据资料
j) 高的/低的燃烧性或爆炸性限度 无数据资料
k) 蒸汽压
无数据资料
l) 蒸汽密度
无数据资料
m) 相对密度
无数据资料
n) 水溶性
无数据资料
o) n-辛醇/水分配系数
无数据资料
p) 自燃温度
无数据资料
q) 分解温度
无数据资料
r) 粘度
无数据资料
模块 10. 稳定性和反应活性
10.1 反应性
无数据资料
10.2 稳定性
无数据资料
10.3 危险反应的可能性
无数据资料
10.4 应避免的条件
无数据资料
10.5 不兼容的材料
强氧化剂
10.6 危险的分解产物
其它分解产物 - 无数据资料
模块 11. 毒理学资料
11.1 毒理学影响的信息
急性毒性
无数据资料
皮肤刺激或腐蚀
无数据资料
眼睛刺激或腐蚀
无数据资料
呼吸道或皮肤过敏
无数据资料
生殖细胞突变性
无数据资料
致癌性
IARC:
此产品中没有大于或等于 0。1%含量的组分被 IARC鉴别为可能的或肯定的人类致癌物。
生殖毒性
无数据资料
特异性靶器官系统毒性(一次接触)
无数据资料
特异性靶器官系统毒性(反复接触)
无数据资料
吸入危险
无数据资料
潜在的健康影响
吸入 吸入可能有害。 可能引起呼吸道刺激。
摄入 如服入是有害的。
皮肤 如果通过皮肤吸收可能是有害的。 可能引起皮肤刺激。
眼睛 可能引起眼睛刺激。
接触后的征兆和症状
据我们所知,此化学,物理和毒性性质尚未经完整的研究。
附加说明
化学物质毒性作用登记: 无数据资料
模块 12. 生态学资料
12.1 生态毒性
无数据资料
12.2 持久存留性和降解性
无数据资料
12.3 潜在的生物蓄积性
无数据资料
12.4 土壤中的迁移性
无数据资料
12.5 PBT 和 vPvB的结果评价
无数据资料
12.6 其它不利的影响
无数据资料
模块 13. 废弃处置
13.1 废物处理方法
产品
将剩余的和未回收的溶液交给处理公司。
受污染的容器和包装
作为未用过的产品弃置。
模块 14. 运输信息
14.1 联合国危险货物编号
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.2 联合国(UN)规定的名称
欧洲陆运危规: 非危险货物
国际海运危规: 非危险货物
国际空运危规: 非危险货物
14.3 运输危险类别
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.4 包裹组
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.5 环境危险
欧洲陆运危规: 否 国际海运危规 海运污染物: 否 国际空运危规: 否
14.6 对使用者的特别提醒
无数据资料
模块 15 - 法规信息
N/A
模块16 - 其他信息
N/A
: Val-Tyr
产品名称
1.2 鉴别的其他方法
无数据资料
1.3 有关的确定了的物质或混合物的用途和建议不适合的用途
仅供科研用途,不作为药物、家庭备用药或其它用途。
模块 2. 危险性概述
2.1 GHS分类
根据化学品全球统一分类与标签制度(GHS)的规定,不是危险物质或混合物。
2.3 其它危害物 - 无
模块 3. 成分/组成信息
3.1 物 质
: C14H20N2O4
分子式
: 280.32 g/mol
分子量
无
模块 4. 急救措施
4.1 必要的急救措施描述
吸入
如果吸入,请将患者移到新鲜空气处。 如果停止了呼吸,给于人工呼吸。
皮肤接触
用肥皂和大量的水冲洗。
眼睛接触
用水冲洗眼睛作为预防措施。
食入
切勿给失去知觉者从嘴里喂食任何东西。 用水漱口。
4.2 主要症状和影响,急性和迟发效应
据我们所知,此化学,物理和毒性性质尚未经完整的研究。
4.3 及时的医疗处理和所需的特殊处理的说明和指示
无数据资料
模块 5. 消防措施
5.1 灭火介质
灭火方法及灭火剂
用水雾,耐醇泡沫,干粉或二氧化碳灭火。
5.2 源于此物质或混合物的特别的危害
碳氧化物, 氮氧化物
5.3 给消防员的建议
如必要的话,戴自给式呼吸器去救火。
5.4 进一步信息
无数据资料
模块 6. 泄露应急处理
6.1 人员的预防,防护设备和紧急处理程序
防止粉尘的生成。 防止吸入蒸汽、气雾或气体。
6.2 环境保护措施
不要让产物进入下水道。
6.3 抑制和清除溢出物的方法和材料
扫掉和铲掉。 存放进适当的闭口容器中待处理。
6.4 参考其他部分
丢弃处理请参阅第13节。
模块 7. 操作处置与储存
7.1 安全操作的注意事项
在有粉尘生成的地方,提供合适的排风设备。一般性的防火保护措施。
7.2 安全储存的条件,包括任何不兼容性
贮存在阴凉处。 容器保持紧闭,储存在干燥通风处。
建议的贮存温度: -20 °C
7.3 特定用途
无数据资料
模块 8. 接触控制和个体防护
8.1 容许浓度
最高容许浓度
没有已知的国家规定的暴露极限。
8.2 暴露控制
适当的技术控制
常规的工业卫生操作。
个体防护设备
眼/面保护
请使用经官方标准如NIOSH (美国) 或 EN 166(欧盟) 检测与批准的设备防护眼部。
皮肤保护
戴手套取 手套在使用前必须受检查。
请使用合适的方法脱除手套(不要接触手套外部表面),避免任何皮肤部位接触此产品.
使用后请将被污染过的手套根据相关法律法规和有效的实验室规章程序谨慎处理. 请清洗并吹干双手
所选择的保护手套必须符合EU的89/686/EEC规定和从它衍生出来的EN 376标准。
身体保护
根据危险物质的类型,浓度和量,以及特定的工作场所来选择人体保护措施。,
防护设备的类型必须根据特定工作场所中的危险物的浓度和含量来选择。
呼吸系统防护
不需要保护呼吸。如需防护粉尘损害,请使用N95型(US)或P1型(EN 143)防尘面具。
呼吸器使用经过测试并通过政府标准如NIOSH(US)或CEN(EU)的呼吸器和零件。
模块 9. 理化特性
9.1 基本的理化特性的信息
a) 外观与性状
形状: 固体
b) 气味
无数据资料
c) 气味阈值
无数据资料
d) pH值
无数据资料
e) 熔点/凝固点
无数据资料
f) 起始沸点和沸程
无数据资料
g) 闪点
无数据资料
h) 蒸发速率
无数据资料
i) 易燃性(固体,气体)
无数据资料
j) 高的/低的燃烧性或爆炸性限度 无数据资料
k) 蒸汽压
无数据资料
l) 蒸汽密度
无数据资料
m) 相对密度
无数据资料
n) 水溶性
无数据资料
o) n-辛醇/水分配系数
无数据资料
p) 自燃温度
无数据资料
q) 分解温度
无数据资料
r) 粘度
无数据资料
模块 10. 稳定性和反应活性
10.1 反应性
无数据资料
10.2 稳定性
无数据资料
10.3 危险反应的可能性
无数据资料
10.4 应避免的条件
无数据资料
10.5 不兼容的材料
强氧化剂
10.6 危险的分解产物
其它分解产物 - 无数据资料
模块 11. 毒理学资料
11.1 毒理学影响的信息
急性毒性
无数据资料
皮肤刺激或腐蚀
无数据资料
眼睛刺激或腐蚀
无数据资料
呼吸道或皮肤过敏
无数据资料
生殖细胞突变性
无数据资料
致癌性
IARC:
此产品中没有大于或等于 0。1%含量的组分被 IARC鉴别为可能的或肯定的人类致癌物。
生殖毒性
无数据资料
特异性靶器官系统毒性(一次接触)
无数据资料
特异性靶器官系统毒性(反复接触)
无数据资料
吸入危险
无数据资料
潜在的健康影响
吸入 吸入可能有害。 可能引起呼吸道刺激。
摄入 如服入是有害的。
皮肤 如果通过皮肤吸收可能是有害的。 可能引起皮肤刺激。
眼睛 可能引起眼睛刺激。
接触后的征兆和症状
据我们所知,此化学,物理和毒性性质尚未经完整的研究。
附加说明
化学物质毒性作用登记: 无数据资料
模块 12. 生态学资料
12.1 生态毒性
无数据资料
12.2 持久存留性和降解性
无数据资料
12.3 潜在的生物蓄积性
无数据资料
12.4 土壤中的迁移性
无数据资料
12.5 PBT 和 vPvB的结果评价
无数据资料
12.6 其它不利的影响
无数据资料
模块 13. 废弃处置
13.1 废物处理方法
产品
将剩余的和未回收的溶液交给处理公司。
受污染的容器和包装
作为未用过的产品弃置。
模块 14. 运输信息
14.1 联合国危险货物编号
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.2 联合国(UN)规定的名称
欧洲陆运危规: 非危险货物
国际海运危规: 非危险货物
国际空运危规: 非危险货物
14.3 运输危险类别
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.4 包裹组
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.5 环境危险
欧洲陆运危规: 否 国际海运危规 海运污染物: 否 国际空运危规: 否
14.6 对使用者的特别提醒
无数据资料
模块 15 - 法规信息
N/A
模块16 - 其他信息
N/A
制备方法与用途
生物活性的H-Val-Tyr-OH是一种内源性代谢产物。
| 人类内源性代谢物 |
|---|
上下游信息
-
上游原料
中文名称 英文名称 CAS号 化学式 分子量 苄氧羰基-缬氨酰-酪氨酸 Z-Val-Tyr-OH 862-26-0 C22H26N2O6 414.458 —— N-(N-benzyloxycarbonyl-L-valyl)-L-tyrosine methyl ester 15149-72-1 C23H28N2O6 428.485 —— N-benzoxycarbonyl-L-valyl-O-benzyl-L-tyrosine 264887-57-2 C29H32N2O6 504.583 叔丁氧羰基-缬氨酰-酪氨酸苄酯 Boc-Val-Tyr-OBzl 75957-53-8 C26H34N2O6 470.566
反应信息
-
作为反应物:描述:参考文献:名称:Preparation of substituted N-carboxymethyl dipeptides摘要:DOI:10.1016/s0040-4039(00)88678-5
-
作为产物:描述:参考文献:名称:合成具有Val 5高血压素I(L-天冬酰胺基-L-精氨酰基-L-戊基-L-酪氨酰基-L-戊基-L-组氨酸-L-脯氨酰基-L-苯丙氨酰基-L-组氨酸-L-亮氨酸和L-天冬酰胺基-L-精氨酸-L-戊基-L-酪氨酰基-L-戊基-L-组氨酸-L-脯氨酰基-L-苯丙氨酰基-L-组氨酸-L-亮氨酸)摘要:先前公开的具有Val 5-高血压蛋白I氨基酸序列的十肽合成(4)已重复了几次。产物显示出高血压活性,与相应的八肽[Val 5-高血压蛋白II和Val 5-高血压蛋白II-Asp-β-酰胺(12)]相当。本文描述了产生最纯净的中间体和产物的合成方法。合成的Val 5-高血压蛋白I和Val 5的化学纯度很高通过逆流分布,纸色谱,元素分析和水解后的氨基酸测定来确定β-高血压蛋白I-Asp-β-酰胺。游离的结晶肽H•Val-Tyr•OH(L-L),H•Val-His•OH(L-L),H•Val-Tyr-Val•OH(L 3),H•Val-Tyr -Val-His ·OH(L 4)和H·Pro-Phe·OH(L-L)由合成中间体制备。DOI:10.1002/hlca.19580410512
文献信息
-
Inhibitors of Tripeptidyl Peptidase II. 2. Generation of the First Novel Lead Inhibitor of Cholecystokinin-8-Inactivating Peptidase: A Strategy for the Design of Peptidase Inhibitors作者:C. Robin Ganellin、Paul B. Bishop、Ramesh B. Bambal、Suzanne M. T. Chan、James K. Law、Benoit Marabout、Pratibha Mehta Luthra、Andrew N. J. Moore、Olivier Peschard、Pierre Bourgeat、Christiane Rose、Froylan Vargas、Jean-Charles SchwartzDOI:10.1021/jm990226g日期:2000.2.1fluorimetric assay based on the hydrolysis of the artificial substrate Ala-Ala-Phe-amidomethylcoumarin. A series of di- and tripeptides having various alkyl or aryl side chains was studied to determine the accessible volume for binding and to probe the potential for hydrophobic interactions. From this initial study the tripeptides Ile-Pro-Ile-OH (K(i) = 1 microM) and Ala-Pro-Ala-OH (K(i) = 3 microM) and dipeptide失活胆囊收缩素8(CCK-8)的肽酶是一种丝氨酸肽酶,已证明是三肽基肽酶II的膜结合同工型(EC 3.4.14.10)。它在Met-Gly键处裂解神经递质CCK-8硫酸盐,得到Asp-Tyr(SO(3)H)-Met-OH + Gly-Trp-Met-Asp-Phe-NH(2)。为了寻找该肽酶的可逆抑制剂,使用基于人工底物Ala-Ala-Phe-酰胺基甲基香豆素水解的荧光分析法来表征酶促结合亚位点。对具有各种烷基或芳基侧链的一系列二肽和三肽进行了研究,以确定可结合的体积并探讨疏水相互作用的可能性。根据这项初步研究,三肽Ile-Pro-Ile-OH(K(i)= 1 microM)和Ala-Pro-Ala-OH(K(i)= 3 microM)和二肽酰胺Val-Nvl-NHBu(K( i)= 3 microM)作为线索出现。这些结构的比较导致Val-Pro-NHBu(K(i)= 0.57 micr
-
The effect of thymopoietin II fragments and their analogs on E-rosette forming cells in the uremic state.作者:TAKASHI ABIKO、IKUKO ONODERA、HIROSHI SEKINODOI:10.1248/cpb.28.2507日期:——The synthesis of four fragments from dipeptide to pentapeptide, corresponding to amino acids 32 to 36 of thymopoietin II, and four analogs is described, together with their effects on E-rosette forming cells in the uremic state. After incubation with amounts of H-Arg-Lys-Asp-Val-Tyr-OH (residues 32-36) varying from 100 to 200 μg/ml of cell suspension, maximum T-cell rosette formation ranged from 65 to 73% compared with 50 to 52% without the peptide. The activity of H-Arg-Lys-Glu-Val-Tyr-OH was lower than that of H-Arg-Lys-Asp-Val-Tyr-OH. The other fragments and analogs had no effect on the E-rosette formation-inhibiting activity of uremic serum at a dose of 200 μg/ml
-
Preparation, Isolation, and Characterization of <i>N</i><sup>α</sup>-Fmoc-peptide Isocyanates: Solution Synthesis of Oligo-α-peptidyl Ureas作者:Vommina V. Sureshbabu、Basanagoud S. Patil、Rao VenkataramanaraoDOI:10.1021/jo0611723日期:2006.9.1Nα-Fmoc-tripeptidyl urea ester and acids containing one each of peptide bond and urea bond. The divergent approach is extended to the synthesis of tetrapeptidyl ureas by the 2 + 2 strategy using bis-TMS−peptide acid as an amino component. To incorporate urea bonds in adjacent positions, Nα-Fmoc-peptidyl urea isocyanates 9a−d were prepared and employed in the synthesis of three tetrapeptidyl ureas 10a−b and 11所述Ñ α -Fmoc-肽的异氰酸酯3A - q,4A - Ç,和图5a - ç通过的Curtius重排制备Ñ α -Fmoc-肽酰基叠氮于甲苯下热,微波,和超声波的条件。所有Ñ α -Fmoc-低聚肽的异氰酸酯制成,分离稳定的结晶固体用71至94%的产率,并通过被完全表征1 H NMR,13 C NMR和质谱。其为寡-α肽脲的合成效用7A - ˚F和图8a -c通过发散耦合法得到证明。的耦合Ñ α -Fmoc-二肽的异氰酸酯与氨基酸酯或具有N,O二(三甲基硅基)氨基酸导致Ñ α -Fmoc-三肽基脲酯和含有各一个肽键和脲键的羧酸。发散的方法扩展到使用双-TMS-肽酸作为氨基成分的2 + 2策略合成四肽基脲。为了将脲键在相邻的位置,Ñ α -Fmoc肽尿素异氰酸9A - d被制备并在三个四肽脲的合成10a的- b和从N-末端开始连续包含一个肽键和两个脲键的11。然后该协议用于五个尿素的类似物的合成13
-
Protecting group free radical C–H trifluoromethylation of peptides作者:Naoko Ichiishi、John P. Caldwell、Melissa Lin、Wendy Zhong、Xiaohong Zhu、Eric Streckfuss、Hai-Young Kim、Craig A. Parish、Shane W. KrskaDOI:10.1039/c8sc00368h日期:——approaches have been developed to effect the trifluoromethylation of aryl C–H bonds in native peptides either using stoichiometric oxidant or visible light photoredox catalysis. The reported methods are able to derivatize tyrosine and tryptophan sidechains under biocompatible conditions, and a number of examples are reported involving fully unprotected peptides with up to 51 amino acids. The development
-
Enhanced carboxypeptidase efficacies and differentiation of peptide epimers作者:Yu-Sheng Sung、Joshua Putman、Siqi Du、Daniel W. ArmstrongDOI:10.1016/j.ab.2021.114451日期:2022.4Carboxypeptidases enzymatically cleaves the peptide bond of C-terminal amino acids within peptides. In humans, it is involved in enzymatic synthesis and maturation of proteins and peptides. Carboxypeptidases A and Y have difficulty hydrolyzing the peptide bond of dipeptides and some other amino acid sequences. Early investigations into different N-blocking groups concluded that larger moieties increased羧肽酶酶促切割肽内C-末端氨基酸的肽键。在人类中,它参与蛋白质和肽的酶促合成和成熟。羧肽酶 A 和 Y 难以水解二肽的肽键和一些其他氨基酸序列。对不同 N 阻断基团的早期研究得出结论,较大的部分增加了底物对用羧肽酶水解肽键的敏感性。该研究最终证明 6-氨基喹啉-N-羟基琥珀酰亚胺氨基甲酸酯 (AQC) 作为 N 封闭基团极大地增强了羧肽酶的底物水解。在氨基酸和肽的 N 末端添加 AQC 还可以通过质谱检测改善色谱峰形和灵敏度。在现代蛋白质组学出现之前,这些酶已用于氨基酸序列测定。然而,大多数现代蛋白质组学方法假定所有肽都由l-氨基酸,因此无法区分肽序列中的 L-和d-氨基酸。允许手性分化的大多数现有方法要么需要合成标准,要么在该过程中引起外消旋化。该研究强调了肽内d-氨基酸对羧肽酶 Y 酶水解的抗性。这种立体选择性在筛选低丰度肽差向异构体时可能是有利的。
表征谱图
-
氢谱1HNMR
-
质谱MS
-
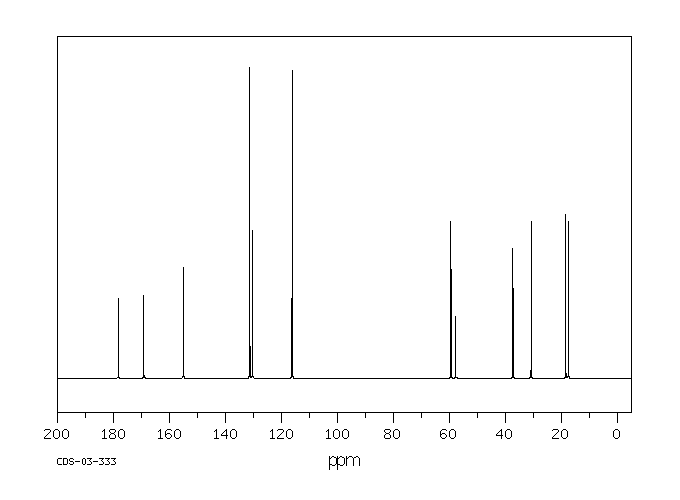
碳谱13CNMR
-
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息
同类化合物
(甲基3-(二甲基氨基)-2-苯基-2H-azirene-2-羧酸乙酯)
(±)-盐酸氯吡格雷
(±)-丙酰肉碱氯化物
(d(CH2)51,Tyr(Me)2,Arg8)-血管加压素
(S)-(+)-α-氨基-4-羧基-2-甲基苯乙酸
(S)-阿拉考特盐酸盐
(S)-赖诺普利-d5钠
(S)-2-氨基-5-氧代己酸,氢溴酸盐
(S)-2-[[[(1R,2R)-2-[[[3,5-双(叔丁基)-2-羟基苯基]亚甲基]氨基]环己基]硫脲基]-N-苄基-N,3,3-三甲基丁酰胺
(S)-2-[3-[(1R,2R)-2-(二丙基氨基)环己基]硫脲基]-N-异丙基-3,3-二甲基丁酰胺
(S)-1-(4-氨基氧基乙酰胺基苄基)乙二胺四乙酸
(S)-1-[N-[3-苯基-1-[(苯基甲氧基)羰基]丙基]-L-丙氨酰基]-L-脯氨酸
(R)-乙基N-甲酰基-N-(1-苯乙基)甘氨酸
(R)-丙酰肉碱-d3氯化物
(R)-4-N-Cbz-哌嗪-2-甲酸甲酯
(R)-3-氨基-2-苄基丙酸盐酸盐
(R)-1-(3-溴-2-甲基-1-氧丙基)-L-脯氨酸
(N-[(苄氧基)羰基]丙氨酰-N〜5〜-(diaminomethylidene)鸟氨酸)
(6-氯-2-吲哚基甲基)乙酰氨基丙二酸二乙酯
(4R)-N-亚硝基噻唑烷-4-羧酸
(3R)-1-噻-4-氮杂螺[4.4]壬烷-3-羧酸
(3-硝基-1H-1,2,4-三唑-1-基)乙酸乙酯
(2S,4R)-Boc-4-环己基-吡咯烷-2-羧酸
(2S,3S,5S)-2-氨基-3-羟基-1,6-二苯己烷-5-N-氨基甲酰基-L-缬氨酸
(2S,3S)-3-((S)-1-((1-(4-氟苯基)-1H-1,2,3-三唑-4-基)-甲基氨基)-1-氧-3-(噻唑-4-基)丙-2-基氨基甲酰基)-环氧乙烷-2-羧酸
(2S)-2,6-二氨基-N-[4-(5-氟-1,3-苯并噻唑-2-基)-2-甲基苯基]己酰胺二盐酸盐
(2S)-2-氨基-N,3,3-三甲基-N-(苯甲基)丁酰胺
(2S)-2-氨基-3-甲基-N-2-吡啶基丁酰胺
(2S)-2-氨基-3,3-二甲基-N-(苯基甲基)丁酰胺,
(2S)-2-氨基-3,3-二甲基-N-2-吡啶基丁酰胺
(2S,4R)-1-((S)-2-氨基-3,3-二甲基丁酰基)-4-羟基-N-(4-(4-甲基噻唑-5-基)苄基)吡咯烷-2-甲酰胺盐酸盐
(2R,3'S)苯那普利叔丁基酯d5
(2R)-2-氨基-3,3-二甲基-N-(苯甲基)丁酰胺
(2-氯丙烯基)草酰氯
(1S,3S,5S)-2-Boc-2-氮杂双环[3.1.0]己烷-3-羧酸
(1R,5R,6R)-5-(1-乙基丙氧基)-7-氧杂双环[4.1.0]庚-3-烯-3-羧酸乙基酯
(1R,4R,5S,6R)-4-氨基-2-氧杂双环[3.1.0]己烷-4,6-二羧酸
齐特巴坦
齐德巴坦钠盐
齐墩果-12-烯-28-酸,2,3-二羟基-,苯基甲基酯,(2a,3a)-
齐墩果-12-烯-28-酸,2,3-二羟基-,羧基甲基酯,(2a,3b)-(9CI)
黄酮-8-乙酸二甲氨基乙基酯
黄荧菌素
黄体生成激素释放激素(1-6)
黄体生成激素释放激素 (1-5) 酰肼
黄体瑞林
麦醇溶蛋白
麦角硫因
麦芽聚糖六乙酸酯
麦根酸