3α-hydroxyreynosin
中文名称
——
中文别名
——
英文名称
3α-hydroxyreynosin
英文别名
3α-hydroxylreynosin;Cxfaeusgwyviju-xfkurjonsa-;(3aS,5aR,6R,8R,9aS,9bS)-6,8-dihydroxy-5a-methyl-3,9-dimethylidene-3a,4,5,6,7,8,9a,9b-octahydrobenzo[g][1]benzofuran-2-one
CAS
——
化学式
C15H20O4
mdl
——
分子量
264.321
InChiKey
CXFAEUSGWYVIJU-XFKURJONSA-N
BEILSTEIN
——
EINECS
——
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
计算性质
-
辛醇/水分配系数(LogP):0.9
-
重原子数:19
-
可旋转键数:0
-
环数:3.0
-
sp3杂化的碳原子比例:0.67
-
拓扑面积:66.8
-
氢给体数:2
-
氢受体数:4
上下游信息
反应信息
-
作为反应物:描述:参考文献:名称:从广玉兰中发现多种倍半萜类化合物,通过诱导细胞凋亡具有细胞毒活性摘要:对广玉兰的植物化学研究分离出 39 种倍半萜类化合物,其中包括 15 种新化合物 ( 1 – 15 )。化合物1和2是天然产物中第一个被发现的13-norgermacrane型倍半萜类化合物。化合物15是一种罕见的5,6-仲愈创木烷型倍半萜,推测其可能的生物前体是化合物20。随后对化合物28进行结构修饰,得到21个衍生物,其中15个衍生物为新化合物。测试了所有化合物对三种肿瘤细胞系的抑制作用,其中 17 种化合物具有活性,IC 50值范围为 1.91 ± 0.39 μM 至 12.29 ± 1.68 μM。构效关系表明α , β-不饱和内酯基团是细胞毒性的重要活性基团。选择对正常人肝细胞系低毒性的两种最活跃的化合物(19和29 )进行进一步的机制研究。化合物29可以通过影响关键的凋亡相关蛋白,如PARP、Cleaved PARP、cleaved Caspase-3和pro-CaspaseDOI:10.1016/j.bioorg.2023.106707
-
作为产物:描述:参考文献:名称:丝状真菌和细胞毒性评价对一些倍半萜内酯的转化。摘要:生物转化是一种经济上和生态上可行的技术,已被用于修饰许多类生物活性产品的结构。一些真菌可能对倍半萜内酯(SLs)的生物转化有用,导致异常结构改变,从而改变其生物活性,而其他转化则模仿其生物合成途径,从而为拟议的生物发生提供证据。筛选了八种丝状真菌转化不同SL的能力(1-9),微生物反应产生的化合物10-17反过来又被分离为天然产物,从而模拟了它们的生物合成。根据NMR和MS光谱分析鉴定了它们的结构。SL 1、4、6、7和9及其生物转化产物的细胞毒性(10、14,DOI:10.1002/cbdv.201700211
文献信息
-
Effects of Solvents and Water in Ti(III)-Mediated Radical Cyclizations of Epoxygermacrolides. Straightforward Synthesis and Absolute Stereochemistry of (+)-3α-Hydroxyreynosin and Related Eudesmanolides作者:Alejandro F. Barrero、J. Enrique Oltra、Juan M. Cuerva、Antonio RosalesDOI:10.1021/jo016277e日期:2002.4.1was carried out using different solvents and additives to develop an expeditious procedure for the synthesis of natural eudesmanolides via free-radical chemistry. In the nonhalogenated solvents THF, benzene, and toluene the transannular cyclization, initiated by the homolytic opening of the oxirane ring, selectively led to the desired exocyclic alkene 5. When water was added to THF, however, the mainCp(2)TiCl介导的1,10-环氧-11beta,13-二氢木香酚(4)的重排使用不同的溶剂和添加剂进行,以开发通过自由基化学合成天然eudesmanolides的快速程序。在非卤代溶剂THF,苯和甲苯中,由环氧乙烷环的均相开环引发的环环环化选择性地导致形成所需的环外烯烃5.然而,将水添加到THF中时,主要产物是还原的奥德曼醇化物8。 D(2)O的实验证实8的H-4来自水。为了使这些结果合理化,提出了一种基于水溶剂化的Cp(2)TiCl复合物的机理假说。最后,在化学制备(+)-3α-羟基雷诺菌素(1)和(+)-雷诺菌素(17)的关键步骤中,已证明使用该试剂可证明Cp(2)TiCl可以用于合成天然奥地香奈德。这些合成证实了1的化学结构,并建立了天然产物1和17的绝对立体化学。获得的结果表明,采用仿生策略与Ti(III)介导的自由基化学的结合可能代表了一种对映体特异性合成170多种在C-4
-
Sesquiterpene lactones and flavonoids from Artemisia ludoviciana ssp. mexicana作者:Alejandro Ruiz-Cancino、Arturo E. Cano、Guillermo DelgadoDOI:10.1016/0031-9422(93)85032-m日期:1993.7Abstract From the aerial parts of the medicinal plant Artemisia ludoviciana spp. mexicana were isolated douglanin, ludovicin A, 1α,3α-dihydroxyarbusculin B, santamarin, arglanin, artemorin, chrysartemin B, armefolin, ridentin, the new eudesmanolide 3α-hydroxyreynosin, and the flavonoids eupatilin and jaceosidin.摘要来自药用植物 Artemisia ludoviciana spp. 的地上部分。mexicana 分别分离出花旗苷、ludovicin A、1α,3α-dihydroxyarbusculin B、santamarin、arglanin、artemorin、chrysartemin B、armefolin、ridentin、新eudesmanolide 3α-hydroxyreynosin,以及黄酮类化合物eupatilin 和 jaceosidin。
-
Synthesis and anti-fibrotic effects of santamarin derivatives as cytotoxic agents against hepatic stellate cell line LX2作者:Jin-Ping Wang、Tian-Ze Li、Xiao-Yan Huang、Chang-An Geng、Cheng Shen、Jin-Jin Sun、Dong Xue、Ji-Jun ChenDOI:10.1016/j.bmcl.2021.127994日期:2021.6
-
Sunflower sesquiterpene lactone models induce Orobanche cumana seed germination作者:Alejandro Pérez de Luque、Juan Carlos G. Galindo、Francisco A. Macı́as、Jesús Jorrı́nDOI:10.1016/s0031-9422(99)00485-9日期:2000.1Six sunflower sesquiterpene lactone models which share structural features of the lactone rings of strigol and its synthetic analogues, the GR family, with different conformational flexibilities were tested as Orobanche cumana germination stimulants. Among them, parthenolide and 3,5-dihydroxydehydrocostus-lactone significantly increased O. cumana germination, presenting higher activity than GR-24, used as a standard in the germination bioassay. The effect of these two compounds is species-specific, showing no germination stimulant activity on other Orobanche spp. tested (O. crenata, O. ramosa and O. aegyptiaca). Data presented are discussed in terms of a structure-activity relationship. (C) 2000 Elsevier Science Ltd. All rights reserved.
表征谱图
-
氢谱1HNMR
-
质谱MS
-
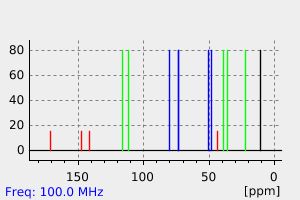
碳谱13CNMR
-
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息
同类化合物
(5β,6α,8α,10α,13α)-6-羟基-15-氧代黄-9(11),16-二烯-18-油酸
(3S,3aR,8aR)-3,8a-二羟基-5-异丙基-3,8-二甲基-2,3,3a,4,5,8a-六氢-1H-天青-6-酮
(2Z)-2-(羟甲基)丁-2-烯酸乙酯
(2S,4aR,6aR,7R,9S,10aS,10bR)-甲基9-(苯甲酰氧基)-2-(呋喃-3-基)-十二烷基-6a,10b-二甲基-4,10-dioxo-1H-苯并[f]异亚甲基-7-羧酸盐
(1aR,4E,7aS,8R,10aS,10bS)-8-[((二甲基氨基)甲基]-2,3,6,7,7a,8,10a,10b-八氢-1a,5-二甲基-氧杂壬酸[9,10]环癸[1,2-b]呋喃-9(1aH)-酮
(+)顺式,反式-脱落酸-d6
龙舌兰皂苷乙酯
龙脑香醇酮
龙脑烯醛
龙脑7-O-[Β-D-呋喃芹菜糖基-(1→6)]-Β-D-吡喃葡萄糖苷
龙牙楤木皂甙VII
龙吉甙元
齿孔醇
齐墩果醛
齐墩果酸苄酯
齐墩果酸甲酯
齐墩果酸溴乙酯
齐墩果酸二甲胺基乙酯
齐墩果酸乙酯
齐墩果酸3-O-alpha-L-吡喃鼠李糖基(1-3)-beta-D-吡喃木糖基(1-3)-alpha-L-吡喃鼠李糖基(1-2)-alpha-L-阿拉伯糖吡喃糖苷
齐墩果酸 beta-D-葡萄糖酯
齐墩果酸 beta-D-吡喃葡萄糖基酯
齐墩果酸 3-乙酸酯
齐墩果酸 3-O-beta-D-葡吡喃糖基 (1→2)-alpha-L-吡喃阿拉伯糖苷
齐墩果酸
齐墩果-12-烯-3b,6b-二醇
齐墩果-12-烯-3,24-二醇
齐墩果-12-烯-3,21,23-三醇,(3b,4b,21a)-(9CI)
齐墩果-12-烯-3,21,23-三醇,(3b,4b,21a)-(9CI)
齐墩果-12-烯-3,11-二酮
齐墩果-12-烯-2α,3β,28-三醇
齐墩果-12-烯-29-酸,3,22-二羟基-11-羰基-,g-内酯,(3b,20b,22b)-
齐墩果-12-烯-28-酸,3-[(6-脱氧-4-O-b-D-吡喃木糖基-a-L-吡喃鼠李糖基)氧代]-,(3b)-(9CI)
齐墩果-12-烯-28-酸,3,7-二羰基-(9CI)
齐墩果-12-烯-28-酸,3,21,29-三羟基-,g-内酯,(3b,20b,21b)-(9CI)
鼠特灵
鼠尾草酸醌
鼠尾草酸
鼠尾草酚酮
鼠尾草苦内脂
黑蚁素
黑蔓醇酯B
黑蔓醇酯A
黑蔓酮酯D
黑海常春藤皂苷A1
黑檀醇
黑果茜草萜 B
黑五味子酸
黏黴酮
黏帚霉酸