异噻唑-5-甲醛 | 5242-57-9
中文名称
异噻唑-5-甲醛
中文别名
——
英文名称
isothiazole-5-carbaldehyde
英文别名
5-Formyl-isothiazol;isothiazole-5-carboxaldehyde;1,2-thiazole-5-carbaldehyde
CAS
5242-57-9
化学式
C4H3NOS
mdl
MFCD07369962
分子量
113.14
InChiKey
TVFJIXAFZXREJQ-UHFFFAOYSA-N
BEILSTEIN
——
EINECS
——
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
物化性质
-
沸点:100.7℃
-
密度:1.350
-
闪点:14.7℃
计算性质
-
辛醇/水分配系数(LogP):0.8
-
重原子数:7
-
可旋转键数:1
-
环数:1.0
-
sp3杂化的碳原子比例:0.0
-
拓扑面积:58.2
-
氢给体数:0
-
氢受体数:3
安全信息
-
海关编码:2934999090
SDS
制备方法与用途
异噻唑-5-甲醛是一种医药中间体,有文献报道其可用于制备PFKFB3和/或PFKFB4的抑制剂。
制备将羟胺-O-磺酸(730 mg,6.5 mmol)溶解于2.5 mL水中,并冷却至0°C。随后加入1 g(6.5 mmol)4,4-二乙氧基丁-2-炔醛处理反应混合物,在0°C下搅拌10分钟后,滴加一当量的固体碳酸氢钠(545 mg,6.5 mmol),再加入5 mL(7.1 mmol,1.4 M)NaSH水溶液。将混合物温热至室温并保持3小时,然后用水和乙醚洗涤,有机相真空浓缩得到纯净的异噻唑二乙缩醛(370 mg)。接着,将该缩醛(370 mg,1.98 mmol)溶解在10 mL湿丙酮中,并用催化量对甲苯磺酸处理。混合物加热回流1小时后冷却至23°C,在饱和碳酸氢钠水溶液和乙醚之间分配有机相并真空浓缩,最终得到标题化合物(产率:330 mg)。
反应信息
-
作为反应物:参考文献:名称:具有异噻唑并乙烯基侧链的新型1β-甲基卡宾烯的合成和生物学评估。摘要:描述了在吡咯烷环的C-5位置带有异噻唑并乙烯基的新型1β-甲基碳烯化合物1a,b的合成及其生物学评价。两种化合物均显示出有效且均衡的抗菌活性以及对DHP-1的高稳定性。特别是,与5-异恶唑衍生物2,亚胺培南和美洛培南相比,5-异噻唑衍生物1a表现出出色的DHP-1稳定性和先进的药代动力学特性。DOI:10.1016/s0960-894x(02)00948-4
-
作为产物:参考文献:名称:[EN] 4-[(4-(CARBOXYETHYL) PIPERIDINYL) METHYL] PYRROLIDINES AS MODULATORS OF CHEMOKINE RECEPTOR ACTIVITY
[FR] 4-[(4-(CARBOXYETHYL)PIPERIDINYL)METHYL]PYRROLIDINES SERVANT DE MODULATEURS DE L'ACTIVITE DES RECEPTEURS DES CHIMIOKINES摘要:公开号:WO2004058702A3
文献信息
-
COMPOUNDS AND USES THEREOF申请人:Yumanity Therapeutics, Inc.公开号:US20190330198A1公开(公告)日:2019-10-31The present invention features compounds useful in the treatment of neurological disorders. The compounds of the invention, alone or in combination with other pharmaceutically active agents, can be used for treating or preventing neurological disorders.本发明涉及用于治疗神经系统疾病的化合物。本发明的化合物可以单独或与其他药用活性剂结合使用,用于治疗或预防神经系统疾病。
-
AMINOPYRIMIDINYL COMPOUNDS申请人:Pfizer Inc.公开号:US20160052930A1公开(公告)日:2016-02-25A compound having the structure: or a pharmaceutically acceptable salt thereof, wherein X is N or CR, where R is hydrogen, deuterium, C 1 -C 4 alkyl, C 1 -C 4 alkoxy, C 3 -C 6 cycloalkyl, aryl, heteroaryl, aryl(C 1 -C 6 alkyl), CN, amino, alkylamino, dialkylamino, CF 3 , or hydroxyl; A is selected from the group consisting of a bond, C═O, —SO 2 —, —(C═O)NR 0 —, and —(CR a R b ) q —, where R 0 is H or C 1 -C 4 alkyl, and R a and R b are independently hydrogen, deuterium, C 1 -C 6 alkyl, C 3 -C 6 cycloalkyl, aryl, aryl(C 1 -C 6 alkyl), heteroaryl, (C 1 -C 6 alkyl)heteroaryl, etc.; A′ is selected from the group consisting of a bond, C═O, —SO 2 —, —(C═O)NR 0 ′, —NR 0 ′(C═O)—, and —(CR a ′R b ′) q —, where R 0 ′ is H or C 1 -C 4 alkyl, and R a ′ and R b ′ are independently hydrogen, deuterium, C 1 -C 6 alkyl, C 3 -C 6 cycloalkyl, aryl, aryl(C 1 -C 6 alkyl), heteroaryl, (C 1 -C 6 alkyl)heteroaryl, heteroaryl(C 1 -C 6 alkyl), and heterocyclic(C 1 -C 6 alkyl); Z is —(CH 2 ) h — or a bond, where one or more methylene units are optionally substituted by one or more C 1 -C 3 alkyl, CN, OH, methoxy, or halo, and where said alkyl may be substituted by one or more fluorine atoms; R 1 and R 1 ′ are independently selected from the group consisting of hydrogen, deuterium, C 1 -C 4 alkyl, C 3 -C 6 cycloalkyl, aryl, heteroaryl, aryl(C 1 -C 6 alkyl), CN, etc., wherein said alkyl, aryl, cycloalkyl, heterocyclic, or heteroaryl is further optionally substituted with one or more substituents selected from the group consisting of C 1 -C 6 alkyl, halo, CN, C 1 -C 4 alkylamino, C 3 -C 6 cycloalkyl, etc.; R 2 is selected from the group consisting of hydrogen, deuterium, C 1 -C 6 alkyl, C 3 -C 6 cycloalkyl, halo, and cyano, where said alkyl may be substituted by one or more fluorine atoms; R 3 is selected from the group consisting of hydrogen, deuterium, and amino; R 4 is monocyclic or bicyclic aryl or monocyclic or bicyclic heteroaryl wherein said aryl or heteroaryl is optionally substituted with one or more substituents selected from the group consisting of C 1 -C 6 alkyl, heterocycloalkyl, halo, C 3 -C 6 cycloalkyl, etc., where said alkyl, cycloalkyl, alkoxy, or heterocycloalkyl may be substituted by one or more C 1 -C 6 alkyl, halo, CN, OH, alkoxy, amino, —CO 2 H, —(CO)NH 2 , —(CO)NH(C 1 -C 6 alkyl), or —(CO)N(C 1 -C 6 alkyl) 2 , and where said alkyl may be further substituted by one or more fluorine atoms; R 5 is independently selected from the group consisting of hydrogen, C 1 -C 6 alkyl, C 1 -C 6 alkoxy, and hydroxyl; h is 1, 2 or 3; j and k are independently 0, 1, 2, or 3; m and n are independently 0, 1 or 2; and, q is 0, 1 or 2. Also provided are methods of treatment as Janus Kinase inhibitors and pharmaceutical compositions containing the compounds of the invention and combinations with other therapeutic agents.一种具有以下结构的化合物:或其药学上可接受的盐,其中X为N或CR,其中R为氢、氘、C1-C4烷基、C1-C4烷氧基、C3-C6环烷基、芳基、杂芳基、芳基(C1-C6烷基)、CN、氨基、烷基氨基、二烷基氨基、CF3或羟基;A从以下群组中选择,即键,C═O,—SO2—,—(C═O)NR0—和—(CRaRb)q—,其中R0为H或C1-C4烷基,Ra和Rb独立地为氢、氘、C1-C6烷基、C3-C6环烷基、芳基、芳基(C1-C6烷基)、杂芳基,(C1-C6烷基)杂芳基等;A'从以下群组中选择,即键,C═O,—SO2—,—(C═O)NR0',—NR0'(C═O)—和—(CRa'Rb')q—,其中R0'为H或C1-C4烷基,Ra'和Rb'独立地为氢、氘、C1-C6烷基、C3-C6环烷基、芳基、芳基(C1-C6烷基)、杂芳基,(C1-C6烷基)杂芳基,杂芳基(C1-C6烷基)和杂环(C1-C6烷基);Z为—(CH2)h—或键,其中一个或多个亚甲基单元可以选择地被一个或多个C1-C3烷基、CN、OH、甲氧基或卤素取代,所述烷基可以被一个或多个氟原子取代;R1和R1'独立地从氢、氘、C1-C4烷基、C3-C6环烷基、芳基、杂芳基、芳基(C1-C6烷基)、CN等群组中选择,其中所述烷基、芳基、环烷基、杂环基或杂芳基可以进一步选择地被一个或多个来自C1-C6烷基、卤素、CN、C1-C4烷基氨基、C3-C6环烷基等群组的取代基取代;R2从氢、氘、C1-C6烷基、C3-C6环烷基、卤素和氰基等群组中选择,其中所述烷基可以被一个或多个氟原子取代;R3从氢、氘和氨基等群组中选择;R4为单环或双环芳基或单环或双环杂芳基,其中所述芳基或杂芳基可以选择地被一个或多个来自C1-C6烷基、杂环烷基、卤素、C3-C6环烷基等群组的取代基取代,其中所述烷基、环烷基、烷氧基或杂环烷基可以被一个或多个C1-C6烷基、卤素、CN、OH、烷氧基、氨基、—CO2H、—(CO)NH2、—(CO)NH(C1-C6烷基)或—(CO)N(C1-C6烷基)2取代,其中所述烷基可以进一步被一个或多个氟原子取代;R5独立地从氢、C1-C6烷基、C1-C6烷氧基和羟基等群组中选择;h为1、2或3;j和k可独立地为0、1、2或3;m和n可独立地为0、1或2;q为0、1或2。还提供了作为Janus激酶抑制剂的治疗方法和包含本发明化合物的药物组合物以及与其他治疗剂的组合。
-
Potent and selective inhibitors of Helicobacter pylori glutamate racemase (MurI): Pyridodiazepine amines作者:Bolin Geng、Gregory Basarab、Janelle Comita-Prevoir、Madhusudhan Gowravaram、Pamela Hill、Andrew Kiely、James Loch、Lawrence MacPherson、Marshall Morningstar、George Mullen、Ekundayo Osimboni、Alexander Satz、Charles Eyermann、Tomas LundqvistDOI:10.1016/j.bmcl.2008.11.113日期:2009.2An SAR study of an HTS screening hit generated a series of pyridodiazepine amines as potent inhibitors of Helicobacter pylori glutamate racemase (MurI) showing highly selective anti-H. pylori activity, marked improved solubility, and reduced plasma protein binding. X-ray co-crystal E–I structures were obtained. These uncompetitive inhibitors bind at the MurI dimer interface.
-
The Chemistry of Pseudomonic Acid. Part 14. Synthesis and In Vivo Biological Activity of Heterocyclyl Substituted Oxazole Derivatives.作者:N. J. P. BROOM、J. S. ELDER、P. C. T. HANNAN、J. E. PONS、P. J. O''HANLON、G. WALKER、J. WILSON、P. WOODALLDOI:10.7164/antibiotics.48.1336日期:——heterocyclyl substituted oxazole. Derivatives in which the heterocycle was thiophene, furan, pyridine, or isoxazole showed good antibacterial potency and were further evaluated in vivo. Both pharmacokinetic parameters and oral activity against an experimental intraperitoneal sepsis were superior to results obtained from previously described pseudomonic acid A derivatives.
-
Nitrogen-Walk Approach to Explore Bioisosteric Replacements in a Series of Potent A<sub>2B</sub> Adenosine Receptor Antagonists作者:Ana Mallo-Abreu、Rubén Prieto-Díaz、Willem Jespers、Jhonny Azuaje、Maria Majellaro、Carmen Velando、Xerardo García-Mera、Olga Caamaño、José Brea、María I. Loza、Hugo Gutiérrez-de-Terán、Eddy SoteloDOI:10.1021/acs.jmedchem.0c00564日期:2020.7.23thiophene cores in a series of potent A2BAR antagonists has been carried out using the nitrogen-walk approach. A collection of 42 novel alkyl 4-substituted-2-methyl-1,4-dihydrobenzo[4,5]imidazo[1,2-a]pyrimidine-3-carboxylates, which contain 18 different pentagonal heterocyclic frameworks at position 4, was synthesized and evaluated. This study enabled the identification of new ligands that combine使用氮游走法已经对一系列有效的A 2B AR拮抗剂中的呋喃和噻吩核的生物立体替代物进行了系统的研究。收集了42种新颖的4-取代-2-甲基-1,4-二氢苯并[4,5]咪唑并[1,2 - a ]嘧啶-3-羧酸烷基酯,它们在4位含有18个不同的五角杂环骨架。综合和评估。这项研究使得能够鉴定结合了显着亲和力(K i<30 nM)和精湛的选择性。基于受体驱动的对接模型并包括系统的自由能扰动(FEP)研究,通过分子建模研究证实了所确定的构效关系(SAR)趋势。在优化配体中对CYP3A4和CYP2D6抑制活性的初步评估分别显示弱和可忽略的活性。验证了h A 2B AR与最有吸引力的新型拮抗剂(S)-18g(K i = 3.66 nM)的eutomer之间的立体定向相互作用。
表征谱图
-
氢谱1HNMR
-
质谱MS
-
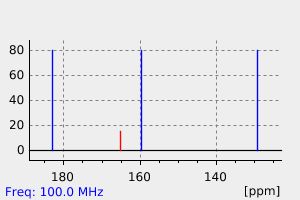
碳谱13CNMR
-
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息
同类化合物
(反式)-4-壬烯醛
(s)-2,3-二羟基丙酸甲酯
([1-(甲氧基甲基)-1H-1,2,4-三唑-5-基](苯基)甲酮)
(Z)-4-辛烯醛
(S)-氨基甲酸酯β-D-O-葡糖醛酸
(S)-3-(((2,2-二氟-1-羟基-7-(甲基磺酰基)-2,3-二氢-1H-茚满-4-基)氧基)-5-氟苄腈
(R)-氨基甲酸酯β-D-O-葡糖醛酸
(5,5-二甲基-2-(哌啶-2-基)环己烷-1,3-二酮)
(2,5-二氟苯基)-4-哌啶基-甲酮
龙胆苦苷
龙胆二糖甲乙酮氰醇(P)
龙胆二糖丙酮氰醇(P)
龙胆三糖
龙涎酮
齐罗硅酮
齐留通beta-D-葡糖苷酸
鼠李糖
黑芥子苷单钾盐
黑海棉酸钠盐
黑木金合欢素
黑曲霉三糖
黑介子苷
黄尿酸8-O-葡糖苷
麻西那霉素II
麦迪霉素
麦芽糖脎
麦芽糖基海藻糖
麦芽糖1-磷酸酯
麦芽糖
麦芽四糖醇
麦芽四糖
麦芽十糖
麦芽六糖
麦芽五糖水合物
麦芽五糖
麦芽五糖
麦芽五糖
麦芽三糖醇
麦芽三糖
麦芽三糖
麦芽三塘水合
麦芽七糖水合物
麦芽七糖
麦法朵
麦可酚酸-酰基-Β-D-葡糖苷酸
麦利查咪
麝香酮
鹤草酚
鸢尾酚酮 3-C-beta-D-吡喃葡萄糖苷
鸡矢藤苷