(+)-T-muurolol
中文名称
——
中文别名
——
英文名称
(+)-T-muurolol
英文别名
ent-T-muurolol;(+)-torreyol;α-muurolol;δ-cadinol;(+)-tau-Muurolol;(1R,4R,4aS,8aR)-1,6-dimethyl-4-propan-2-yl-3,4,4a,7,8,8a-hexahydro-2H-naphthalen-1-ol
CAS
——
化学式
C15H26O
mdl
——
分子量
222.371
InChiKey
LHYHMMRYTDARSZ-KBUPBQIOSA-N
BEILSTEIN
——
EINECS
——
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
计算性质
-
辛醇/水分配系数(LogP):3.3
-
重原子数:16
-
可旋转键数:1
-
环数:2.0
-
sp3杂化的碳原子比例:0.87
-
拓扑面积:20.2
-
氢给体数:1
-
氢受体数:1
反应信息
-
作为反应物:描述:(+)-T-muurolol 在 cytochrome P450 monooxygenase CYP267B1 from Sorangium cellulosum 作用下, 生成 (1S,4S,6R,7R,10R)-4β,7α-dihydroxy-(+)-α-muurolene 、 、 (1S,6R,7R,10R)-7α-hydroxy-4-oxo-(+)-α-muurolene参考文献:名称:研究萜烯的细胞色素P450氧化的同位素标记策略。摘要:将来自Sorangium cellulosum的细胞色素P450单加氧酶CYP267B1用于倍半萜烯醇T-muurolol和isodauc-8-en-11-ol的酶促氧化。各种同位素标记的香叶基和法呢基二磷酸酯用于微量反应中的产物鉴定,确定未知化合物的绝对构型,遵循细胞色素P450催化的羟基化步骤的立体化学过程,并研究动力学同位素效应。总的来说,这项研究表明,同位素标记的萜烯前体对于跟踪细胞色素P450依赖的萜烯氧化非常有用。DOI:10.1002/cbic.201800215
-
作为产物:描述:farnesyl pyrophosphate 在 (+)-T-muurolol synthase from Roseiflexus castenholzii 、 碳酸氢铵 作用下, 以 aq. buffer 为溶剂, 反应 4.0h, 生成 (+)-T-muurolol参考文献:名称:倍半萜和双萜的EI-MS裂解机理摘要:通过使用每个分子的全部15或20种酶促合成的13 C 1标记的同位素异构体,研究了一种细菌倍半萜烯醇和四种二萜烃的EI-MS断裂机理。特定位置的质量偏移分析表明形成每个碎片离子的碳主链部分。HR-MS / MS分析已开发出可能的破碎机制,并进一步加强了这种破碎机制。DOI:10.1002/ejoc.201800217
文献信息
-
Lessons from 1,3-Hydride Shifts in Sesquiterpene Cyclizations作者:Jan Rinkel、Patrick Rabe、Paolina Garbeva、Jeroen S. DickschatDOI:10.1002/anie.201608042日期:2016.10.17initial 1,10‐cyclisation‐1,3‐hydride shift cascades. Enzymes with products of known absolute configuration showed a coherent stereochemical course, except for (−)‐α‐amorphene synthase, for which the obtained results are better explained by an initial 1,6‐cyclisation. The link between the absolute configuration of the product and the stereochemical course of the 1,3‐hydride shifts enabled assignment of
-
Antimalarial Properties of Simplified Kalihinol Analogues作者:Mary Elisabeth Daub、Jacques Prudhomme、Choukri Ben Mamoun、Karine G. Le Roch、Christopher D. VanderwalDOI:10.1021/acsmedchemlett.7b00013日期:2017.3.9Several kalihinol natural products, members of the broader isocyanoterpene family of antimalarial agents, are potent inhibitors of Plasmodium falciparum, the agent of the most severe form of human malaria. Our previous total synthesis of kalihinol B provided a blueprint to generate many analogues within this family, some as complex as the natural product and some much simplified and easier to access. Each analogue was tested for blood-stage antimalarial activity using both drug-sensitive and -resistant P. falciparum strains. Many considerably simpler analogues of the kalihinols retained potent activity, as did a compound with a different decalin scaffold made in only three steps from sclareolide. Finally, one representative compound showed reasonable stability toward microsomal metabolism, suggesting that the isonitrile functional group that is critical for activity is not an inherent liability in these compounds.
-
Genome Mining in Streptomyces clavuligerus: Expression and Biochemical Characterization of Two New Cryptic Sesquiterpene Synthases作者:Yunfeng Hu、Wayne K.W. Chou、Russell Hopson、David E. CaneDOI:10.1016/j.chembiol.2010.11.008日期:2011.1Two presumptive terpene synthases of unknown biochemical function encoded by the sscg_02150 and sscg_03688 genes of Streptomyces clavuligerus ATCC 27074 were individually expressed in Escherichia coli as N-terminal-His(6)-tag proteins, using codon-optimized synthetic genes. Incubation of recombinant SSCG_02150 with farnesyl diphosphate (1, FPP) gave (-)-delta-cadinene (2) while recombinant SSCG_03688 converted FPP to (+)-T-muurolol (3). Individual incubations of (-)-delta-cadinene synthase with [1,1-H-2(2)]FPP (1a), (1S)-[1-H-2]-FPP (1b), and (1R)-[1-H-2]-FPP (1c) and NMR analysis of the resulting samples of deuterated (-)-delta-cadinene supported a cyclization mechanism involving the intermediacy of nerolidyl diphosphate (4) leading to a helminthogermacradienyl cation 5. Following a 1,3-hydride shift of the original H-1(si) of FPP, cyclization and deprotonation will give (-)-delta-cadinene. Similar incubations with recombinant SSCG_03688 supported an analogous mechanism for the formation of (+)-T-muurolol (3), also involving a 1,3-hydride shift of the original H-1(si) of FPP.
-
Bowden, Bruce F.; Coll, John C.; Willis, Richard H., Australian Journal of Chemistry, 1986, vol. 39, # 10, p. 1717 - 1722作者:Bowden, Bruce F.、Coll, John C.、Willis, Richard H.DOI:——日期:——
表征谱图
-
氢谱1HNMR
-
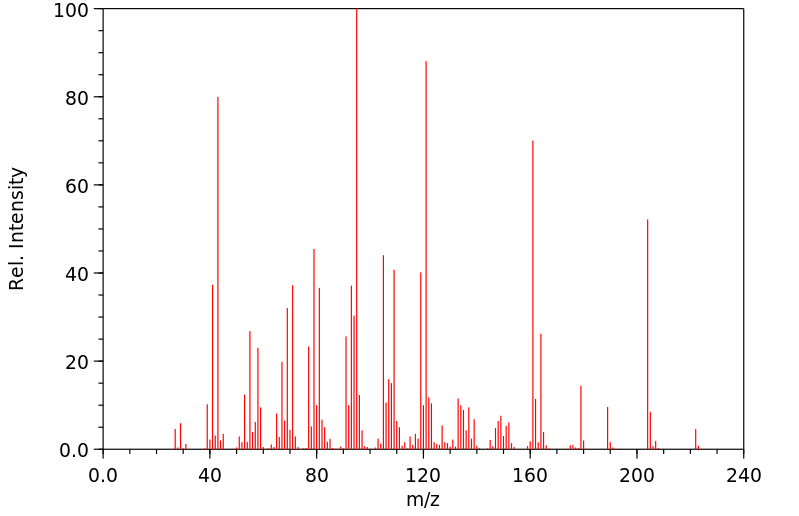
质谱MS
-
碳谱13CNMR
-
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息
同类化合物
(5β,6α,8α,10α,13α)-6-羟基-15-氧代黄-9(11),16-二烯-18-油酸
(3S,3aR,8aR)-3,8a-二羟基-5-异丙基-3,8-二甲基-2,3,3a,4,5,8a-六氢-1H-天青-6-酮
(2Z)-2-(羟甲基)丁-2-烯酸乙酯
(2S,4aR,6aR,7R,9S,10aS,10bR)-甲基9-(苯甲酰氧基)-2-(呋喃-3-基)-十二烷基-6a,10b-二甲基-4,10-dioxo-1H-苯并[f]异亚甲基-7-羧酸盐
(1aR,4E,7aS,8R,10aS,10bS)-8-[((二甲基氨基)甲基]-2,3,6,7,7a,8,10a,10b-八氢-1a,5-二甲基-氧杂壬酸[9,10]环癸[1,2-b]呋喃-9(1aH)-酮
(+)顺式,反式-脱落酸-d6
龙舌兰皂苷乙酯
龙脑香醇酮
龙脑烯醛
龙脑7-O-[Β-D-呋喃芹菜糖基-(1→6)]-Β-D-吡喃葡萄糖苷
龙牙楤木皂甙VII
龙吉甙元
齿孔醇
齐墩果醛
齐墩果酸苄酯
齐墩果酸甲酯
齐墩果酸溴乙酯
齐墩果酸二甲胺基乙酯
齐墩果酸乙酯
齐墩果酸3-O-alpha-L-吡喃鼠李糖基(1-3)-beta-D-吡喃木糖基(1-3)-alpha-L-吡喃鼠李糖基(1-2)-alpha-L-阿拉伯糖吡喃糖苷
齐墩果酸 beta-D-葡萄糖酯
齐墩果酸 beta-D-吡喃葡萄糖基酯
齐墩果酸 3-乙酸酯
齐墩果酸 3-O-beta-D-葡吡喃糖基 (1→2)-alpha-L-吡喃阿拉伯糖苷
齐墩果酸
齐墩果-12-烯-3b,6b-二醇
齐墩果-12-烯-3,24-二醇
齐墩果-12-烯-3,21,23-三醇,(3b,4b,21a)-(9CI)
齐墩果-12-烯-3,21,23-三醇,(3b,4b,21a)-(9CI)
齐墩果-12-烯-3,11-二酮
齐墩果-12-烯-2α,3β,28-三醇
齐墩果-12-烯-29-酸,3,22-二羟基-11-羰基-,g-内酯,(3b,20b,22b)-
齐墩果-12-烯-28-酸,3-[(6-脱氧-4-O-b-D-吡喃木糖基-a-L-吡喃鼠李糖基)氧代]-,(3b)-(9CI)
齐墩果-12-烯-28-酸,3,7-二羰基-(9CI)
齐墩果-12-烯-28-酸,3,21,29-三羟基-,g-内酯,(3b,20b,21b)-(9CI)
鼠特灵
鼠尾草酸醌
鼠尾草酸
鼠尾草酚酮
鼠尾草苦内脂
黑蚁素
黑蔓醇酯B
黑蔓醇酯A
黑蔓酮酯D
黑海常春藤皂苷A1
黑檀醇
黑果茜草萜 B
黑五味子酸
黏黴酮
黏帚霉酸