炔丙基三甲基硅烷 | 13361-64-3
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
物化性质
-
熔点:148-151 °C(Solv: ethyl ether (60-29-7))
-
沸点:91-93 °C (lit.)
-
密度:0.753 g/mL at 25 °C (lit.)
-
闪点:13 °F
-
溶解度:溶胶醚、THF、CH2Cl2。
-
保留指数:676
-
稳定性/保质期:
在常温、常压和空气中比较稳定。
计算性质
-
辛醇/水分配系数(LogP):2.44
-
重原子数:7
-
可旋转键数:1
-
环数:0.0
-
sp3杂化的碳原子比例:0.666
-
拓扑面积:0
-
氢给体数:0
-
氢受体数:0
安全信息
-
危险等级:3.1
-
危险品标志:F,Xi
-
安全说明:S16,S26,S36
-
危险类别码:R36/37/38,R11
-
WGK Germany:3
-
海关编码:2931900090
-
危险品运输编号:UN 1993
-
危险类别:3.1
-
包装等级:II
-
危险标志:GHS02,GHS07
-
危险性描述:H225,H315,H319,H335
-
危险性防范说明:P210,P261,P305 + P351 + P338
-
储存条件:建议低温避光保存。
SDS
: 炔丙基三甲基硅烷
产品名称
1.2 鉴别的其他方法
无数据资料
1.3 有关的确定了的物质或混合物的用途和建议不适合的用途
仅供科研用途,不作为药物、家庭备用药或其它用途。
模块 2. 危险性概述
2.1 GHS分类
易燃液体 (类别2)
皮肤刺激 (类别2)
眼刺激 (类别2A)
特异性靶器官系统毒性(一次接触) (类别3)
2.2 GHS 标记要素,包括预防性的陈述
象形图
警示词 危险
危险申明
H225 高度易燃液体和蒸气
H315 造成皮肤刺激。
H319 造成严重眼刺激。
H335 可能引起呼吸道刺激。
警告申明
预防
P210 远离热源、火花、明火和热表面。- 禁止吸烟。
P233 保持容器密闭。
P240 容器和接收设备接地/等势连接。
P241 使用防爆的电气/ 通风/ 照明 设备。
P242 只能使用不产生火花的工具。
P243 采取防止静电放电的措施。
P261 避免吸入粉尘/烟/气体/烟雾/蒸气/喷雾.
P264 操作后彻底清洁皮肤。
P271 只能在室外或通风良好之处使用。
P280 戴防护手套/穿防护服/戴护目镜/戴面罩.
措施
P303 + P361 + P353 如皮肤(或头发)沾染:立即去除/ 脱掉所有沾染的衣服。用水清洗皮肤/
淋浴。
P304 + P340 如吸入,将患者移至新鲜空气处并保持呼吸顺畅的姿势休息.
P305 + P351 + P338 如与眼睛接触,用水缓慢温和地冲洗几分钟。如戴隐形眼镜并可方便地取
出,取出隐形眼镜,然后继续冲洗.
P312 如感觉不适,呼救中毒控制中心或医生.
P321 具体治疗(见本标签上提供的急救指导)。
P332 + P313 如发生皮肤刺激:求医/ 就诊。
P337 + P313 如仍觉眼睛刺激:求医/就诊。 如仍觉眼睛刺激:求医/就诊.
P362 脱掉沾染的衣服,清洗后方可重新使用。
P370 + P378 火灾时: 用干的砂子,干的化学品或耐醇性的泡沫来灭火。
储存
P403 + P233 存放于通风良的地方。 保持容器密闭。
P403 + P235 存放在通风良好的地方。保持低温。
P405 存放处须加锁。
处理
P501 将内容物/ 容器处理到得到批准的废物处理厂。
2.3 其它危害物 - 无
模块 3. 成分/组成信息
3.1 物 质
: C6H12Si
分子式
: 112.24 g/mol
分子量
组分 浓度或浓度范围
Trimethyl-2-propynylsiLAne
-
CAS 号 13361-64-3
EC-编号 236-427-6
模块 4. 急救措施
4.1 必要的急救措施描述
一般的建议
请教医生。 出示此安全技术说明书给到现场的医生看。
吸入
如果吸入,请将患者移到新鲜空气处。 如果停止了呼吸,给于人工呼吸。 请教医生。
皮肤接触
用肥皂和大量的水冲洗。 请教医生。
眼睛接触
用大量水彻底冲洗至少15分钟并请教医生。
食入
禁止催吐。 切勿给失去知觉者从嘴里喂食任何东西。 用水漱口。 请教医生。
4.2 主要症状和影响,急性和迟发效应
据我们所知,此化学,物理和毒性性质尚未经完整的研究。
4.3 及时的医疗处理和所需的特殊处理的说明和指示
无数据资料
模块 5. 消防措施
5.1 灭火介质
灭火方法及灭火剂
小(起始)火时,使用媒介物如“乙醇”泡沫、干化学品或二氧化碳。大火时,尽可能使用水灭火。使用大量(
洪水般的)水以喷雾状应用;水柱可能是无效的。用大量水降温所有受影响的容器。
5.2 源于此物质或混合物的特别的危害
碳氧化物, 二氧化硅
5.3 给消防员的建议
如必要的话,戴自给式呼吸器去救火。
5.4 进一步信息
水喷雾可用来冷却未打开的容器。
模块 6. 泄露应急处理
6.1 人员的预防,防护设备和紧急处理程序
使用个人防护设备。 防止吸入蒸汽、气雾或气体。 保证充分的通风。 移去所有火源。
将人员撤离到安全区域。 防范蒸汽积累达到可爆炸的浓度,蒸汽能在低洼处积聚。
6.2 环境保护措施
在确保安全的前提下,采取措施防止进一步的泄漏或溢出。 不要让产物进入下水道。
6.3 抑制和清除溢出物的方法和材料
用防电真空清洁器或湿的刷子将溢出物收集起来并放置到容器中去,根据当地规定处理(见第13部分)。
6.4 参考其他部分
丢弃处理请参阅第13节。
模块 7. 操作处置与储存
7.1 安全操作的注意事项
避免接触皮肤和眼睛。 防止吸入蒸汽和烟雾。
切勿靠近火源。-严禁烟火。采取措施防止静电积聚。
7.2 安全储存的条件,包括任何不兼容性
贮存在阴凉处。 容器保持紧闭,储存在干燥通风处。
打开了的容器必须仔细重新封口并保持竖放位置以防止泄漏。
建议的贮存温度: -20 °C
7.3 特定用途
无数据资料
模块 8. 接触控制和个体防护
8.1 容许浓度
最高容许浓度
没有已知的国家规定的暴露极限。
8.2 暴露控制
适当的技术控制
按照良好工业和安全规范操作。 休息前和工作结束时洗手。
个体防护设备
眼/面保护
面罩與安全眼鏡请使用经官方标准如NIOSH (美国) 或 EN 166(欧盟) 检测与批准的设备防护眼部。
皮肤保护
戴手套取 手套在使用前必须受检查。
请使用合适的方法脱除手套(不要接触手套外部表面),避免任何皮肤部位接触此产品.
使用后请将被污染过的手套根据相关法律法规和有效的实验室规章程序谨慎处理. 请清洗并吹干双手
所选择的保护手套必须符合EU的89/686/EEC规定和从它衍生出来的EN 376标准。
身体保护
防渗透的衣服, 阻燃防静电防护服,
防护设备的类型必须根据特定工作场所中的危险物的浓度和含量来选择。
呼吸系统防护
如危险性评测显示需要使用空气净化的防毒面具,请使用全面罩式多功能防毒面具(US)或ABEK型
(EN
14387)防毒面具筒作为工程控制的候补。如果防毒面具是保护的唯一方式,则使用全面罩式送风防
毒面具。 呼吸器使用经过测试并通过政府标准如NIOSH(US)或CEN(EU)的呼吸器和零件。
模块 9. 理化特性
9.1 基本的理化特性的信息
a) 外观与性状
形状: 透明, 液体
颜色: 无色
b) 气味
无数据资料
c) 气味阈值
无数据资料
d) pH值
无数据资料
e) 熔点/凝固点
无数据资料
f) 起始沸点和沸程
91 - 93 °C
g) 闪点
-5 °C - 闭杯
h) 蒸发速率
无数据资料
i) 易燃性(固体,气体)
无数据资料
j) 高的/低的燃烧性或爆炸性限度 无数据资料
k) 蒸汽压
无数据资料
l) 蒸汽密度
无数据资料
m) 相对密度
0.753 g/mL 在 25 °C
n) 水溶性
无数据资料
o) n-辛醇/水分配系数
无数据资料
p) 自燃温度
无数据资料
q) 分解温度
无数据资料
r) 粘度
无数据资料
模块 10. 稳定性和反应活性
10.1 反应性
无数据资料
10.2 稳定性
无数据资料
含有下列稳定剂:
BHT (0.05 %)
10.3 危险反应的可能性
无数据资料
10.4 应避免的条件
热,火焰和火花。 极端的温度和直接日光。
10.5 不兼容的材料
强氧化剂
10.6 危险的分解产物
其它分解产物 - 无数据资料
模块 11. 毒理学资料
11.1 毒理学影响的信息
急性毒性
无数据资料
皮肤刺激或腐蚀
无数据资料
眼睛刺激或腐蚀
无数据资料
呼吸道或皮肤过敏
无数据资料
生殖细胞突变性
无数据资料
致癌性
IARC:
此产品中没有大于或等于 0。1%含量的组分被 IARC鉴别为可能的或肯定的人类致癌物。
生殖毒性
无数据资料
特异性靶器官系统毒性(一次接触)
吸入 - 可能引起呼吸道刺激。
特异性靶器官系统毒性(反复接触)
无数据资料
吸入危险
无数据资料
潜在的健康影响
吸入 吸入可能有害。 引起呼吸道刺激。
摄入 如服入是有害的。
皮肤 如果通过皮肤吸收可能是有害的。 造成皮肤刺激。
眼睛 造成严重眼刺激。
接触后的征兆和症状
据我们所知,此化学,物理和毒性性质尚未经完整的研究。
附加说明
化学物质毒性作用登记: 无数据资料
模块 12. 生态学资料
12.1 生态毒性
无数据资料
12.2 持久存留性和降解性
无数据资料
12.3 潜在的生物蓄积性
无数据资料
12.4 土壤中的迁移性
无数据资料
12.5 PBT 和 vPvB的结果评价
无数据资料
12.6 其它不利的影响
无数据资料
模块 13. 废弃处置
13.1 废物处理方法
产品
在装备有加力燃烧室和洗刷设备的化学焚烧炉内燃烧处理,特别在点燃的时候要注意,因为此物质是高度易燃
性物质 将剩余的和未回收的溶液交给处理公司。 联系专业的拥有废弃物处理执照的机构来处理此物质。
受污染的容器和包装
作为未用过的产品弃置。
模块 14. 运输信息
14.1 联合国危险货物编号
欧洲陆运危规: 1993 国际海运危规: 1993 国际空运危规: 1993
14.2 联合国(UN)规定的名称
欧洲陆运危规: FLAMMABLE LIQUID, N.O.S. (Trimethyl-2-propynylsiLAne)
国际海运危规: FLAMMABLE LIQUID, N.O.S. (Trimethyl-2-propynylsiLAne)
国际空运危规: FLAMMAble liquid, n.o.s. (Trimethyl-2-propynylsiLAne)
14.3 运输危险类别
欧洲陆运危规: 3 国际海运危规: 3 国际空运危规: 3
14.4 包裹组
欧洲陆运危规: II 国际海运危规: II 国际空运危规: II
14.5 环境危险
欧洲陆运危规: 否 国际海运危规 海运污染物: 否 国际空运危规: 否
14.6 对使用者的特别提醒
无数据资料
模块 15 - 法规信息
N/A
模块16 - 其他信息
N/A
制备方法与用途
用3-炔丙基溴化镁与TMSCl反应来制备。
合成制备方法同样地,用3-炔丙基溴化镁与TMSCl反应来制备。[1]
用途简介炔丙基三甲基硅烷在有机合成中常被用作烷基化试剂,以丙炔基或丙二烯基的形式引入三个碳原子到底物分子中。该化合物的反应性主要集中在分子两端。当炔基一端的活性氢与金属置换后生成的金属炔化物与其他烷基金属类似,可以参与各种类型的亲核反应。例如:3-炔丙基溴化镁与丁基锂交换生成3-(三甲基硅基)丙炔锂,然后与醛酮发生加成反应生成相应的醇[2, 3];与环丙烷作用生成开环产物(式1)[4]等。最近的研究显示,在Zn(OTf)₂存在下,炔丙基三甲基硅烷随即生成3-(三甲基硅基)丙炔锌,然后在温和条件下与酰化亚铵盐发生高产率的加成反应。这一过程不仅形成新的C-C键,还生成含氮的炔烃化合物(式2)[5]。当在催化剂存在下,分子另一端的三甲基硅可以作为反应位点,在路易斯酸如BF₃·Et₂O、ZnI₂等的作用下,O,O-半缩醛或N,N-半缩醛衍生物中的羟基、醚基或者氨基可被炔丙基取代,主要生成丙二烯的衍生物(式3, 式4)[6-9]。另外,简单路易斯酸催化剂可以使炔丙基三甲基硅烷直接对叔醇和叔卤代烃进行烷基化反应,在分子中引入炔丙基或丙二烯基。而金属InCl₃作用下,该试剂也可以直接对仲醇进行烷基化反应,生成丙二烯的衍生物(式5)[11, 12]。
用途炔丙基三甲基硅烷在有机合成中常被用作烷基化试剂,在底物分子中以丙炔基或丙二烯基的形式引入三个碳原子。该化合物的反应性主要集中在分子两端。当炔基一端的活性氢与金属置换后生成的金属炔化物与其他烷基金属类似,可以参与各种类型的亲核反应。例如:3-炔丙基溴化镁与丁基锂交换生成3-(三甲基硅基)丙炔锂,然后与醛酮发生加成反应生成相应的醇[2, 3];与环丙烷作用生成开环产物(式1)[4]等。最近的研究显示,在Zn(OTf)₂存在下,炔丙基三甲基硅烷随即生成3-(三甲基硅基)丙炔锌,然后在温和条件下与酰化亚铵盐发生高产率的加成反应。这一过程不仅形成新的C-C键,还生成含氮的炔烃化合物(式2)[5]。
当在催化剂存在下,分子另一端的三甲基硅可以作为反应位点,在路易斯酸如BF₃·Et₂O、ZnI₂等的作用下,O,O-半缩醛或N,N-半缩醛衍生物中的羟基、醚基或者氨基可被炔丙基取代,主要生成丙二烯的衍生物(式3, 式4)[6-9]。此外,在简单路易斯酸催化剂作用下,该试剂可以直接对叔醇和叔卤代烃进行烷基化反应,在分子中引入炔丙基或丙二烯基。而在金属InCl₃的作用下,该试剂也可以直接对仲醇进行烷基化反应,生成丙二烯的衍生物(式5)[11, 12]。
上下游信息
-
下游产品
中文名称 英文名称 CAS号 化学式 分子量 —— but-2-ynyltrimethylsilane 18825-29-1 C7H14Si 126.274 —— (3-iodoprop-2-yn-1-yl)trimethylsilane 138081-27-3 C6H11ISi 238.143 —— 1,4-bis(trimethylsilyl)-2-butyne 21752-78-3 C10H22Si2 198.456 —— (4-Chloro-but-2-ynyl)-trimethyl-silane 108460-02-2 C7H13ClSi 160.719 —— 4-(trimethylsilyl)but-2-yn-1-ol 90933-84-9 C7H14OSi 142.273 4-溴丁-2-炔基(三甲基)硅烷 1-bromo-4-trimethylsilyl-but-2-yne 121823-55-0 C7H13BrSi 205.17 —— 1,3-bis(trimethylsilyl)propyne 21752-80-7 C9H20Si2 184.429 —— Bis-trimethylsilylmethyl-diacetylen 21752-84-1 C12H22Si2 222.478
反应信息
-
作为反应物:描述:参考文献:名称:Stannyldienes,有机合成的新工具。准备和反应摘要:三丁基锡烷基-1,3-二烯可以被认为是共轭二烯阴离子的合成等价物。据报道从炔丙基三甲基戊烷开始制备不同取代的2-和3-三烷基锡烷基-1,3-二烯。可以通过(三甲基甲硅烷基)炔丙基醇的加氢甲锡烷基化或(三甲基甲硅烷基)炔丙基酮的甲锡醇杯化来控制二苯乙烯骨架上的苯乙烯基部分的位置。将如此获得的苯乙烯亚胺进行二烯Alder反应,并通过C-Sn将相应的环加合物官能化。键。甲炔还适合通过以下方法进行二烯结构的区域控制转移:a)锡-锂交换,并与醛进一步反应,生成共轭二烯醇;b)在钯催化剂的存在下与酰氯偶联,得到共轭二烯酮;c)AlCl 3,促进与酰氯的反应,生成烯丙基酮。DOI:10.1016/0040-4020(89)80022-5
-
作为产物:参考文献:名称:PORNET, J.;DAMOUR, D.;MIGINIAC, L., TETRAHEDRON, 1986, 42, N 7, 2017-2024摘要:DOI:
-
作为试剂:描述:参考文献:名称:Synthesis and biological evaluation of extraordinarily potent C-10 carba artemisinin dimers against P. falciparum malaria parasites and HL-60 cancer cells摘要:A series of artemisinin dimers incorporating a metabolically stable C-10 carba-linkage have been prepared, several of which show remarkable in vitro antimalarial activity ( as low as 30 pM) versus Plasmodium falciparum and in vitro anticancer activity in the micromolar to nanomolar range versus HL-60 cell lines. (c) 2009 Elsevier Ltd. All rights reserved.DOI:10.1016/j.bmc.2008.12.017
文献信息
-
Access to Perfluoroalkyl-Substituted Enones and Indolin-2-ones via Multicomponent Pd-Catalyzed Carbonylative Reactions作者:Hongfei Yin、Troels SkrydstrupDOI:10.1021/acs.joc.7b00942日期:2017.6.16A simple method for accessing perfluoroalkyl-substituted enones is described applying a four-component palladium-catalyzed carbonylative coupling of aryl boronic acids together with terminal alkynes and perfluoroalkyl iodides in the presence of carbon monoxide. A wide range of highly functionalized enones can thus be prepared in a single operation in good yields. With 2-aminophenylalkynes, an intramolecular
-
Robust perfluorophenylboronic acid-catalyzed stereoselective synthesis of 2,3-unsaturated <i>O</i>-, <i>C</i>-, <i>N</i>- and <i>S</i>-linked glycosides作者:Madhu Babu Tatina、Xia Mengxin、Rao Peilin、Zaher M A JudehDOI:10.3762/bjoc.15.125日期:——A convenient protocol was developed for the synthesis of 2,3-unsaturated C-, O-, N- and S-linked glycosides (enosides) using 20 mol % perflurophenylboronic acid catalyst via Ferrier rearrangement. Using this protocol, D-glucals and L-rhamnals reacted with various C-, O-, N- and S-nucleophiles to give a wide range of glycosides in up to 98% yields with mainly α-anomeric selectivity. The perflurophenylboronic
-
Triazolone derivatives, use thereof, and intermediates therefor申请人:Sumitomo Chemical Company, Limited公开号:US06489487B1公开(公告)日:2002-12-03Triazolone derivatives represented by the formula wherein R1 represents optionally substituted C1-10 alkyl, A1—L1—, A1—ON═CA2, etc.; R2 represents hydrogen, C1-6 alkyl, etc.; R3 represents C1-6 alkoxy, etc.; one of T, U, and V represents CR4, another represents CH or nitrogen, and the remaining one represents CR5 or nitrogen; and W represents CR6 or nitrogen.
-
Two directional electroorganic synthesis—electrochemical oxidation and application of a C2-symmetric building block作者:Marc Zelgert、Martin Nieger、Michael Lennartz、Eberhard SteckhanDOI:10.1016/s0040-4020(02)00147-3日期:2002.3The C2-symmetric building block 1,2:5,6-di-N,O-carbonyl-1,6-diamino-3,4-O-isopropylidene-d-mannitol can be synthesized from d-mannitol in four steps using a nucleophilic substitution with cyanate and a subsequent cyclization in the final key step. The direct electrochemical oxidation of the resulting dioxazolidinone at 40 mA/cm2 in methanol at graphite electrodes with sodium benzene sulfonate as supporting
-
Azabicyclic compounds for the treatment of disease申请人:——公开号:US20030232853A1公开(公告)日:2003-12-18The invention provides compounds of Formula I: 1 wherein Azabicyclo is 2 These compounds may be in the form of pharmaceutical salts or compositions, may be in pure enantiomeric form or racemic mixtures, and are useful in pharmaceuticals in which &agr;7 is known to be involved.这项发明提供了Formula I的化合物: 其中Azabicyclo是 这些化合物可以是药用盐或组合物的形式,可以是纯对映体形式或混合物,对已知涉及α7的药物具有用处。
表征谱图
-
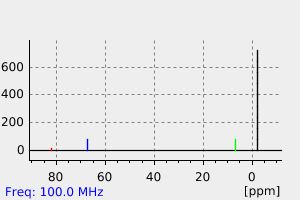
氢谱1HNMR
-
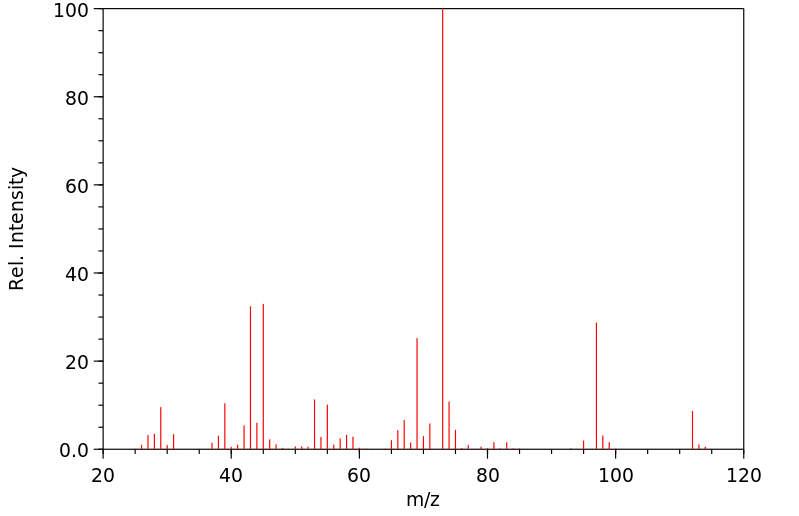
质谱MS
-
碳谱13CNMR
-
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息