乙酰乙酸异戊酯 | 2308-18-1
中文名称
乙酰乙酸异戊酯
中文别名
异戊基乙酰乙酸酯
英文名称
isoamyl acetoacetate
英文别名
3-methylbutyl 3-oxobutanoate
CAS
2308-18-1
化学式
C9H16O3
mdl
MFCD00059355
分子量
172.224
InChiKey
XHRGPLDMNNGHCX-UHFFFAOYSA-N
BEILSTEIN
——
EINECS
——
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
物化性质
-
沸点:218°C
-
密度:0,97 g/cm3
-
闪点:101°C
-
溶解度:可溶于氯仿(少许)、DMSO(少许)
-
LogP:2.13
-
物理描述:colourless liquid; ethereal, fruity, somewhat herbaceous, winey, fermented apple-like odour
-
折光率:1.426-1.433
计算性质
-
辛醇/水分配系数(LogP):1.6
-
重原子数:12
-
可旋转键数:6
-
环数:0.0
-
sp3杂化的碳原子比例:0.777
-
拓扑面积:43.4
-
氢给体数:0
-
氢受体数:3
安全信息
-
安全说明:S26,S36/37/39
-
危险类别码:R36/37/38
-
海关编码:2918300090
-
储存条件:室温且干燥
SDS
乙酰乙酸异戊酯 修改号码:5
模块 1. 化学品
产品名称: Isoamyl Acetoacetate
修改号码: 5
模块 2. 危险性概述
GHS分类
物理性危害 未分类
健康危害
皮肤腐蚀/刺激 第2级
严重损伤/刺激眼睛 2A类
环境危害 未分类
GHS标签元素
图标或危害标志
信号词 警告
危险描述 造成皮肤刺激
造成严重眼刺激
防范说明
[预防] 处理后要彻底清洗双手。
穿戴防护手套/护目镜/防护面具。
[急救措施] 眼睛接触:用水小心清洗几分钟。如果方便,易操作,摘除隐形眼镜。继续冲洗。
眼睛接触:求医/就诊
皮肤接触:用大量肥皂和水轻轻洗。
若皮肤刺激:求医/就诊。
脱掉被污染的衣物,清洗后方可重新使用。
模块 3. 成分/组成信息
单一物质/混和物 单一物质
化学名(中文名): 乙酰乙酸异戊酯
百分比: >97.0%(GC)
CAS编码: 2308-18-1
俗名: Acetoacetic Acid Isoamyl Ester , IsopeNTyl Acetoacetate
乙酰乙酸异戊酯 修改号码:5
模块 3. 成分/组成信息
分子式: C9H16O3
模块 4. 急救措施
吸入: 将受害者移到新鲜空气处,保持呼吸通畅,休息。若感不适请求医/就诊。
皮肤接触: 立即去除/脱掉所有被污染的衣物。用大量肥皂和水轻轻洗。
若皮肤刺激或发生皮疹:求医/就诊。
眼睛接触: 用水小心清洗几分钟。如果方便,易操作,摘除隐形眼镜。继续清洗。
如果眼睛刺激:求医/就诊。
食入: 若感不适,求医/就诊。漱口。
紧急救助者的防护: 救援者需要穿戴个人防护用品,比如橡胶手套和气密性护目镜。
模块 5. 消防措施
合适的灭火剂: 干粉,泡沫,二氧化碳
不适用的灭火剂: 水(有可能扩大灾情。)
特定方法: 从上风处灭火,根据周围环境选择合适的灭火方法。
非相关人员应该撤离至安全地方。
周围一旦着火:如果安全,移去可移动容器。
消防员的特殊防护用具: 灭火时,一定要穿戴个人防护用品。
模块 6. 泄漏应急处理
个人防护措施,防护用具, 使用个人防护用品。远离溢出物/泄露处并处在上风处。确保足够通风。
紧急措施: 泄露区应该用安全带等圈起来,控制非相关人员进入。
环保措施: 防止进入下水道。
控制和清洗的方法和材料: 用合适的吸收剂(如:旧布,干砂,土,锯屑)吸收泄漏物。一旦大量泄漏,筑堤控
制。附着物或收集物应该立即根据合适的法律法规废弃处置。
模块 7. 操作处置与储存
处理
技术措施: 在通风良好处进行处理。穿戴合适的防护用具。防止烟雾产生。处理后彻底清洗双手
和脸。
注意事项: 如果蒸气或浮质产生,使用通风、局部排气。
操作处置注意事项: 避免接触皮肤、眼睛和衣物。
贮存
储存条件: 保持容器密闭。存放于凉爽、阴暗处。
远离不相容的材料比如氧化剂存放。
包装材料: 依据法律。
模块 8. 接触控制和个体防护
工程控制: 尽可能安装封闭体系或局部排风系统,操作人员切勿直接接触。同时安装淋浴器和洗
眼器。
个人防护用品
呼吸系统防护: 防毒面具。依据当地和政府法规。
手部防护: 防护手套。
眼睛防护: 安全防护镜。如果情况需要,佩戴面具。
皮肤和身体防护: 防护服。如果情况需要,穿戴防护靴。
模块 9. 理化特性
外形(20°C): 液体
外观: 透明
乙酰乙酸异戊酯 修改号码:5
模块 9. 理化特性
颜色: 无色-几乎无色
气味: 无资料
pH: 无数据资料
熔点: 无资料
沸点/沸程 218 °C
闪点: 101°C
爆炸特性
爆炸下限: 无资料
爆炸上限: 无资料
密度: 0.97
溶解度:
[水] 无资料
[其他溶剂] 无资料
模块 10. 稳定性和反应性
化学稳定性: 一般情况下稳定。
危险反应的可能性: 未报道特殊反应性。
须避免接触的物质 氧化剂
危险的分解产物: 一氧化碳, 二氧化碳
模块 11. 毒理学信息
急性毒性: 无资料
对皮肤腐蚀或刺激: 无资料
对眼睛严重损害或刺激: 无资料
生殖细胞变异原性: 无资料
致癌性:
IARC = 无资料
NTP = 无资料
生殖毒性: 无资料
模块 12. 生态学信息
生态毒性:
鱼类: 无资料
甲壳类: 无资料
藻类: 无资料
残留性 / 降解性: 无资料
潜在生物累积 (BCF): 无资料
土壤中移动性
log水分配系数: 无资料
土壤吸收系数 (Koc): 无资料
亨利定律 无资料
constaNT(PaM3/mol):
模块 13. 废弃处置
如果可能,回收处理。请咨询当地管理部门。建议在装有后燃和洗涤装置的化学焚烧炉中焚烧。废弃处置时请遵守
国家、地区和当地的所有法规。
模块 14. 运输信息
联合国分类: 与联合国分类标准不一致
乙酰乙酸异戊酯 修改号码:5
模块 14. 运输信息
UN编号: 未列明
模块 15. 法规信息
《危险化学品安全管理条例》(2002年1月26日国务院发布,2011年2月16日修订): 针对危险化学品的安全使用、
生产、储存、运输、装卸等方面均作了相应的规定。
模块16 - 其他信息
N/A
模块 1. 化学品
产品名称: Isoamyl Acetoacetate
修改号码: 5
模块 2. 危险性概述
GHS分类
物理性危害 未分类
健康危害
皮肤腐蚀/刺激 第2级
严重损伤/刺激眼睛 2A类
环境危害 未分类
GHS标签元素
图标或危害标志
信号词 警告
危险描述 造成皮肤刺激
造成严重眼刺激
防范说明
[预防] 处理后要彻底清洗双手。
穿戴防护手套/护目镜/防护面具。
[急救措施] 眼睛接触:用水小心清洗几分钟。如果方便,易操作,摘除隐形眼镜。继续冲洗。
眼睛接触:求医/就诊
皮肤接触:用大量肥皂和水轻轻洗。
若皮肤刺激:求医/就诊。
脱掉被污染的衣物,清洗后方可重新使用。
模块 3. 成分/组成信息
单一物质/混和物 单一物质
化学名(中文名): 乙酰乙酸异戊酯
百分比: >97.0%(GC)
CAS编码: 2308-18-1
俗名: Acetoacetic Acid Isoamyl Ester , IsopeNTyl Acetoacetate
乙酰乙酸异戊酯 修改号码:5
模块 3. 成分/组成信息
分子式: C9H16O3
模块 4. 急救措施
吸入: 将受害者移到新鲜空气处,保持呼吸通畅,休息。若感不适请求医/就诊。
皮肤接触: 立即去除/脱掉所有被污染的衣物。用大量肥皂和水轻轻洗。
若皮肤刺激或发生皮疹:求医/就诊。
眼睛接触: 用水小心清洗几分钟。如果方便,易操作,摘除隐形眼镜。继续清洗。
如果眼睛刺激:求医/就诊。
食入: 若感不适,求医/就诊。漱口。
紧急救助者的防护: 救援者需要穿戴个人防护用品,比如橡胶手套和气密性护目镜。
模块 5. 消防措施
合适的灭火剂: 干粉,泡沫,二氧化碳
不适用的灭火剂: 水(有可能扩大灾情。)
特定方法: 从上风处灭火,根据周围环境选择合适的灭火方法。
非相关人员应该撤离至安全地方。
周围一旦着火:如果安全,移去可移动容器。
消防员的特殊防护用具: 灭火时,一定要穿戴个人防护用品。
模块 6. 泄漏应急处理
个人防护措施,防护用具, 使用个人防护用品。远离溢出物/泄露处并处在上风处。确保足够通风。
紧急措施: 泄露区应该用安全带等圈起来,控制非相关人员进入。
环保措施: 防止进入下水道。
控制和清洗的方法和材料: 用合适的吸收剂(如:旧布,干砂,土,锯屑)吸收泄漏物。一旦大量泄漏,筑堤控
制。附着物或收集物应该立即根据合适的法律法规废弃处置。
模块 7. 操作处置与储存
处理
技术措施: 在通风良好处进行处理。穿戴合适的防护用具。防止烟雾产生。处理后彻底清洗双手
和脸。
注意事项: 如果蒸气或浮质产生,使用通风、局部排气。
操作处置注意事项: 避免接触皮肤、眼睛和衣物。
贮存
储存条件: 保持容器密闭。存放于凉爽、阴暗处。
远离不相容的材料比如氧化剂存放。
包装材料: 依据法律。
模块 8. 接触控制和个体防护
工程控制: 尽可能安装封闭体系或局部排风系统,操作人员切勿直接接触。同时安装淋浴器和洗
眼器。
个人防护用品
呼吸系统防护: 防毒面具。依据当地和政府法规。
手部防护: 防护手套。
眼睛防护: 安全防护镜。如果情况需要,佩戴面具。
皮肤和身体防护: 防护服。如果情况需要,穿戴防护靴。
模块 9. 理化特性
外形(20°C): 液体
外观: 透明
乙酰乙酸异戊酯 修改号码:5
模块 9. 理化特性
颜色: 无色-几乎无色
气味: 无资料
pH: 无数据资料
熔点: 无资料
沸点/沸程 218 °C
闪点: 101°C
爆炸特性
爆炸下限: 无资料
爆炸上限: 无资料
密度: 0.97
溶解度:
[水] 无资料
[其他溶剂] 无资料
模块 10. 稳定性和反应性
化学稳定性: 一般情况下稳定。
危险反应的可能性: 未报道特殊反应性。
须避免接触的物质 氧化剂
危险的分解产物: 一氧化碳, 二氧化碳
模块 11. 毒理学信息
急性毒性: 无资料
对皮肤腐蚀或刺激: 无资料
对眼睛严重损害或刺激: 无资料
生殖细胞变异原性: 无资料
致癌性:
IARC = 无资料
NTP = 无资料
生殖毒性: 无资料
模块 12. 生态学信息
生态毒性:
鱼类: 无资料
甲壳类: 无资料
藻类: 无资料
残留性 / 降解性: 无资料
潜在生物累积 (BCF): 无资料
土壤中移动性
log水分配系数: 无资料
土壤吸收系数 (Koc): 无资料
亨利定律 无资料
constaNT(PaM3/mol):
模块 13. 废弃处置
如果可能,回收处理。请咨询当地管理部门。建议在装有后燃和洗涤装置的化学焚烧炉中焚烧。废弃处置时请遵守
国家、地区和当地的所有法规。
模块 14. 运输信息
联合国分类: 与联合国分类标准不一致
乙酰乙酸异戊酯 修改号码:5
模块 14. 运输信息
UN编号: 未列明
模块 15. 法规信息
《危险化学品安全管理条例》(2002年1月26日国务院发布,2011年2月16日修订): 针对危险化学品的安全使用、
生产、储存、运输、装卸等方面均作了相应的规定。
模块16 - 其他信息
N/A
制备方法与用途
上下游信息
反应信息
-
作为反应物:参考文献:名称:Komnenos, Monatshefte fur Chemie, 1910, vol. 31, p. 689摘要:DOI:
-
作为产物:参考文献:名称:Conrad, Justus Liebigs Annalen der Chemie, 1877, vol. 186, p. 241摘要:DOI:
文献信息
-
Visible Light-Mediated Coupling of Thioureas and 1,3-Dicarbonyls: Towards a Leaving Group-Free Synthesis of Aminothiazoles作者:Irwan Iskandar Roslan、Kian-Hong Ng、Mohammed Ashraf Gondal、Chanbasha Basheer、Mohamed A. Dastageer、Stephan Jaenicke、Gaik-Khuan ChuahDOI:10.1002/adsc.201701565日期:2018.4.17A synthesis of aminothiazoles from various 1,3‐dicarbonyls and thioureas without a leaving group has been developed. The reaction is photocatalyzed by tetraiodofluorescein, an organic dye. Under irradiation with green LEDs, a sulfur radical is generated in situ from thiourea, followed by addition to the enol tautomer, forming the aminothiazole backbone. This novel strategy provides a greener alternative
-
Synthesis of Heterobiaryl 4-Aryl Furans through a Base-Promoted Decarboxylative Propargylation/Cycloisomerization Annulation作者:Sasa Wang、Meimei Song、Xiuguang Li、Yunhong Huang、Tingxiang Zhao、Zhuoji Wei、Yanyun Lan、Haibo TanDOI:10.1021/acs.orglett.0c02668日期:2020.11.20A transition-metal-free synthesis of heterobiaryl 4-aryl furans through a base-promoted decarboxylative propargylation/cycloisomerization annulation of ethynyl benzoxazinanones and readily accessible β-keto esters or 1,3-diketones has been developed. A series of novel heterobiaryl 4-aryl furans were accessed efficiently in the presence of base under mild reaction conditions. This protocol is significant
-
Single‐Point Mutant Inverts the Stereoselectivity of a Carbonyl Reductase toward β‐Ketoesters with Enhanced Activity作者:Aipeng Li、Ting Wang、Qing Tian、Xiaohong Yang、Dongming Yin、Yong Qin、Lianbing ZhangDOI:10.1002/chem.202005195日期:2021.4.7Enzyme stereoselectivity control is still a major challenge. To gain insight into the molecular basis of enzyme stereo‐recognition and expand the source of antiPrelog carbonyl reductase toward β‐ketoesters, rational enzyme design aiming at stereoselectivity inversion was performed. The designed variant Q139G switched the enzyme stereoselectivity toward β‐ketoesters from Prelog to antiPrelog, providing酶的立体选择性控制仍然是主要挑战。为了深入了解酶立体识别的分子基础,并将antiPrelog羰基还原酶的来源扩展至β-酮酸酯,进行了针对立体选择性反转的合理酶设计。设计的Q139G变体将酶对β-酮酸酯的立体选择性从Prelog切换为antiPrelog,从而提供了相应的具有高对映体纯度(89.1–99.1%ee)的醇。更重要的是,在立体选择性和活性之间未找到众所周知的折衷方案。Q139G表现出比野生型酶更高的催化活性,提高了催化效率(k cat / K m)从1.1到27.1倍不等。有趣的是,突变体Q139G并未导致对芳族酮的立体选择性反转。酶-底物复合物的分析表明,β-酮酸酯的结构柔韧性和新形成的空穴共同促进了抗Prelog-首选构象的形成。相比之下,芳族酮的相对较大和刚性的结构阻止了它们形成抗Prelog优先的构象。
-
Sequential Organocatalytic Synthesis of [1,2,3]Triazolo[1,5‐ <i>a</i> ]quinolines作者:Gabriel P. Costa、Mariana F. Bach、Maiara C. Moraes、Thiago Barcellos、Eder J. Lenardão、Márcio S. Silva、Diego AlvesDOI:10.1002/adsc.202000887日期:2020.11.18organocatalytic method for the synthesis of fused [1,2,3]triazolo[1,5‐a]quinolines through successive cyclization and condensation is presented. In this synthetic strategy, the intermolecular [3+2]‐cycloaddition occurs between 1,3‐dicarbonyl compounds and o‐carbonyl‐substituted phenylazide compounds, for the formation of the 1,2,3‐triazole intermediates. Subsequently, an intramolecular condensation reaction在这项工作中,提出了一种通过连续环化和缩合反应合成稠合[1,2,3]三唑并[1,5- a ]喹啉的单锅顺序有机催化方法。在这种合成策略中,分子间的[3 + 2]-环加成反应发生在1,3-二羰基化合物与邻羰基取代的苯叠氮化合物之间,从而形成1,2,3-三唑中间体。随后,分子内的缩合反应通过新的C-C键的形成生成稠合的喹啉环,从而使产物的收率从中等到极好。在DMSO作为溶剂存在下,使用20 mol%的1,8-二氮杂双环[5.4.0]十一碳-7-烯(DBU)作为催化剂,在120°C下进行24 h,反应范围为1。 ,3-二羰基化合物,例如β-酮酸酯和1,3-二酮,以及邻甲酰基,邻乙酰基或邻苯甲酰基取代的苯叠氮化合物。
-
Synthesis and Antihypertensive Activities of New 1,4-Dihydropyridine Derivatives Containing a Nitrooxy Moiety at the 3-Ester Position.作者:Toshihisa OGAWA、Atsuro NAKAZATO、Katsuharu TSUCHIDA、Katsuo HATAYAMADOI:10.1248/cpb.41.108日期:——The synthesis of a new series of dihydropyridines containing a nitrooxy mojety at the 3-ester position is described.The antihypertensive activity of the compounds was examined and compared with that of nifedipine; some of them were relatively potent. The structure-activity relationship is also discussed.研究合成了一系列在3-酯位含有硝氧基的二氢吡啶类新化合物。这些化合物的降压活性经检验并与尼非地平相比较;其中一些相对具有较强的活性。同时还讨论了结构与活性之间的关系。
表征谱图
-
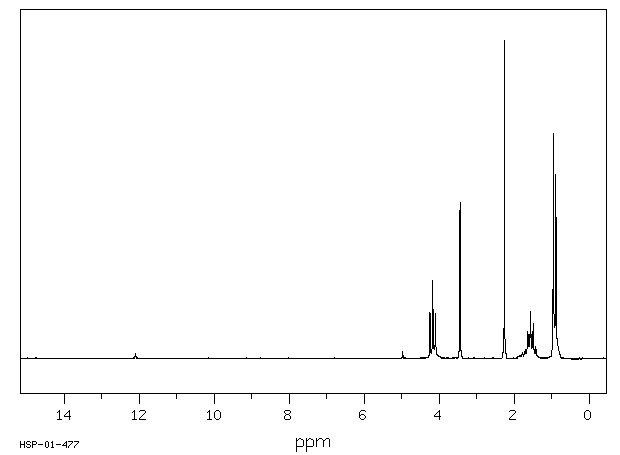
氢谱1HNMR
-
质谱MS
-
碳谱13CNMR
-
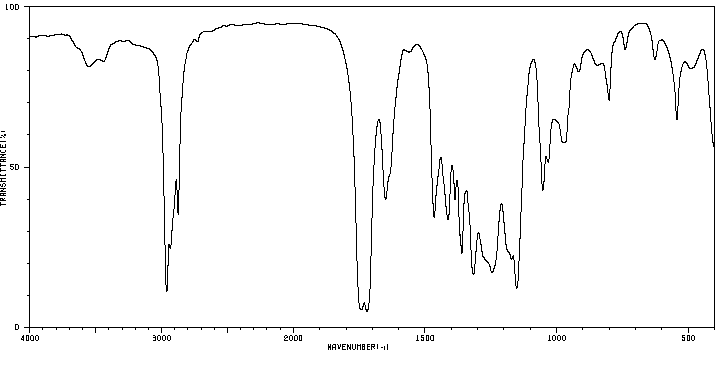
红外IR
-
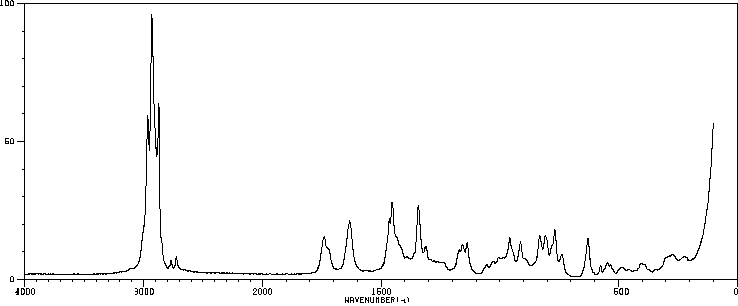
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息
同类化合物
马来酰基乙酸
顺-3-己烯-1-丙酮酸
青霉酸
钠氟草酰乙酸二乙酯
醚化物
酮霉素
辛酸,2,4-二羰基-,乙基酯
草酸乙酯钠盐
草酰乙酸二乙酯钠盐
草酰乙酸二乙酯
草酰乙酸
草酰丙酸二乙酯
苯乙酰丙二酸二乙酯
苯丁酸,b-羰基-,2-丙烯基酯
聚氧化乙烯
羟基-(3-羟基-2,3-二氧代丙基)-氧代鏻
磷酸二氢2-{(E)-2-[4-(二乙胺基)-2-甲基苯基]乙烯基}-1,3,3-三甲基-3H-吲哚正离子
碘化镝
硬脂酰乙酸乙酯
甲氧基乙酸乙酯
甲氧基乙酰乙酸酯
甲基氧代琥珀酸二甲盐
甲基4-环己基-3-氧代丁酸酯
甲基4-氯-3-氧代戊酸酯
甲基4-氧代癸酸酯
甲基4-氧代月桂酸酯
甲基4-(甲氧基-甲基磷酰)-2,2,4-三甲基-3-氧代戊酸酯
甲基3-羰基-2-丙酰戊酸酯
甲基3-氧代十五烷酸酯
甲基2-氟-3-氧戊酯
甲基2-氟-3-氧代己酸酯
甲基2-氟-3-氧代丁酸酯
甲基2-乙酰基环丙烷羧酸酯
甲基2-乙酰基-4-甲基-4-戊烯酸酯
甲基2-乙酰基-2-丙-2-烯基戊-4-烯酸酯
甲基2,5-二氟-3-氧代戊酸酯
甲基2,4-二氟-3-氧代戊酸酯
甲基2,4-二氟-3-氧代丁酸酯
甲基1-异丁酰基环戊烷羧酸酯
甲基1-乙酰基环戊烷羧酸酯
甲基1-乙酰基环丙烷羧酸酯
甲基1-乙酰基-2-乙基环丙烷羧酸酯
甲基(2Z,4E,6E)-2-乙酰基-7-(二甲基氨基)-2,4,6-庚三烯酸酯
甲基(2S)-2-甲基-4-氧代戊酸酯
甲基(1S,2R)-2-乙酰基环丙烷羧酸酯
甲基(1R,2R)-2-乙酰基环丙烷羧酸酯
瑞舒伐他汀杂质
瑞舒伐他汀杂质
环氧乙烷基甲基乙酰乙酸酯
环戊戊烯酸,Β-氧代,乙酯