aspartate anion
中文名称
——
中文别名
——
英文名称
aspartate anion
英文别名
L-aspartate;aspartate;Asp;L-aspartate(1-);(2S)-2-amino-4-hydroxy-4-oxobutanoate
CAS
——
化学式
C4H6NO4
mdl
——
分子量
132.096
InChiKey
CKLJMWTZIZZHCS-REOHCLBHSA-M
BEILSTEIN
——
EINECS
——
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
计算性质
-
辛醇/水分配系数(LogP):-2.6
-
重原子数:9
-
可旋转键数:1
-
环数:0.0
-
sp3杂化的碳原子比例:0.5
-
拓扑面积:108
-
氢给体数:1
-
氢受体数:4
反应信息
-
作为反应物:描述:aspartate anion 在 L-半胱氨酸 、 磷酸吡哆醛 、 aspartate decarboxylase 作用下, 以 aq. phosphate buffer 为溶剂, 反应 0.17h, 生成 β-丙氨酸参考文献:名称:天冬氨酸/谷氨酸/半胱氨酸亚磺酸α-脱羧酶的半胱氨酸依赖性失活机制摘要:动物天冬氨酸脱羧酶 (ADC)、谷氨酸脱羧酶 (GDC) 和半胱氨酸亚磺酸脱羧酶 (CSADC) 分别催化天冬氨酸、谷氨酸和半胱氨酸亚磺酸脱羧为 β-丙氨酸、γ-氨基丁酸和亚牛磺酸。每种酶产物都涉及不同的生理功能。这些脱羧酶使用 5-磷酸吡哆醛 (PLP) 作为辅因子并具有高度的序列同源性。在不同氨基存在下对 ADC 活性的分析确定,在半胱氨酸存在下,天冬氨酸产生的 β-丙氨酸减少。比较分析确定半胱氨酸也以浓度依赖性方式抑制 GDC 和 CSADC。游离 PLP 和半胱氨酸以及 ADC 和半胱氨酸的光谱比较导致可比较的光谱偏移。这种光谱变化表明半胱氨酸能够进入酶的活性位点,与 PLP-赖氨酸内部醛亚胺相互作用,形成半胱氨酸-PLP 醛亚胺并通过其巯基进行分子内亲核环化,导致不可逆的 ADC 失活。半胱氨酸是蛋白质合成的基石和半胱氨酸亚磺酸的前体,后者是 CSADC 的底物,因此存在于许多细DOI:10.1007/s00726-012-1342-7
-
作为产物:描述:参考文献:名称:A thermodynamic insight into the recognition of hydrophilic and hydrophobic amino acids in pure water by aza-scorpiand type receptors摘要:在水中关于蝎烯和氮杂大环与氨基酸相互作用的热力学研究表明,熵驱动的稳定化通常与溶解/脱溶过程相关。DOI:10.1039/c4ob02092h
-
作为试剂:描述:参考文献:名称:Biochemical and Structural Characterization of a Ureidoglycine Aminotransferase in the Klebsiella pneumoniae Uric Acid Catabolic Pathway摘要:Many plants, fungi, and bacteria catabolize allantoin as a mechanism for nitrogen assimilation. Recent reports have shown that in plants and some bacteria the product of hydrolysis of allantoin by allantoinase is the unstable intermediate ureidoglycine. While this molecule can spontaneously decay, genetic analysis of some bacterial genomes indicates that an aminotransferase may be present in the pathway. Here we present evidence that Klebsiella pneumoniae HpxJ is an aminotransferase that preferentially converts ureidoglycine and an a-keto acid into oxalurate and the corresponding amino acid. We determined the crystal structure of HpxJ, allowing us to present an explanation for substrate specificity.DOI:10.1021/bi1006755
文献信息
-
Purification and Characterization of the First Archaeal Glutamate Decarboxylase from<i>Pyrococcus horikoshii</i>作者:Han-Woo KIM、Yasuhiro KASHIMA、Kazuhiko ISHIKAWA、Naoko YAMANODOI:10.1271/bbb.80583日期:2009.1.23Glutamate decarboxylase (GAD) from the archaeon Pyrococcus horikoshii was successfully expressed and purified, with the aim of developing a hyperthermostable GAD for industrial applications. Its biochemical properties were different from those reported for other GADs. The enzyme had broad substrate specificity, and its optimum pH and temperature were pH 8.0 and >97 °C.来自古菌株Pyrococcus horikoshii的谷氨酸脱羧酶(GAD)成功表达并纯化,旨在开发用于工业应用的超热稳定GAD。其生化特性与之前报道的其他GAD不同。该酶具有广泛的底物特异性,其最适pH和温度分别为pH 8.0和>97 °C。
-
An investigation of the equilibrium of the reaction {L-aspartate(aq)+2-oxoglutarate(aq)=oxaloacetate(aq)+L-glutamate(aq)}作者:Nand Kishore、Yadu B. Tewari、Robert N. GoldbergDOI:10.1006/jcht.1998.0404日期:1998.11accompanied the reaction. Values of ΔRwere measured for several solutions under near equilibrium conditions. The chromatographic response ΔRis expected to be zero for a solution that is at equilibrium with regard to the above reaction and prior to the addition of the enzyme. The results were used to calculate the standard molar Gibbs energy change ΔrGm°=(4.82±0.21) kJ·mol−1, the equilibrium constantK=(0已测量以下生化反应的表观平衡常数:L-天冬氨酸(aq) + 2-酮戊二酸(aq) = 草酰乙酸(aq) + L-谷氨酸(aq)。该反应由天冬氨酸转氨酶催化,在 283.15≤T/K≤303.15、6.94≤pH≤7.13 和 0.163≤Im/(mol·kg-1)≤0.167 的范围内进行研究,其中 Ti 是温度和 Imis 离子强度。溶液中草酰乙酸的不稳定性需要使用简短的实验程序。因此,所使用的程序是测量伴随反应的草酰乙酸酯色谱峰的色谱响应ΔR的变化。在接近平衡条件下测量几种溶液的 ΔR 值。对于在上述反应中处于平衡状态且在添加酶之前的溶液,色谱响应 ΔRis 预计为零。结果用于计算标准摩尔吉布斯能量变化ΔrGm°=(4.82±0.21) kJ·mol−1,平衡常数K=(0.143±0.012),标准摩尔焓变ΔrHm°=(1.9±2.9) kJ ·mol−1,标准摩尔熵变ΔrSm°=− -03(10±10)
-
Direct evidence that an extended hydrogen-bonding network influences activation of pyridoxal 5′-phosphate in aspartate aminotransferase作者:Steven Dajnowicz、Jerry M. Parks、Xiche Hu、Korie Gesler、Andrey Y. Kovalevsky、Timothy C. MueserDOI:10.1074/jbc.m116.774588日期:2017.4protonation state of the pyridine nitrogen of PLP, which affects the rates of catalysis. We analyzed perturbations caused by single- and double-mutant variants using steady-state kinetics, high resolution X-ray crystallography, and quantum chemical calculations. Protonation of the pyridinyl nitrogen to form a pyridinium cation induces electronic delocalization in the PLP, which correlates with the enhancement吡rid醛5'-磷酸(PLP)是一种基本的多功能酶辅因子,用于催化氨基酸代谢中涉及的多种化学反应。依赖PLP的酶可通过不同的活性位点环境调节PLP的电子状态,从而优化特定的化学反应。在天冬氨酸氨基转移酶(AAT)中,扩展的氢键网络与PLP的吡啶基氮偶联,影响辅因子的亲电性。该网络涉及残基Asp-222,His-143,Thr-139,His-189和结构水,位于与反应席夫碱相对的PLP边缘。我们证明该氢键网络直接影响PLP吡啶氮的质子化状态,从而影响催化速率。我们使用稳态动力学,高分辨率X射线晶体学和量子化学计算分析了由单突变体和双突变体引起的扰动。吡啶基氮的质子化形成吡啶鎓阳离子会在PLP中引起电子离域,这与AAT催化速率的提高相关。因此,通过吡啶基氮与氢键微环境的接近来控制PLP活化。量子化学计算表明,直接与吡啶基氮偶合的Asp-222增加了吡啶氮的pKa并使吡啶鎓阳离子稳定。His-
-
The Stereochemistry and Reactivity of Metal-Schiff Base Complexes. VII. Contribution of Hydrophobic Interligand Interaction to Chiral Recognition of Phenylalaninate and Tryptophanate with (1<i>R</i>,2<i>R</i>)-<i>N</i>,<i>N</i>′-Disalicylidene-1,2-cyclohexanediaminecobalt(III) Complex作者:Yuki Fujii、Yuzo Yoshikawa、Masato Syoji、Homare ShinoharaDOI:10.1246/bcsj.63.138日期:1990.1The stability constants, K1, of Δ-β2-diastereomers of mixed ligand cobalt(III) complexes with a chiral quadridentate Schiff base (sal-(R,R)-chxn), derived from salicylaldehyde and (R,R)-1,2-cyclohexanediamine, and d- or l-amino acidate (aa−=gly, ala, val, leu, thr, phe, trp, pro, asp, asn, and glu) were determined spectrophotometrically in water–methanol (2:3 by volume) containing acetate buffer (0.3 mol dm−3) at 22°C: trans-[Cosal-(R,R)-chxn}(H2O)2]++aa−\oversetK1\ightleftharpoonsΔ-β2-[Cosal-(R,R)-chxn}(aa)]. The K1 values range from 5.6×106 to 1.2×109 mol−1 dm3 and obey a linear free energy relationship except for d-phe, d-trp, d-asp, d-asn, and d-pro. In the cases of d-phe, d-trp, d-asp, and d-asn, their stability constants are 5–30 times as high as those for the corresponding l-aa. Extraordinary stabilization of the d-phe and d-trp complexes is discussed in terms of the interligand stacking of the aromatic rings between the Schiff base ligand and a side chain of amino acidate on the basis of conformational analysis and 1H NMR spectra.Δ-β2-型混配体钴(III)配合物的稳定常数K1是通过光谱法在22°C下,在含有乙酸盐缓冲液(0.3 mol dm−3)的水-甲醇(2:3体积比)混合溶液中测定的。这些配合物由手性四齿席夫碱(sal-(R,R)-chxn)和d-或l-氨基酸根(aa− = gly、ala、val、leu、thr、phe、trp、pro、asp、asn和glu)组成。sal-(R,R)-chxn是由水杨醛和(R,R)-1,2-环己二胺衍生而来。 K1值范围在5.6×106到1.2×109 mol−1 dm3之间,除了d-phe、d-trp、d-asp、d-asn和d-pro外,都符合线性自由能关系。对于d-phe、d-trp、d-asp和d-asn,它们的稳定常数是相应l-氨基酸的5-30倍。 基于构象分析和1H NMR光谱,文章讨论了d-phe和d-trp配合物的特殊稳定性,认为这与席夫碱配体和氨基酸侧链之间的芳香环层间堆积有关。
-
Altering the Substrate Specificity of Glutamate Dehydrogenase from<i>Bacillus subtilis</i>by Site-Directed Mutagenesis作者:Md. Iqbal Hassan KHAN、Hyeung KIM、Hiroyuki ASHIDA、Takahiro ISHIKAWA、Hitoshi SHIBATA、Yoshihiro SAWADOI:10.1271/bbb.69.1802日期:2005.1The Lys80, Gly82 and Met101 residues of glutamate dehydrogenase from Bacillus subtilis were mutated into a series of single mutants. The wild-type enzyme was highly specific for 2-oxoglutarate, whereas G82K and M101S dramatically switched to increased specificity for oxaloacetate with kcat values 3.45 and 5.68 s-1, which were 265-fold and 473-fold higher respectively than those for 2-oxoglutarate.
表征谱图
-
氢谱1HNMR
-
质谱MS
-
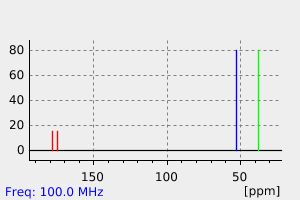
碳谱13CNMR
-
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息
同类化合物
(甲基3-(二甲基氨基)-2-苯基-2H-azirene-2-羧酸乙酯)
(±)-盐酸氯吡格雷
(±)-丙酰肉碱氯化物
(d(CH2)51,Tyr(Me)2,Arg8)-血管加压素
(S)-(+)-α-氨基-4-羧基-2-甲基苯乙酸
(S)-阿拉考特盐酸盐
(S)-赖诺普利-d5钠
(S)-2-氨基-5-氧代己酸,氢溴酸盐
(S)-2-[[[(1R,2R)-2-[[[3,5-双(叔丁基)-2-羟基苯基]亚甲基]氨基]环己基]硫脲基]-N-苄基-N,3,3-三甲基丁酰胺
(S)-2-[3-[(1R,2R)-2-(二丙基氨基)环己基]硫脲基]-N-异丙基-3,3-二甲基丁酰胺
(S)-1-(4-氨基氧基乙酰胺基苄基)乙二胺四乙酸
(S)-1-[N-[3-苯基-1-[(苯基甲氧基)羰基]丙基]-L-丙氨酰基]-L-脯氨酸
(R)-乙基N-甲酰基-N-(1-苯乙基)甘氨酸
(R)-丙酰肉碱-d3氯化物
(R)-4-N-Cbz-哌嗪-2-甲酸甲酯
(R)-3-氨基-2-苄基丙酸盐酸盐
(R)-1-(3-溴-2-甲基-1-氧丙基)-L-脯氨酸
(N-[(苄氧基)羰基]丙氨酰-N〜5〜-(diaminomethylidene)鸟氨酸)
(6-氯-2-吲哚基甲基)乙酰氨基丙二酸二乙酯
(4R)-N-亚硝基噻唑烷-4-羧酸
(3R)-1-噻-4-氮杂螺[4.4]壬烷-3-羧酸
(3-硝基-1H-1,2,4-三唑-1-基)乙酸乙酯
(2S,4R)-Boc-4-环己基-吡咯烷-2-羧酸
(2S,3S,5S)-2-氨基-3-羟基-1,6-二苯己烷-5-N-氨基甲酰基-L-缬氨酸
(2S,3S)-3-((S)-1-((1-(4-氟苯基)-1H-1,2,3-三唑-4-基)-甲基氨基)-1-氧-3-(噻唑-4-基)丙-2-基氨基甲酰基)-环氧乙烷-2-羧酸
(2S)-2,6-二氨基-N-[4-(5-氟-1,3-苯并噻唑-2-基)-2-甲基苯基]己酰胺二盐酸盐
(2S)-2-氨基-N,3,3-三甲基-N-(苯甲基)丁酰胺
(2S)-2-氨基-3-甲基-N-2-吡啶基丁酰胺
(2S)-2-氨基-3,3-二甲基-N-(苯基甲基)丁酰胺,
(2S)-2-氨基-3,3-二甲基-N-2-吡啶基丁酰胺
(2S,4R)-1-((S)-2-氨基-3,3-二甲基丁酰基)-4-羟基-N-(4-(4-甲基噻唑-5-基)苄基)吡咯烷-2-甲酰胺盐酸盐
(2R,3'S)苯那普利叔丁基酯d5
(2R)-2-氨基-3,3-二甲基-N-(苯甲基)丁酰胺
(2-氯丙烯基)草酰氯
(1S,3S,5S)-2-Boc-2-氮杂双环[3.1.0]己烷-3-羧酸
(1R,5R,6R)-5-(1-乙基丙氧基)-7-氧杂双环[4.1.0]庚-3-烯-3-羧酸乙基酯
(1R,4R,5S,6R)-4-氨基-2-氧杂双环[3.1.0]己烷-4,6-二羧酸
齐特巴坦
齐德巴坦钠盐
齐墩果-12-烯-28-酸,2,3-二羟基-,苯基甲基酯,(2a,3a)-
齐墩果-12-烯-28-酸,2,3-二羟基-,羧基甲基酯,(2a,3b)-(9CI)
黄酮-8-乙酸二甲氨基乙基酯
黄荧菌素
黄体生成激素释放激素(1-6)
黄体生成激素释放激素 (1-5) 酰肼
黄体瑞林
麦醇溶蛋白
麦角硫因
麦芽聚糖六乙酸酯
麦根酸