反式-2-苯基-2-丁烯 | 768-00-3
中文名称
反式-2-苯基-2-丁烯
中文别名
——
英文名称
(E)-2-phenyl-2-butene
英文别名
(E)-but-2-en-2-ylbenzene;(E)-2-phenylbut-2-ene;trans-2-phenyl-2-butene;but-2-en-2-ylbenzene;α,β-dimethylstyrene;Benzene, (1-methyl-1-propenyl)-, (E)-;[(E)-but-2-en-2-yl]benzene
CAS
768-00-3
化学式
C10H12
mdl
——
分子量
132.205
InChiKey
UGUYQBMBIJFNRM-YCRREMRBSA-N
BEILSTEIN
——
EINECS
——
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
物化性质
-
熔点:-23.5°C
-
沸点:194.85°C
-
密度:0.9138
-
保留指数:1090.7;1090.7
计算性质
-
辛醇/水分配系数(LogP):3.7
-
重原子数:10
-
可旋转键数:1
-
环数:1.0
-
sp3杂化的碳原子比例:0.2
-
拓扑面积:0
-
氢给体数:0
-
氢受体数:0
SDS
上下游信息
-
上游原料
中文名称 英文名称 CAS号 化学式 分子量 反式-2-苯基-2-丁烯 (Z)-2-phenylbut-2-ene 767-99-7 C10H12 132.205 —— (E)-3-phenylbut-2-en-1-ol 54976-38-4 C10H12O 148.205 —— (E)-1-bromo-3-phenyl-2-butene —— C10H11Br 211.101 2-苯基-1-丙烯 isopropenylbenzene 98-83-9 C9H10 118.178 —— (Z)-(1-bromobut-2-en-2-yl)benzene —— C10H11Br 211.101 —— 1-methyl-1-phenylallene 22433-39-2 C10H10 130.189 Alpha-乙基苯乙烯 1-ethylstyrene 2039-93-2 C10H12 132.205 —— (E)-(1-bromoprop-1-en-2-yl)benzene 16917-35-4 C9H9Br 197.074 反-β-甲基肉桂酸乙酯 ethyl (E)-3-phenylbut-2-enoate 1504-72-9 C12H14O2 190.242 -
下游产品
中文名称 英文名称 CAS号 化学式 分子量 反式-2-苯基-2-丁烯 (Z)-2-phenylbut-2-ene 767-99-7 C10H12 132.205 —— β-methylcinnamyl acetate 20883-16-3 C12H14O2 190.242 Alpha-乙基苯乙烯 1-ethylstyrene 2039-93-2 C10H12 132.205
反应信息
-
作为反应物:描述:参考文献:名称:探索在 Jacobsen-Katsuki 环氧化中运行的竞争性对映选择性方法载体:甲基取代苯乙烯的动力学研究摘要:本文描述了一系列甲基取代苯乙烯在 Jacobsen-Katsuki(Mn(salen)催化)环氧化反应中的反应性和对映选择性研究。竞争实验提供了七种可能的甲基取代苯乙烯(单取代、二取代和三取代)相对于苯乙烯本身的反应性的动力学数据,ee 值通过手性 GC 测量,绝对构型通过化学相关性得到保证。特别令人感兴趣的是分别衍生自 (Z)-和 (E)-α,β-二甲基苯乙烯的环氧化物在苄基位置的绝对构型转换。结果可以根据具有接近 salen 的苯基取代基的方法向量进行合理化。与烷基相反,近端苯基对反应速率的影响很小。考虑远端与近端方法允许预测绝对立体化学作为烯烃取代模式的函数。具有一个与烯烃氢顺式的苯基的三取代烯烃可以被确定为标题反应中有利的底物类别,其速率和选择性都接近经典的 (Z)-β-取代的苯乙烯底物。DOI:10.1021/ja051851f
-
作为产物:描述:反式-2-苯基-2-丁烯 在 2,6-双[(3aR,8aS)-(+)-8H-茚[1,2-d]恶唑啉-2-基]吡啶 、 indium(III) chloride 、 silver hexafluoroantimonate 作用下, 以 1,2-二氯乙烷 为溶剂, 反应 48.0h, 以21%的产率得到反式-2-苯基-2-丁烯参考文献:名称:Highly Enantioselective and Anti-Diastereoselective Catalytic Intermolecular Glyoxylate–Ene Reactions: Effect of the Geometrical Isomers of Alkenes摘要:An efficient method for the synthesis of homoallylic alcohols with high enantioselectivities and anti-diastereoselectivities via an In(III)-catalyzed intermolecular glyoxylateene reaction has been developed. The geometrical isomers of alkenes were shown to have different reactivities. Only the isomers of the alkenes having a proton beta-cis to the substituent reacted in this catalytic system.DOI:10.1021/acs.orglett.5b01151
文献信息
-
Nickel-Catalyzed Kumada Reaction of Tosylalkanes with Grignard Reagents to Produce Alkenes and Modified Arylketones作者:Ji-Cheng Wu、Lu-Bing Gong、Yuanzhi Xia、Ren-Jie Song、Ye-Xiang Xie、Jin-Heng LiDOI:10.1002/anie.201205969日期:2012.9.24Open a new door: The first example of alkene synthesis from alkyl electrophiles with Grignard reagents using the Kumada cross‐coupling reaction strategy is reported. This method opens a new door for the Kumada cross‐coupling reaction, allowing alkenes to be prepared from the reaction of tosylalkanes with Grignard reagents.
-
Copper(I)-Catalyzed Allylic Substitutions with a Hydride Nucleophile作者:T. N. Thanh Nguyen、Niklas O. Thiel、Felix Pape、Johannes F. TeichertDOI:10.1021/acs.orglett.6b00941日期:2016.5.20easily accessible copper(I)/N-heterocyclic carbene (NHC) complex enables a regioselective hydride transfer to allylic bromides, an allylic reduction. The resulting aryl- and alkyl-substituted branched α-olefins, which are valuable building blocks for synthesis, are obtained in good yields and regioselectivity. A commercially available silane, (TMSO)2Si(Me)H, is employed as hydride source. This protocol
-
Catalytic asymmetric epoxidation申请人:——公开号:US06348608B1公开(公告)日:2002-02-19A compound and method for producing an enantiomerically enriched epoxide from an olefin using a chiral ketone and an oxidizing agent is disclosed.一种化合物及其生产方法被披露,该方法使用手性酮和氧化剂从烯烃生产具有对映体富集的环氧乙烷。
-
Stereoselective Alkene Isomerization over One Position作者:Casey R. Larsen、Douglas B. GrotjahnDOI:10.1021/ja3036477日期:2012.6.27Although controlling both the position of the double bond and E:Z selectivity in alkene isomerization is difficult, 1 is a very efficient catalyst for selective mono-isomerization of a variety of multifunctional alkenes to afford >99.5% E-products. Many reactions are complete within 10 min at room temperature. Even sensitive enols and enamides susceptible to further reaction can be generated. Catalyst尽管在烯烃异构化中控制双键的位置和 E:Z 选择性很困难,但 1 是一种非常有效的催化剂,可用于多种多功能烯烃的选择性单异构化,以提供 >99.5% 的 E 产物。许多反应在室温下 10 分钟内完成。甚至可以生成对进一步反应敏感的敏感烯醇和烯酰胺。可以使用 0.01-0.1 mol% 范围内的催化剂负载量。二烯丙基醚产物的 E-to-Z 异构化速度仅为其形成速度的 <10(-6) 倍,显示出极高的动力学选择性 1。
-
Asymmetric Epoxidation of Conjugated Olefins with Dioxygen作者:Shota Koya、Yota Nishioka、Hirotaka Mizoguchi、Tatsuya Uchida、Tsutomu KatsukiDOI:10.1002/anie.201201848日期:2012.8.13A complex situation: Asymmetric epoxidation of conjugated olefins was achieved at room temperature using ruthenium complex 1 as the catalyst and air as the oxidant to give epoxides in up to 95 % ee (see scheme). When the product was acid sensitive, the reaction was carried out at 0 °C under oxygen.
表征谱图
-
氢谱1HNMR
-
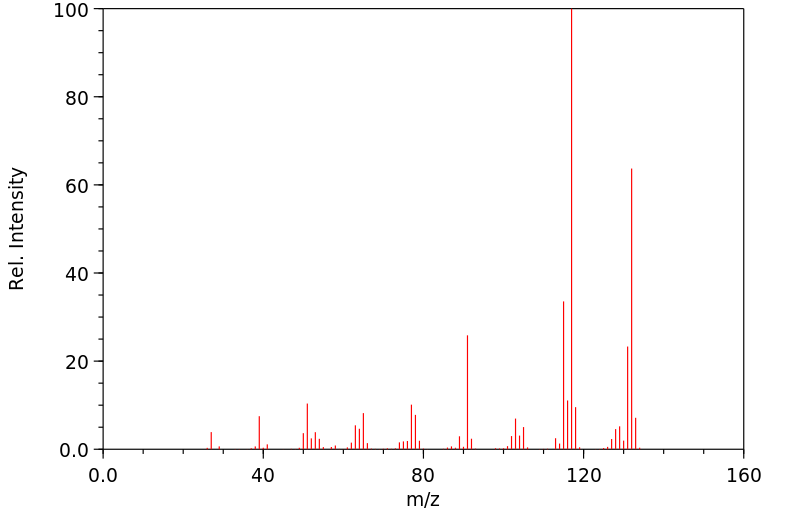
质谱MS
-
碳谱13CNMR
-
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息
同类化合物
(βS)-β-氨基-4-(4-羟基苯氧基)-3,5-二碘苯甲丙醇
(S,S)-邻甲苯基-DIPAMP
(S)-(-)-7'-〔4(S)-(苄基)恶唑-2-基]-7-二(3,5-二-叔丁基苯基)膦基-2,2',3,3'-四氢-1,1-螺二氢茚
(S)-盐酸沙丁胺醇
(S)-3-(叔丁基)-4-(2,6-二甲氧基苯基)-2,3-二氢苯并[d][1,3]氧磷杂环戊二烯
(S)-2,2'-双[双(3,5-三氟甲基苯基)膦基]-4,4',6,6'-四甲氧基联苯
(S)-1-[3,5-双(三氟甲基)苯基]-3-[1-(二甲基氨基)-3-甲基丁烷-2-基]硫脲
(R)富马酸托特罗定
(R)-(-)-盐酸尼古地平
(R)-(-)-4,12-双(二苯基膦基)[2.2]对环芳烷(1,5环辛二烯)铑(I)四氟硼酸盐
(R)-(+)-7-双(3,5-二叔丁基苯基)膦基7''-[((6-甲基吡啶-2-基甲基)氨基]-2,2'',3,3''-四氢-1,1''-螺双茚满
(R)-(+)-7-双(3,5-二叔丁基苯基)膦基7''-[(4-叔丁基吡啶-2-基甲基)氨基]-2,2'',3,3''-四氢-1,1''-螺双茚满
(R)-(+)-7-双(3,5-二叔丁基苯基)膦基7''-[(3-甲基吡啶-2-基甲基)氨基]-2,2'',3,3''-四氢-1,1''-螺双茚满
(R)-(+)-4,7-双(3,5-二-叔丁基苯基)膦基-7“-[(吡啶-2-基甲基)氨基]-2,2”,3,3'-四氢1,1'-螺二茚满
(R)-3-(叔丁基)-4-(2,6-二苯氧基苯基)-2,3-二氢苯并[d][1,3]氧杂磷杂环戊烯
(R)-2-[((二苯基膦基)甲基]吡咯烷
(R)-1-[3,5-双(三氟甲基)苯基]-3-[1-(二甲基氨基)-3-甲基丁烷-2-基]硫脲
(N-(4-甲氧基苯基)-N-甲基-3-(1-哌啶基)丙-2-烯酰胺)
(5-溴-2-羟基苯基)-4-氯苯甲酮
(5-溴-2-氯苯基)(4-羟基苯基)甲酮
(5-氧代-3-苯基-2,5-二氢-1,2,3,4-oxatriazol-3-鎓)
(4S,5R)-4-甲基-5-苯基-1,2,3-氧代噻唑烷-2,2-二氧化物-3-羧酸叔丁酯
(4S,4''S)-2,2''-亚环戊基双[4,5-二氢-4-(苯甲基)恶唑]
(4-溴苯基)-[2-氟-4-[6-[甲基(丙-2-烯基)氨基]己氧基]苯基]甲酮
(4-丁氧基苯甲基)三苯基溴化磷
(3aR,8aR)-(-)-4,4,8,8-四(3,5-二甲基苯基)四氢-2,2-二甲基-6-苯基-1,3-二氧戊环[4,5-e]二恶唑磷
(3aR,6aS)-5-氧代六氢环戊基[c]吡咯-2(1H)-羧酸酯
(2Z)-3-[[(4-氯苯基)氨基]-2-氰基丙烯酸乙酯
(2S,3S,5S)-5-(叔丁氧基甲酰氨基)-2-(N-5-噻唑基-甲氧羰基)氨基-1,6-二苯基-3-羟基己烷
(2S,2''S,3S,3''S)-3,3''-二叔丁基-4,4''-双(2,6-二甲氧基苯基)-2,2'',3,3''-四氢-2,2''-联苯并[d][1,3]氧杂磷杂戊环
(2S)-(-)-2-{[[[[3,5-双(氟代甲基)苯基]氨基]硫代甲基]氨基}-N-(二苯基甲基)-N,3,3-三甲基丁酰胺
(2S)-2-[[[[[((1S,2S)-2-氨基环己基]氨基]硫代甲基]氨基]-N-(二苯甲基)-N,3,3-三甲基丁酰胺
(2S)-2-[[[[[[((1R,2R)-2-氨基环己基]氨基]硫代甲基]氨基]-N-(二苯甲基)-N,3,3-三甲基丁酰胺
(2-硝基苯基)磷酸三酰胺
(2,6-二氯苯基)乙酰氯
(2,3-二甲氧基-5-甲基苯基)硼酸
(1S,2S,3S,5S)-5-叠氮基-3-(苯基甲氧基)-2-[(苯基甲氧基)甲基]环戊醇
(1S,2S,3R,5R)-2-(苄氧基)甲基-6-氧杂双环[3.1.0]己-3-醇
(1-(4-氟苯基)环丙基)甲胺盐酸盐
(1-(3-溴苯基)环丁基)甲胺盐酸盐
(1-(2-氯苯基)环丁基)甲胺盐酸盐
(1-(2-氟苯基)环丙基)甲胺盐酸盐
(1-(2,6-二氟苯基)环丙基)甲胺盐酸盐
(-)-去甲基西布曲明
龙蒿油
龙胆酸钠
龙胆酸叔丁酯
龙胆酸
龙胆紫-d6
龙胆紫