3-(4-chloro-phenyl)-oxazolidin-2-one | 5198-49-2
中文名称
——
中文别名
——
英文名称
3-(4-chloro-phenyl)-oxazolidin-2-one
英文别名
N-(4-chlorophenyl)oxazolidin-2-one;2-Oxazolidinone, 3-(4-chlorophenyl)-;3-(4-chlorophenyl)-1,3-oxazolidin-2-one
CAS
5198-49-2
化学式
C9H8ClNO2
mdl
——
分子量
197.621
InChiKey
VCXDTSPEDCOTCJ-UHFFFAOYSA-N
BEILSTEIN
——
EINECS
——
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
计算性质
-
辛醇/水分配系数(LogP):2.1
-
重原子数:13
-
可旋转键数:1
-
环数:2.0
-
sp3杂化的碳原子比例:0.22
-
拓扑面积:29.5
-
氢给体数:0
-
氢受体数:2
安全信息
-
海关编码:2934999090
SDS
上下游信息
-
上游原料
中文名称 英文名称 CAS号 化学式 分子量 N-(p-氯苯基)氨基钾酸酯 ethyl p-chlorophenylcarbamate 2621-80-9 C9H10ClNO2 199.637 —— 1-chloro-2-(4-chloro-phenylcarbamoyloxy)-ethane 25217-18-9 C9H9Cl2NO2 234.082 4-氯-(N-Boc)苯胺 N-(t-butoxycarbonyl)-4-chloroaniline 18437-66-6 C11H14ClNO2 227.691 -
下游产品
中文名称 英文名称 CAS号 化学式 分子量 —— 3-(4-chlorophenyl)-4-methyloxazolidin-2-one 121485-41-4 C10H10ClNO2 211.648
反应信息
-
作为反应物:描述:3-(4-chloro-phenyl)-oxazolidin-2-one 在 potassium hydroxide 作用下, 以 乙醇 为溶剂, 生成 2-(4-chlorophenylamino)ethanol参考文献:名称:Bis-aryl Urea Derivatives as Potent and Selective LIM Kinase (Limk) Inhibitors摘要:The discovery/optimization of bis-aryl ureas as Limk inhibitors to obtain high potency and selectivity and appropriate pharmacokinetic properties through systematic SAR studies is reported. Docking studies supported the observed SAR. Optimized Limk inhibitors had high biochemical potency (IC50 < 25 nM), excellent selectivity against ROCK and JNK kinases (>400-fold), potent inhibition of cofilin phosphorylation in A7r5, PC-3, and CEM-SS T cells (IC50 < 1 mu M), and good in vitro and in vivo pharmacokinetic properties. In the profiling against a panel of 61 kinases, compound 18b at 1 mu M inhibited only Limk1 and STK16 with >= 80% inhibition. Compounds 18b and 18f were highly efficient in inhibiting cell-invasion/migration in PC-3 cells. In addition, compound 18w was demonstrated to be effective on reducing intraocular pressure (IOP) on rat eyes. Taken together, these data demonstrated that we had developed a novel class of bis-aryl urea derived potent and selective Limk inhibitors.DOI:10.1021/jm501680m
-
作为产物:描述:1-chloro-2-(4-chloro-phenylcarbamoyloxy)-ethane 在 sodium ethanolate 作用下, 以 乙醇 为溶剂, 反应 1.0h, 生成 3-(4-chloro-phenyl)-oxazolidin-2-one参考文献:名称:2-恶唑烷酮的研究。I. 3-取代 2-恶唑烷酮的简便合成摘要:已经开发出一种从三种组分(脂肪族或芳香族胺、光气和乙烯氯醇)开始合成 3-取代 2-恶唑烷酮的方法。DOI:10.1246/bcsj.35.1309
文献信息
-
Synthesis of Oxazolidinones and Derivatives through Three-Component Fixation of Carbon Dioxide作者:Congmin Mei、Yibo Zhao、Qianwei Chen、Changsheng Cao、Guangsheng Pang、Yanhui ShiDOI:10.1002/cctc.201800142日期:2018.7.19three‐component fixation of atmospheric CO2 with readily available 1,2‐dichloroethane and aromatic amine toward oxazolidinones catalyzed by in situ NHC was developed. The reaction occurred in good to excellent yields with good generality and wide functional group tolerance, including challenging steric hindered substituted‐dichloroethane (e.g. 1,2‐dichloropropane and 2,3‐dichlorobutane). The catalytic system已经开发了一种有效的三组分固定方法,用现成的NHC催化的1,2-二氯乙烷和芳香族胺直接固定在恶唑烷酮上,以固定大气中的CO 2。该反应以良好的通用性和宽泛的官能团耐受性(包括具有挑战性的位阻取代的二氯乙烷(例如1,2-二氯丙烷和2,3-二氯丁烷))以良好的收率获得了良好的收率。该催化体系对空气和湿气不敏感,即使在约0.3atm的二氧化碳压力下也可获得高产率的恶唑烷酮。机理研究表明,该反应是通过NHC-CO 2原位催化NHC催化的加合物中,1-丁基-3-甲基咪唑-2-羧酸盐为中间体,而氨基氯化物参与反应路径。催化剂可以循环使用至少3次而不会明显降低催化活性。该协议还可以有效地制备六元3-芳基-1,3-氧杂嗪酮-2-一,甚至七元3-芳基-1,3-氧杂氮杂-2-酮,当1,3-二氯丙烷和1时使用了4-二氯丁烷。
-
Selective Synthesis of 5‐Substituted <i>N</i> ‐Aryloxazolidinones by Cycloaddition Reaction of Epoxides with Arylcarbamates Catalyzed by the Ionic Liquid BmimOAc作者:Elnazeer H. M. Elageed、Bihua Chen、Binshen Wang、Yongya Zhang、Shi Wu、Xiuli Liu、Guohua GaoDOI:10.1002/ejoc.201600474日期:2016.75-substituted N-aryloxazolidinones in excellent yields. In addition, chiral 5-substituted oxazolidinones were synthesized by this procedure in good-to-excellent yields with enantiomeric excesses in excess of 99.9 % starting from chiral terminal epoxides. A possible reaction mechanism is discussed in accord with the results obtained by 1H NMR spectroscopy and DFT calculations, which indicate the cooperative activation
-
Pd-Catalyzed Intermolecular Amidation of Aryl Halides: The Discovery that Xantphos Can Be Trans-Chelating in a Palladium Complex作者:Jingjun Yin、Stephen L. BuchwaldDOI:10.1021/ja012610k日期:2002.5.1A general method for the intermolecular coupling of aryl halides and amides using a Xantphos/Pd catalyst is described. This system displays good functional group compatibility, and the desired C-N bond forming process proceeds in good to excellent yields with 1-4 mol % of the Pd catalyst. Additionally, the arylation of sulfonamides, oxazolidinones, and ureas is reported. The efficiency of these transformations
-
A One-Pot Synthesis of <i>N</i> -Aryl-2-Oxazolidinones and Cyclic Urethanes by the Lewis Base Catalyzed Fixation of Carbon Dioxide into Anilines and Bromoalkanes作者:Teemu Niemi、Jesus E. Perea-Buceta、Israel Fernández、Otto-Matti Hiltunen、Vili Salo、Sari Rautiainen、Minna T. Räisänen、Timo RepoDOI:10.1002/chem.201602338日期:2016.7.18catalytic amounts of an organosuperbase such as Barton's base enables this transformation to proceed with high yields and exquisite substrate functional‐group tolerance under ambient CO2 pressure and mild temperature. This report also provides the first proof‐of‐principle for the single‐operation synthesis of elusive seven‐membered ring cyclic urethanes.
-
Late-stage oxidative C(sp3)–H methylation作者:Kaibo Feng、Raundi E. Quevedo、Jeffrey T. Kohrt、Martins S. Oderinde、Usa Reilly、M. Christina WhiteDOI:10.1038/s41586-020-2137-8日期:2020.4.30molecules1,2,3. However, existing methylation methods show limited scope and have not been demonstrated in complex settings1. Here we report a regioselective and chemoselective oxidative C(sp3)–H methylation method that is compatible with late-stage functionalization of drug scaffolds and natural products. This combines a highly site-selective and chemoselective C–H hydroxylation with a mild, functional-group-tolerant通常被称为“神奇的甲基效应”,甲基基团的安装——尤其是与杂原子相邻的 (α)——已被证明可以显着提高生物活性分子1,2,3的效力。然而,现有的甲基化方法显示范围有限,尚未在复杂环境中得到证实1。在这里,我们报告了一种区域选择性和化学选择性氧化 C( sp 3 )-H 甲基化方法,该方法与药物支架和天然产物的后期功能化兼容。这结合了高度位点选择性和化学选择性的 C-H 羟基化与温和的、官能团耐受的甲基化。使用小分子锰催化剂,Mn(CF 3PDP),在低负载(底物/催化剂比率为 200)下,在杂环核上提供靶向 C-H 羟基化,同时保留电子中性和富电子芳基。氟或路易斯酸辅助形成反应性亚胺或氧鎓中间体使得能够使用温和亲核的有机铝甲基化试剂,该试剂在基底上保留其他亲电子功能。我们展示了这个后期 C( sp 3)–H 甲基化在 41 个底物上,包含 16 个不同的药用重要核心,包括富电子芳基、杂环、羰
表征谱图
-
氢谱1HNMR
-
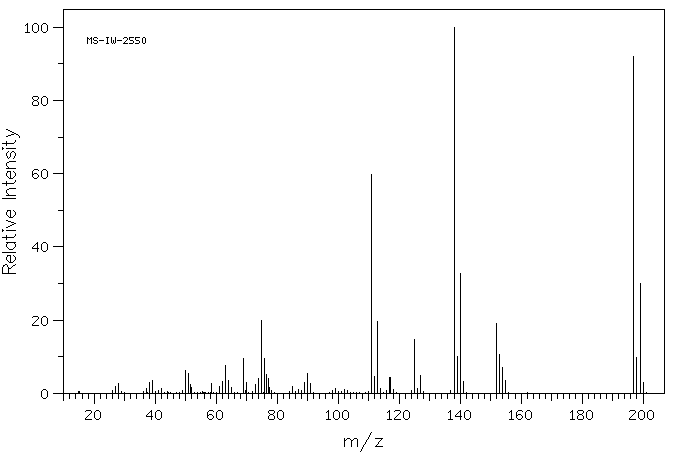
质谱MS
-
碳谱13CNMR
-
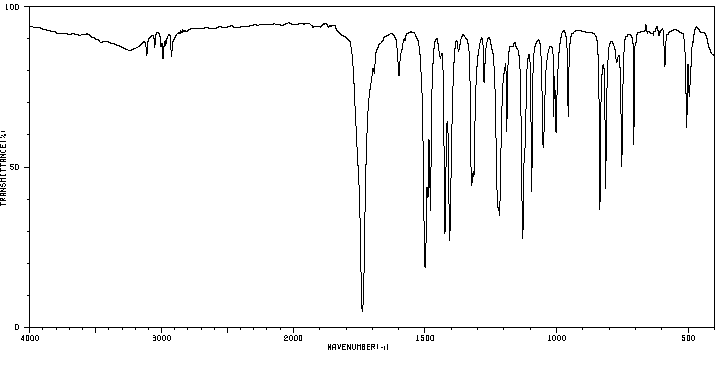
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息
同类化合物
(βS)-β-氨基-4-(4-羟基苯氧基)-3,5-二碘苯甲丙醇
(S,S)-邻甲苯基-DIPAMP
(S)-(-)-7'-〔4(S)-(苄基)恶唑-2-基]-7-二(3,5-二-叔丁基苯基)膦基-2,2',3,3'-四氢-1,1-螺二氢茚
(S)-盐酸沙丁胺醇
(S)-3-(叔丁基)-4-(2,6-二甲氧基苯基)-2,3-二氢苯并[d][1,3]氧磷杂环戊二烯
(S)-2,2'-双[双(3,5-三氟甲基苯基)膦基]-4,4',6,6'-四甲氧基联苯
(S)-1-[3,5-双(三氟甲基)苯基]-3-[1-(二甲基氨基)-3-甲基丁烷-2-基]硫脲
(R)富马酸托特罗定
(R)-(-)-盐酸尼古地平
(R)-(-)-4,12-双(二苯基膦基)[2.2]对环芳烷(1,5环辛二烯)铑(I)四氟硼酸盐
(R)-(+)-7-双(3,5-二叔丁基苯基)膦基7''-[((6-甲基吡啶-2-基甲基)氨基]-2,2'',3,3''-四氢-1,1''-螺双茚满
(R)-(+)-7-双(3,5-二叔丁基苯基)膦基7''-[(4-叔丁基吡啶-2-基甲基)氨基]-2,2'',3,3''-四氢-1,1''-螺双茚满
(R)-(+)-7-双(3,5-二叔丁基苯基)膦基7''-[(3-甲基吡啶-2-基甲基)氨基]-2,2'',3,3''-四氢-1,1''-螺双茚满
(R)-(+)-4,7-双(3,5-二-叔丁基苯基)膦基-7“-[(吡啶-2-基甲基)氨基]-2,2”,3,3'-四氢1,1'-螺二茚满
(R)-3-(叔丁基)-4-(2,6-二苯氧基苯基)-2,3-二氢苯并[d][1,3]氧杂磷杂环戊烯
(R)-2-[((二苯基膦基)甲基]吡咯烷
(R)-1-[3,5-双(三氟甲基)苯基]-3-[1-(二甲基氨基)-3-甲基丁烷-2-基]硫脲
(N-(4-甲氧基苯基)-N-甲基-3-(1-哌啶基)丙-2-烯酰胺)
(5-溴-2-羟基苯基)-4-氯苯甲酮
(5-溴-2-氯苯基)(4-羟基苯基)甲酮
(5-氧代-3-苯基-2,5-二氢-1,2,3,4-oxatriazol-3-鎓)
(4S,5R)-4-甲基-5-苯基-1,2,3-氧代噻唑烷-2,2-二氧化物-3-羧酸叔丁酯
(4S,4''S)-2,2''-亚环戊基双[4,5-二氢-4-(苯甲基)恶唑]
(4-溴苯基)-[2-氟-4-[6-[甲基(丙-2-烯基)氨基]己氧基]苯基]甲酮
(4-丁氧基苯甲基)三苯基溴化磷
(3aR,8aR)-(-)-4,4,8,8-四(3,5-二甲基苯基)四氢-2,2-二甲基-6-苯基-1,3-二氧戊环[4,5-e]二恶唑磷
(3aR,6aS)-5-氧代六氢环戊基[c]吡咯-2(1H)-羧酸酯
(2Z)-3-[[(4-氯苯基)氨基]-2-氰基丙烯酸乙酯
(2S,3S,5S)-5-(叔丁氧基甲酰氨基)-2-(N-5-噻唑基-甲氧羰基)氨基-1,6-二苯基-3-羟基己烷
(2S,2''S,3S,3''S)-3,3''-二叔丁基-4,4''-双(2,6-二甲氧基苯基)-2,2'',3,3''-四氢-2,2''-联苯并[d][1,3]氧杂磷杂戊环
(2S)-(-)-2-{[[[[3,5-双(氟代甲基)苯基]氨基]硫代甲基]氨基}-N-(二苯基甲基)-N,3,3-三甲基丁酰胺
(2S)-2-[[[[[((1S,2S)-2-氨基环己基]氨基]硫代甲基]氨基]-N-(二苯甲基)-N,3,3-三甲基丁酰胺
(2S)-2-[[[[[[((1R,2R)-2-氨基环己基]氨基]硫代甲基]氨基]-N-(二苯甲基)-N,3,3-三甲基丁酰胺
(2-硝基苯基)磷酸三酰胺
(2,6-二氯苯基)乙酰氯
(2,3-二甲氧基-5-甲基苯基)硼酸
(1S,2S,3S,5S)-5-叠氮基-3-(苯基甲氧基)-2-[(苯基甲氧基)甲基]环戊醇
(1S,2S,3R,5R)-2-(苄氧基)甲基-6-氧杂双环[3.1.0]己-3-醇
(1-(4-氟苯基)环丙基)甲胺盐酸盐
(1-(3-溴苯基)环丁基)甲胺盐酸盐
(1-(2-氯苯基)环丁基)甲胺盐酸盐
(1-(2-氟苯基)环丙基)甲胺盐酸盐
(1-(2,6-二氟苯基)环丙基)甲胺盐酸盐
(-)-去甲基西布曲明
龙蒿油
龙胆酸钠
龙胆酸叔丁酯
龙胆酸
龙胆紫-d6
龙胆紫