3-苄基唑烷 | 13657-16-4
中文名称
3-苄基唑烷
中文别名
3-苄基恶唑烷;3-(苯甲基)唑烷
英文名称
3-benzyl-1,3-oxazolidine
英文别名
3-Benzyloxazolidine
CAS
13657-16-4
化学式
C10H13NO
mdl
MFCD00059028
分子量
163.219
InChiKey
FQNODHUYZYLTPN-UHFFFAOYSA-N
BEILSTEIN
——
EINECS
——
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
物化性质
-
沸点:127 °C / 18mmHg
-
密度:1,07 g/cm3
计算性质
-
辛醇/水分配系数(LogP):1.7
-
重原子数:12
-
可旋转键数:2
-
环数:2.0
-
sp3杂化的碳原子比例:0.4
-
拓扑面积:12.5
-
氢给体数:0
-
氢受体数:2
安全信息
-
WGK Germany:3
-
安全说明:S26,S36/37/39
-
危险标志:GHS07
-
危险类别码:R36/37/38
-
危险性描述:H302
-
海关编码:2934999090
SDS
3-苄基恶唑烷 修改号码:5
模块 1. 化学品
产品名称: 3-Benzyloxazolidine
修改号码: 5
模块 2. 危险性概述
GHS分类
物理性危害 未分类
健康危害 未分类
环境危害 未分类
GHS标签元素
图标或危害标志 无
信号词 无信号词
危险描述 无
防范说明 无
模块 3. 成分/组成信息
单一物质/混和物 单一物质
化学名(中文名): 3-苄基恶唑烷
百分比: >98.0%(GC)(T)
CAS编码: 13657-16-4
分子式: C10H13NO
模块 4. 急救措施
吸入: 将受害者移到新鲜空气处,保持呼吸通畅,休息。若感不适请求医/就诊。
皮肤接触: 立即去除/脱掉所有被污染的衣物。用水清洗皮肤/淋浴。
若皮肤刺激或发生皮疹:求医/就诊。
眼睛接触: 用水小心清洗几分钟。如果方便,易操作,摘除隐形眼镜。继续清洗。
如果眼睛刺激:求医/就诊。
食入: 若感不适,求医/就诊。漱口。
紧急救助者的防护: 救援者需要穿戴个人防护用品,比如橡胶手套和气密性护目镜。
模块 5. 消防措施
合适的灭火剂: 干粉,泡沫,雾状水,二氧化碳
不适用的灭火剂: 棒状水
特殊危险性: 小心,燃烧或高温下可能分解产生毒烟。
3-苄基恶唑烷 修改号码:5
模块 5. 消防措施
特定方法: 从上风处灭火,根据周围环境选择合适的灭火方法。
非相关人员应该撤离至安全地方。
周围一旦着火:如果安全,移去可移动容器。
消防员的特殊防护用具: 灭火时,一定要穿戴个人防护用品。
模块 6. 泄漏应急处理
个人防护措施,防护用具, 使用个人防护用品。远离溢出物/泄露处并处在上风处。确保足够通风。
紧急措施: 泄露区应该用安全带等圈起来,控制非相关人员进入。
环保措施: 防止进入下水道。
控制和清洗的方法和材料: 用合适的吸收剂(如:旧布,干砂,土,锯屑)吸收泄漏物。一旦大量泄漏,筑堤控
制。附着物或收集物应该立即根据合适的法律法规废弃处置。
模块 7. 操作处置与储存
处理
技术措施: 在通风良好处进行处理。穿戴合适的防护用具。防止烟雾产生。处理后彻底清洗双手
和脸。
注意事项: 如果蒸气或浮质产生,使用通风、局部排气。
操作处置注意事项: 避免接触皮肤、眼睛和衣物。
贮存
储存条件: 保持容器密闭。存放于凉爽、阴暗处。
存放于惰性气体环境中。
远离不相容的材料比如氧化剂存放。
气敏
包装材料: 依据法律。
模块 8. 接触控制和个体防护
工程控制: 尽可能安装封闭体系或局部排风系统,操作人员切勿直接接触。同时安装淋浴器和洗
眼器。
个人防护用品
呼吸系统防护: 防毒面具。依据当地和政府法规。
手部防护: 防护手套。
眼睛防护: 安全防护镜。如果情况需要,佩戴面具。
皮肤和身体防护: 防护服。如果情况需要,穿戴防护靴。
模块 9. 理化特性
液体
外形(20°C):
外观: 透明
颜色: 极淡的黄色-浅黄色
气味: 无资料
pH: 无数据资料
熔点: 无资料
沸点/沸程 127 °C/2.4kPa
闪点: 无资料
爆炸特性
爆炸下限: 无资料
爆炸上限: 无资料
密度: 1.07
溶解度:
[水] 无资料
3-苄基恶唑烷 修改号码:5
模块 9. 理化特性
[其他溶剂] 无资料
模块 10. 稳定性和反应性
化学稳定性: 一般情况下稳定。
危险反应的可能性: 未报道特殊反应性。
须避免接触的物质 氧化剂
危险的分解产物: 一氧化碳, 二氧化碳, 氮氧化物 (NOx)
模块 11. 毒理学信息
急性毒性: 无资料
对皮肤腐蚀或刺激: 无资料
对眼睛严重损害或刺激: 无资料
生殖细胞变异原性: 无资料
致癌性:
IARC = 无资料
NTP = 无资料
生殖毒性: 无资料
模块 12. 生态学信息
生态毒性:
鱼类: 无资料
甲壳类: 无资料
藻类: 无资料
残留性 / 降解性: 无资料
潜在生物累积 (BCF): 无资料
土壤中移动性
log水分配系数: 无资料
土壤吸收系数 (Koc): 无资料
亨利定律 无资料
constaNT(PaM3/mol):
模块 13. 废弃处置
如果可能,回收处理。请咨询当地管理部门。建议在装有后燃和洗涤装置的化学焚烧炉中焚烧。废弃处置时请遵守
国家、地区和当地的所有法规。
模块 14. 运输信息
联合国分类: 与联合国分类标准不一致
UN编号: 未列明
模块 15. 法规信息
《危险化学品安全管理条例》(2002年1月26日国务院发布,2011年2月16日修订): 针对危险化学品的安全使用、
生产、储存、运输、装卸等方面均作了相应的规定。
3-苄基恶唑烷 修改号码:5
模块16 - 其他信息
N/A
模块 1. 化学品
产品名称: 3-Benzyloxazolidine
修改号码: 5
模块 2. 危险性概述
GHS分类
物理性危害 未分类
健康危害 未分类
环境危害 未分类
GHS标签元素
图标或危害标志 无
信号词 无信号词
危险描述 无
防范说明 无
模块 3. 成分/组成信息
单一物质/混和物 单一物质
化学名(中文名): 3-苄基恶唑烷
百分比: >98.0%(GC)(T)
CAS编码: 13657-16-4
分子式: C10H13NO
模块 4. 急救措施
吸入: 将受害者移到新鲜空气处,保持呼吸通畅,休息。若感不适请求医/就诊。
皮肤接触: 立即去除/脱掉所有被污染的衣物。用水清洗皮肤/淋浴。
若皮肤刺激或发生皮疹:求医/就诊。
眼睛接触: 用水小心清洗几分钟。如果方便,易操作,摘除隐形眼镜。继续清洗。
如果眼睛刺激:求医/就诊。
食入: 若感不适,求医/就诊。漱口。
紧急救助者的防护: 救援者需要穿戴个人防护用品,比如橡胶手套和气密性护目镜。
模块 5. 消防措施
合适的灭火剂: 干粉,泡沫,雾状水,二氧化碳
不适用的灭火剂: 棒状水
特殊危险性: 小心,燃烧或高温下可能分解产生毒烟。
3-苄基恶唑烷 修改号码:5
模块 5. 消防措施
特定方法: 从上风处灭火,根据周围环境选择合适的灭火方法。
非相关人员应该撤离至安全地方。
周围一旦着火:如果安全,移去可移动容器。
消防员的特殊防护用具: 灭火时,一定要穿戴个人防护用品。
模块 6. 泄漏应急处理
个人防护措施,防护用具, 使用个人防护用品。远离溢出物/泄露处并处在上风处。确保足够通风。
紧急措施: 泄露区应该用安全带等圈起来,控制非相关人员进入。
环保措施: 防止进入下水道。
控制和清洗的方法和材料: 用合适的吸收剂(如:旧布,干砂,土,锯屑)吸收泄漏物。一旦大量泄漏,筑堤控
制。附着物或收集物应该立即根据合适的法律法规废弃处置。
模块 7. 操作处置与储存
处理
技术措施: 在通风良好处进行处理。穿戴合适的防护用具。防止烟雾产生。处理后彻底清洗双手
和脸。
注意事项: 如果蒸气或浮质产生,使用通风、局部排气。
操作处置注意事项: 避免接触皮肤、眼睛和衣物。
贮存
储存条件: 保持容器密闭。存放于凉爽、阴暗处。
存放于惰性气体环境中。
远离不相容的材料比如氧化剂存放。
气敏
包装材料: 依据法律。
模块 8. 接触控制和个体防护
工程控制: 尽可能安装封闭体系或局部排风系统,操作人员切勿直接接触。同时安装淋浴器和洗
眼器。
个人防护用品
呼吸系统防护: 防毒面具。依据当地和政府法规。
手部防护: 防护手套。
眼睛防护: 安全防护镜。如果情况需要,佩戴面具。
皮肤和身体防护: 防护服。如果情况需要,穿戴防护靴。
模块 9. 理化特性
液体
外形(20°C):
外观: 透明
颜色: 极淡的黄色-浅黄色
气味: 无资料
pH: 无数据资料
熔点: 无资料
沸点/沸程 127 °C/2.4kPa
闪点: 无资料
爆炸特性
爆炸下限: 无资料
爆炸上限: 无资料
密度: 1.07
溶解度:
[水] 无资料
3-苄基恶唑烷 修改号码:5
模块 9. 理化特性
[其他溶剂] 无资料
模块 10. 稳定性和反应性
化学稳定性: 一般情况下稳定。
危险反应的可能性: 未报道特殊反应性。
须避免接触的物质 氧化剂
危险的分解产物: 一氧化碳, 二氧化碳, 氮氧化物 (NOx)
模块 11. 毒理学信息
急性毒性: 无资料
对皮肤腐蚀或刺激: 无资料
对眼睛严重损害或刺激: 无资料
生殖细胞变异原性: 无资料
致癌性:
IARC = 无资料
NTP = 无资料
生殖毒性: 无资料
模块 12. 生态学信息
生态毒性:
鱼类: 无资料
甲壳类: 无资料
藻类: 无资料
残留性 / 降解性: 无资料
潜在生物累积 (BCF): 无资料
土壤中移动性
log水分配系数: 无资料
土壤吸收系数 (Koc): 无资料
亨利定律 无资料
constaNT(PaM3/mol):
模块 13. 废弃处置
如果可能,回收处理。请咨询当地管理部门。建议在装有后燃和洗涤装置的化学焚烧炉中焚烧。废弃处置时请遵守
国家、地区和当地的所有法规。
模块 14. 运输信息
联合国分类: 与联合国分类标准不一致
UN编号: 未列明
模块 15. 法规信息
《危险化学品安全管理条例》(2002年1月26日国务院发布,2011年2月16日修订): 针对危险化学品的安全使用、
生产、储存、运输、装卸等方面均作了相应的规定。
3-苄基恶唑烷 修改号码:5
模块16 - 其他信息
N/A
上下游信息
-
上游原料
中文名称 英文名称 CAS号 化学式 分子量 N-甲基-N-羟乙基苄胺 2-(N-benzyl-N-methyl)amino-1-ethanol 101-98-4 C10H15NO 165.235 N-苄基乙醇胺 N-Benzylethanolamine 104-63-2 C9H13NO 151.208 -
下游产品
中文名称 英文名称 CAS号 化学式 分子量 N-甲基-N-羟乙基苄胺 2-(N-benzyl-N-methyl)amino-1-ethanol 101-98-4 C10H15NO 165.235
反应信息
-
作为反应物:描述:3-苄基唑烷 在 [,14-bis(diphenylphosphino)butane] (1,5-cyclooctadiene)rhodium(I) tetrafluoroborate 氢气 作用下, 以 甲醇 为溶剂, 20.0 ℃ 、5.2 MPa 条件下, 反应 3.0h, 生成 N-甲基-N-羟乙基苄胺参考文献:名称:环状N,O-缩醛均相催化氢解合成N-(二烷基氨基烷基)醇摘要:据报道,1,3-恶唑烷的均相催化氢化得到不对称取代的 2-N-(二烷基氨基)乙醇,这首次表明基于螯合二膦的 Rh(I) 催化剂可能对该反应有利。DOI:10.1055/s-2002-20039
-
作为产物:描述:参考文献:名称:Use of N-[(trimethylsilyl)methyl]amino ethers as capped azomethine ylide equivalents摘要:DOI:10.1021/jo00378a013
-
作为试剂:描述:利卡灵A 、 3-苄基唑烷 在 3-苄基唑烷 作用下, 以 乙醇 为溶剂, 反应 48.0h, 以there is obtained 17.2 g of N-(5-(trans-2,3-dihydro-7-methoxy-3-methyl-5-(E)-propenyl-benzofuran-2-yl)-2-hydroxy-3-methoxy-phenylmethyl)-N-(2-hydroxyethyl)-N-benzylamine的产率得到N-(5-(trans-2,3-dihydro-7-methoxy-3-methyl-5-(E)-propenyl-benzofuran-2-yl)-2-hydroxy-3-methoxy-phenylmethyl)-N-(2-hydroxyethyl)-N-benzylamine参考文献:名称:Process for making derivatives of dimers of isoeugenol摘要:式子为##STR1##的化合物具有保护肝脏的性质。它们是通过将脱氢异丁香酚或二异丁香酚与式子为##STR2##的噁唑烷反应制备的。公开号:US04256764A1
文献信息
-
Direct synthesis of N-substituted 1,3-oxazolidines via a hetero-domino Petasis borono-Mannich reaction of 1,2-amino alcohols, formaldehyde, and organoboronic acids作者:Yiting Zheng、Lu Sun、Jiayi Wang、Gonghua SongDOI:10.1007/s10593-019-02511-8日期:2019.7A simple and convenient approach to the synthesis of N-substituted 1,3-oxazolidines via a hetero-domino Petasis borono-Mannich reaction of 1,2-amino alcohols, formaldehyde, and organoboronic acids has been reported. The transformation provides an effective and complementary pathway toward 1,3-oxazolidine derivatives.
-
Efficient Synthesis of NK<sub>1</sub> Receptor Antagonist Aprepitant Using a Crystallization-Induced Diastereoselective Transformation作者:Karel M. J. Brands、Joseph F. Payack、Jonathan D. Rosen、Todd D. Nelson、Alexander Candelario、Mark A. Huffman、Matthew M. Zhao、Jing Li、Bridgette Craig、Zhiguo J. Song、David M. Tschaen、Karl Hansen、Paul N. Devine、Philip J. Pye、Kai Rossen、Peter G. Dormer、Robert A. Reamer、Christopher J. Welch、David J. Mathre、Nancy N. Tsou、James M. McNamara、Paul J. ReiderDOI:10.1021/ja027458g日期:2003.2.1efficient stereoselective synthesis of the orally active NK(1) receptor antagonist Aprepitant is described. A direct condensation of N-benzyl ethanolamine with glyoxylic acid yielded a 2-hydroxy-1,4-oxazin-3-one which was activated as the corresponding trifluoroacetate. A Lewis acid mediated coupling with enantiopure (R)-1-(3,5-bis(trifluoromethyl)phenyl)ethan-1-ol afforded a 1:1 mixture of acetal diastereomers描述了口服活性 NK(1) 受体拮抗剂阿瑞匹坦的有效立体选择性合成。N-苄基乙醇胺与乙醛酸的直接缩合产生 2-羟基-1,4-恶嗪-3-酮,其被活化为相应的三氟乙酸酯。路易斯酸介导的与对映体纯 (R)-1-(3,5-双(三氟甲基)苯基)乙-1-醇的偶联提供了缩醛非对映异构体的 1:1 混合物,该混合物通过新型结晶转化为单一异构体-诱导不对称转变。所得 1,4-oxazin-3-one 通过独特且高度立体选择性的一锅法转化为所需的 α-(氟苯基)吗啉衍生物。在这些关键步骤的优化过程中,发现了有趣且出乎意料的 [1,2]-Wittig 和 [1,3]-sigmatropic 重排。在最后一步,三唑啉酮侧链附加到吗啉核心。因此,在最长的线性序列中以 55% 的总产率获得了靶向临床候选物。
-
Nucleophilic ring opening of tetrahydro-1,3-oxazines and 1,3-oxazolidines by alkynyl anions: A novel synthesis of β-aminoacetylenes作者:Ming-Jung Wu、Der-Shenq Yan、Hui-Wen Tsai、Shu-Hui ChenDOI:10.1016/s0040-4039(00)73304-1日期:1994.7The reaction of alkynyl boranes, generated in situ from lithium acetylides and boron trifluoride etherate, with 3-benzyl-tetrahydro-1,3-oxazines and 1,3-oxazolidines gave the corresponding β-aminoacetylenes in modest to good yield. By the employment of titanium acetylides to the same reaction provided comparable results.
-
Cyclische Aldehydderivate als Alkylierungsreagenzien, 1. Mitt. Acyclo- und Azaacycloanaloga von Nucleosiden作者:Herfried Griengl、Walter Hayden、Elke Schindler、Erich WanekDOI:10.1002/ardp.19833160211日期:——Ringöffnung von 1,3‐Dioxolan und von 3‐Alkyl‐1,3‐oxazolidinen mit Acetylchlorid oder Trimethyliodsilan führt zu den α‐Halogenethern 2a—2e. Diese stellen Alkylierungsreagenzien dar. Ihre Umsetzung mit Adenin, 6‐Chlorpurin oder silyliertem Cytosin bzw. silylierten Uracilderivaten gibt die 2‐Hydroxyethoxymethyl‐ bzw. 2‐Acetamidoethoxymethylverbindungen 4, 5 und 7..
-
Electrooxidative Cyclization of Hydroxyamino Compounds Possessing a Benzyl Group作者:Mitsuhiro Okimoto、Kousuke Ohashi、Haruki Yamamori、Shinnosuke Nishikawa、Masayuki Hoshi、Takashi YoshidaDOI:10.1055/s-0031-1290755日期:2012.53-oxazinane derivatives using only a small excess of base. Several novel 2-aryl-1,3-oxazinane and 2-aryl-1,3-oxazolidine derivatives were synthesized from N-benzyl-2-piperidineethanols and N-benzyl-2-piperidinemethanols, respectively, by using electrooxidative methods in methanol. For these reactions, the yields of the corresponding cyclized compounds were significantly increased by using catalytic amounts摘要 通过在甲醇中使用电氧化法,分别从N-苄基-2-哌啶甲醇和N-苄基-2-哌啶甲醇合成了几种新颖的2-芳基-1,3-恶嗪烷和2-芳基-1,3-恶唑烷衍生物。对于这些反应,通过使用催化量的碘离子显着提高了相应环化化合物的产率。相反,3-二烷基氨基-1-苯基丙醇仅使用少量过量的碱即可得到预期的环状6-苯基-1,3-恶嗪烷衍生物。 通过在甲醇中使用电氧化法,分别从N-苄基-2-哌啶甲醇和N-苄基-2-哌啶甲醇合成了几种新颖的2-芳基-1,3-恶嗪烷和2-芳基-1,3-恶唑烷衍生物。对于这些反应,通过使用催化量的碘离子显着提高了相应环化化合物的产率。相反,3-二烷基氨基-1-苯基丙醇仅使用少量过量的碱即可得到预期的环状6-苯基-1,3-恶嗪烷衍生物。
表征谱图
-
氢谱1HNMR
-
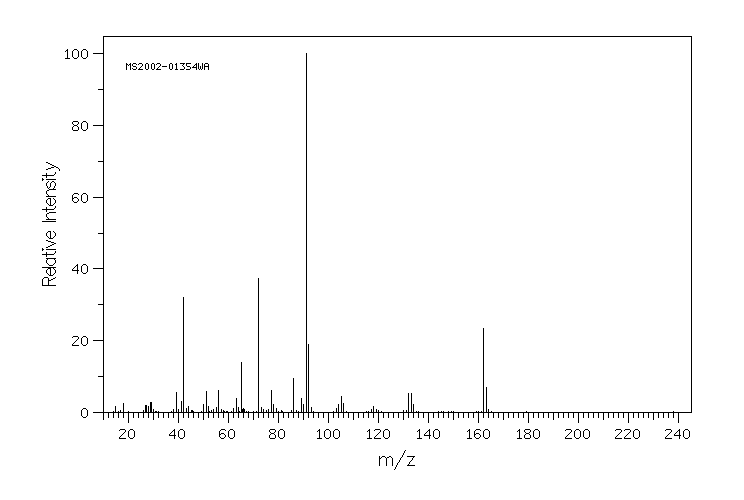
质谱MS
-
碳谱13CNMR
-
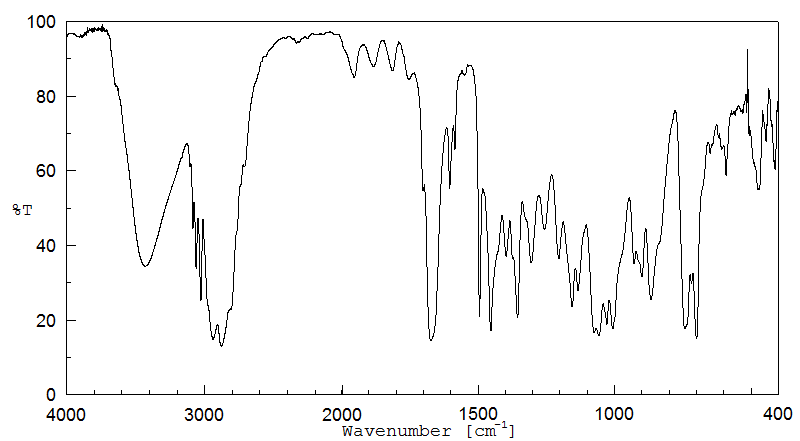
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息
同类化合物
(βS)-β-氨基-4-(4-羟基苯氧基)-3,5-二碘苯甲丙醇
(S,S)-邻甲苯基-DIPAMP
(S)-(-)-7'-〔4(S)-(苄基)恶唑-2-基]-7-二(3,5-二-叔丁基苯基)膦基-2,2',3,3'-四氢-1,1-螺二氢茚
(S)-盐酸沙丁胺醇
(S)-3-(叔丁基)-4-(2,6-二甲氧基苯基)-2,3-二氢苯并[d][1,3]氧磷杂环戊二烯
(S)-2,2'-双[双(3,5-三氟甲基苯基)膦基]-4,4',6,6'-四甲氧基联苯
(S)-1-[3,5-双(三氟甲基)苯基]-3-[1-(二甲基氨基)-3-甲基丁烷-2-基]硫脲
(R)富马酸托特罗定
(R)-(-)-盐酸尼古地平
(R)-(-)-4,12-双(二苯基膦基)[2.2]对环芳烷(1,5环辛二烯)铑(I)四氟硼酸盐
(R)-(+)-7-双(3,5-二叔丁基苯基)膦基7''-[((6-甲基吡啶-2-基甲基)氨基]-2,2'',3,3''-四氢-1,1''-螺双茚满
(R)-(+)-7-双(3,5-二叔丁基苯基)膦基7''-[(4-叔丁基吡啶-2-基甲基)氨基]-2,2'',3,3''-四氢-1,1''-螺双茚满
(R)-(+)-7-双(3,5-二叔丁基苯基)膦基7''-[(3-甲基吡啶-2-基甲基)氨基]-2,2'',3,3''-四氢-1,1''-螺双茚满
(R)-(+)-4,7-双(3,5-二-叔丁基苯基)膦基-7“-[(吡啶-2-基甲基)氨基]-2,2”,3,3'-四氢1,1'-螺二茚满
(R)-3-(叔丁基)-4-(2,6-二苯氧基苯基)-2,3-二氢苯并[d][1,3]氧杂磷杂环戊烯
(R)-2-[((二苯基膦基)甲基]吡咯烷
(R)-1-[3,5-双(三氟甲基)苯基]-3-[1-(二甲基氨基)-3-甲基丁烷-2-基]硫脲
(N-(4-甲氧基苯基)-N-甲基-3-(1-哌啶基)丙-2-烯酰胺)
(5-溴-2-羟基苯基)-4-氯苯甲酮
(5-溴-2-氯苯基)(4-羟基苯基)甲酮
(5-氧代-3-苯基-2,5-二氢-1,2,3,4-oxatriazol-3-鎓)
(4S,5R)-4-甲基-5-苯基-1,2,3-氧代噻唑烷-2,2-二氧化物-3-羧酸叔丁酯
(4S,4''S)-2,2''-亚环戊基双[4,5-二氢-4-(苯甲基)恶唑]
(4-溴苯基)-[2-氟-4-[6-[甲基(丙-2-烯基)氨基]己氧基]苯基]甲酮
(4-丁氧基苯甲基)三苯基溴化磷
(3aR,8aR)-(-)-4,4,8,8-四(3,5-二甲基苯基)四氢-2,2-二甲基-6-苯基-1,3-二氧戊环[4,5-e]二恶唑磷
(3aR,6aS)-5-氧代六氢环戊基[c]吡咯-2(1H)-羧酸酯
(2Z)-3-[[(4-氯苯基)氨基]-2-氰基丙烯酸乙酯
(2S,3S,5S)-5-(叔丁氧基甲酰氨基)-2-(N-5-噻唑基-甲氧羰基)氨基-1,6-二苯基-3-羟基己烷
(2S,2''S,3S,3''S)-3,3''-二叔丁基-4,4''-双(2,6-二甲氧基苯基)-2,2'',3,3''-四氢-2,2''-联苯并[d][1,3]氧杂磷杂戊环
(2S)-(-)-2-{[[[[3,5-双(氟代甲基)苯基]氨基]硫代甲基]氨基}-N-(二苯基甲基)-N,3,3-三甲基丁酰胺
(2S)-2-[[[[[((1S,2S)-2-氨基环己基]氨基]硫代甲基]氨基]-N-(二苯甲基)-N,3,3-三甲基丁酰胺
(2S)-2-[[[[[[((1R,2R)-2-氨基环己基]氨基]硫代甲基]氨基]-N-(二苯甲基)-N,3,3-三甲基丁酰胺
(2-硝基苯基)磷酸三酰胺
(2,6-二氯苯基)乙酰氯
(2,3-二甲氧基-5-甲基苯基)硼酸
(1S,2S,3S,5S)-5-叠氮基-3-(苯基甲氧基)-2-[(苯基甲氧基)甲基]环戊醇
(1S,2S,3R,5R)-2-(苄氧基)甲基-6-氧杂双环[3.1.0]己-3-醇
(1-(4-氟苯基)环丙基)甲胺盐酸盐
(1-(3-溴苯基)环丁基)甲胺盐酸盐
(1-(2-氯苯基)环丁基)甲胺盐酸盐
(1-(2-氟苯基)环丙基)甲胺盐酸盐
(1-(2,6-二氟苯基)环丙基)甲胺盐酸盐
(-)-去甲基西布曲明
龙蒿油
龙胆酸钠
龙胆酸叔丁酯
龙胆酸
龙胆紫-d6
龙胆紫