2-ketoisovalerate | 2507-77-9
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
计算性质
-
辛醇/水分配系数(LogP):1.4
-
重原子数:8
-
可旋转键数:1
-
环数:0.0
-
sp3杂化的碳原子比例:0.6
-
拓扑面积:57.2
-
氢给体数:0
-
氢受体数:3
反应信息
-
作为反应物:描述:2-ketoisovalerate 在 1,6-di-o-phosphonohex-2-ulofuranose 、 piperazine*HCl buffer 、 还原型辅酶Ⅰ 作用下, 生成 2-羟基-3-甲基丁酸参考文献:名称:Gln102Arg和Cys97Gly突变对嗜热脂肪芽孢杆菌L-乳酸脱氢酶结构特异性和立体特异性的影响摘要:嗜热脂肪芽孢杆菌 (BSLDH) 的 L-乳酸脱氢酶是一种热稳定酶,在不对称合成中具有相当大的应用潜力。因此,了解控制其结构特异性和立体特异性的因素是很有意义的。本文评估了 GIn 102→Arg 和 Cys97→Gly 突变的影响。在对 13 种 2-酮酸的调查中,发现 Q102R 突变降低了 BSLDH 还原具有小或亲水 R 基团的 RCOCOOH 底物的活性,而不影响其对具有较大疏水性 R 取代基的那些的活性DOI:10.1021/ja00038a016
-
作为产物:参考文献:名称:Skopan, Haike; Guenther, Helmut; Simon, Helmut, Angewandte Chemie, 1987, vol. 99, # 2, p. 139 - 141摘要:DOI:
文献信息
-
Donor Promiscuity of a Thermostable Transketolase by Directed Evolution: Efficient Complementation of 1-Deoxy-<scp>d</scp> -xylulose-5-phosphate Synthase Activity作者:Thangavelu Saravanan、Sebastian Junker、Michael Kickstein、Sascha Hein、Marie-Kristin Link、Jan Ranglack、Samantha Witt、Marion Lorillière、Laurence Hecquet、Wolf-Dieter FessnerDOI:10.1002/anie.201701169日期:2017.5.2Enzymes catalyzing asymmetric carboligation reactions typically show very high substrate specificity for their nucleophilic donor substrate components. Structure‐guided engineering of the thermostable transketolase from Geobacillus stearothermophilus by directed in vitro evolution yielded new enzyme variants that are able to utilize pyruvate and higher aliphatic homologues as nucleophilic components
-
Thermodynamics of reactions catalysed by branched-chain-amino-acid transaminase作者:Yadu B. Tewari、Robert N. Goldberg、J.David RozzellDOI:10.1006/jcht.2000.0686日期:2000.10Abstract Apparent equilibrium constants and calorimetric enthalpies of reaction have been measured for reactions catalysed by branched-chain-amino-acid transaminase. The following biochemical reactions have been studied at the temperature 298.15 K and in the pH range (7.15 to 7.24):l-valine(aq) + 2-oxoglutarate(aq) = 2-oxoisovalerate(aq) + l-glutamate(aq);l-leucine(aq) + 2-oxoglutarate(aq) = 2-oxoisocaproate(aq)摘要 测量了支链氨基酸转氨酶催化反应的表观平衡常数和反应热焓。在温度 298.15 K 和 pH 范围(7.15 至 7.24)下研究了以下生化反应:l-缬氨酸(aq)+ 2-氧代戊二酸(aq)= 2-氧代异戊酸(aq)+ l-谷氨酸(aq) ;l-亮氨酸(aq) + 2-氧代戊二酸(aq) = 2-氧代异己酸(aq) + l-谷氨酸(aq); 和叔-亮氨酸(aq) + 2-氧代戊二酸(aq) = 3,3-二甲基-2-氧代丁酸(aq) + l-谷氨酸(aq)。结果已用于计算涉及特定物种的参考反应的平衡常数和标准摩尔焓 ΔrHmo、熵 ΔrSmo 和吉布斯自由能 ΔrGmochanges。还计算了这些反应在生理条件下的表观平衡常数和标准转换吉布斯自由能变化。讨论了使用这些结果优化支链氨基酸的产品产量。
-
Detailed Structure-Function Correlations of<i>Bacillus subtilis</i>Acetolactate Synthase作者:Bettina Sommer、Holger von Moeller、Martina Haack、Farah Qoura、Clemens Langner、Gleb Bourenkov、Daniel Garbe、Bernhard Loll、Thomas BrückDOI:10.1002/cbic.201402541日期:2015.1.2Acetolactate synthase (ALS) is an essential enzyme in designed isobutanol biosynthesis pathways. Because of its efficient catalytic conversion of pyruvate to acetolactate and its reactivity towards the alternative substrate ketoisovalerate (KIV), the ALS of B. subtilis is of particular interest. This study provides new insights into the structure–function relationships of this catalytic mechanism.
-
Isoleucine Biosynthesis in <i>Leptospira interrogans</i> Serotype lai Strain 56601 Proceeds via a Threonine-Independent Pathway作者:Hai Xu、Yuzhen Zhang、Xiaokui Guo、Shuangxi Ren、Andreas A. Staempfli、Juishen Chiao、Weihong Jiang、Guoping ZhaoDOI:10.1128/jb.186.16.5400-5409.2004日期:2004.8.15
ABSTRACT Three
leuA -like protein-coding sequences were identified inLeptospira interrogans . One of these, thecimA gene, was shown to encode citramalate synthase (EC 4.1.3.-). The other two encoded α-isopropylmalate synthase (EC 4.1.3.12). Expressed inEscherichia coli , the citramalate synthase was purified and characterized. Although its activity was relatively low, it was strictly specific for pyruvate as the keto acid substrate. Unlike the citramalate synthase of the thermophileMethanococcus jannaschii , theL. interrogans enzyme is temperature sensitive but exhibits a much lowerK m (0.04 mM) for pyruvate. The reaction product was characterized as (R )-citramalate, and the proposed β-methyl-d -malate pathway was further confirmed by demonstrating that citraconate was the substrate for the following reaction. This alternative pathway for isoleucine biosynthesis from pyruvate was analyzed both in vitro by assays of leptospiral isopropylmalate isomerase (EC 4.2.1.33) and β-isopropylmalate dehydrogenase (EC 1.1.1.85) inE. coli extracts bearing the corresponding clones and in vivo by complementation ofE. coli ilvA ,leuC /D , andleuB mutants. Thus, the existence of a leucine-like pathway for isoleucine biosynthesis inL. interrogans under physiological conditions was unequivocally proven. Significant variations in either the enzymatic activities or mRNA levels of thecimA andleuA genes were detected inL. interrogans grown on minimal medium supplemented with different levels of the corresponding amino acids or in cells grown on serum-containing rich medium. The similarity of this metabolic pathway in leptospires and archaea is consistent with the evolutionarily primitive status of the eubacterial spirochetes.摘要 三 leuA -蛋白编码序列。 钩端螺旋体 .其中一个 cimA 基因编码柠檬醛酸合成酶(EC 4.1.3.-)。另外两个基因编码α-异丙基丙二酸合成酶(EC 4.1.3.12)。在 大肠杆菌 纯化并鉴定了柠檬丙二酸合成酶。虽然其活性相对较低,但它对酮酸底物丙酮酸具有严格的特异性。与嗜热菌的柠檬醛酸合成酶不同的是 不同。 不同的是 L. interrogans 酶对温度敏感,但它对酮酸底物丙酮酸的特异性要低得多。 K m (0.04 mM)。反应产物的特征为 R )-柠檬醛酸,以及拟议的 β-甲基-(R) d 通过证明柠檬酸盐是接下来反应的底物,进一步证实了所提出的 β-甲基-d-丙二酸盐途径。通过检测大肠杆菌中的钩端螺旋异丙基丙二酸异构酶(EC 4.2.1.33)和 β-异丙基丙二酸脱氢酶(EC 1.1.1.85),分析了丙酮酸异亮氨酸的体外生物合成途径。 大肠杆菌 大肠杆菌ilvA 的互补作用,在含有相应克隆的大肠杆菌提取物和体内 大肠杆菌 ilvA , leuC / D 和 突变体 突变体。因此,异亮氨酸生物合成的亮氨酸样途径存在于 L. interrogans 在生理条件下异亮氨酸生物合成途径的存在得到了明确的证明。cimA 突变体的酶活性或 mRNA 水平的显著变化 cimA 和 leuA 基因在 L. interrogans 细胞中检测到了 cimA 和 leuA 基因。这种代谢途径在钩端螺旋体和古细菌中的相似性与真细菌螺旋体在进化过程中的原始地位是一致的。 -
Snake Venom L-Amino Acid Oxidases: Trends in Pharmacology and Biochemistry作者:Luiz Fernando M. Izidoro、Juliana C. Sobrinho、Mirian M. Mendes、Tássia R. Costa、Amy N. Grabner、Veridiana M. Rodrigues、Saulo L. da Silva、Fernando B. Zanchi、Juliana P. Zuliani、Carla F. C. Fernandes、Leonardo A. Calderon、Rodrigo G. Stábeli、Andreimar M. SoaresDOI:10.1155/2014/196754日期:——
L-amino acid oxidases are enzymes found in several organisms, including venoms of snakes, where they contribute to the toxicity of ophidian envenomation. Their toxicity is primarily due to enzymatic activity, but other mechanisms have been proposed recently which require further investigation. L-amino acid oxidases exert biological and pharmacological effects, including actions on platelet aggregation and the induction of apoptosis, hemorrhage, and cytotoxicity. These proteins present a high biotechnological potential for the development of antimicrobial, antitumor, and antiprotozoan agents. This review provides an overview of the biochemical properties and pharmacological effects of snake venom L-amino acid oxidases, their structure/activity relationship, and supposed mechanisms of action described so far.
表征谱图
-
氢谱1HNMR
-
质谱MS
-
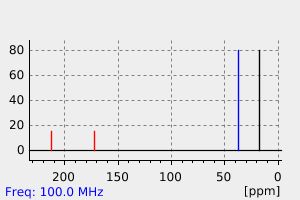
碳谱13CNMR
-
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息