氘 | 12184-84-8
物质功能分类
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
物化性质
-
熔点:-254.43° (18.73 K) at 128.5 mm (triple point)
-
沸点:-249.5 °C(lit.)
-
密度:0.169 g/mL at 25 °C(lit.)
-
蒸气密度:0.07 (vs air)
-
介电常数:1.3(20℃)
-
物理描述:Deuterium is an isotope of hydrogen but it is chemically identical. It is a colorless, odorless gas. It is easily ignited. Once ignited it burns with a pale blue, almost invisible flame. The vapors are lighter than air. It is flammable over a wide range of vapor/air concentrations. Under prolonged exposure to fire or intense heat the containers may rupture violently and rocket. It is not toxic but is a simple asphyxiate by the displacement of oxygen in the air.
-
颜色/状态:COLORLESS GAS
-
气味:Odorless
-
溶解度:SLIGHTLY SOL IN COLD WATER
-
蒸汽压力:17.14 kPa
-
自燃温度:1085 °F
-
腐蚀性:Noncorrosive
-
汽化热:1225 J/mol
计算性质
-
辛醇/水分配系数(LogP):0
-
重原子数:0
-
可旋转键数:0
-
环数:0.0
-
sp3杂化的碳原子比例:0.0
-
拓扑面积:0
-
氢给体数:0
-
氢受体数:0
ADMET
安全信息
-
危险等级:2.1
制备方法与用途
氘又称重氢(符号D或2H),是氢的一种同位素。在自然界的氢气中,氘占约0.02%。尽管大部分理化性质与氕相似,但氘的反应性较弱,并且可以参与形成重水(D2O)。由于重水主要以重水形式存在,因此它常被用于研究氢的反应机理和核现象。在人工加速条件下,氘能够参与核反应,在热核反应中释放大量能量,同时也能作为氢反应机理的示踪原子。
如果人体内的氘含量过高,则可能无法产生足够的能量,从而引发疲劳、癌症及其他慢性疾病。许多人的病症可能与体内过高的氘水平有关,比如食用转基因食品和工业化食品,或者居住在临海地区等。
药效作用由于氘(D)的原子质量显著高于氢(H),碳-氘键会在较低频率上振动,且其零点基础能量低于相应的碳氢键。虽然过渡态活化能相近,但使碳氘键断裂所需的能量更高。因此,当化合物中的氢被氘取代后,化学反应速率会显著减缓。具体而言,在涉及碳氢键对称断裂的反应中,氢被氘取代可以使反应速度降低约85%。
理论上讲,如果碳氢键断裂是代谢途径的关键步骤,则氢被氘取代会导致该代谢过程在生物体内的催化速率下降甚至停止。例如,细胞色素P450、单胺氧化酶和醛氧化酶等关键酶的作用可能会受到影响。
危害自1931年美国H.C.尤里和F.G.布里克维德发现氘以来,其在生物学及生态学中的重要性立即引起了广泛的关注。重水由两个重氢原子和一个氧原子组成(D2O),尽管与普通水性质相似,但在密度、熔点、沸点以及电离度等方面有所差异。
由于重水分子量较大且运动速度较慢,在高山冰雪中含量极低,尤其是在南极冰雪中更为稀少。重水在原子能技术中有重要应用,特别作为核反应堆中的减速剂。此外,电解重水可以制备出重氢,后者是制造威力巨大的核武器——氢弹的重要原料。
制备方法氘可通过电解重水或在较高温度下用铁或钨还原重水而获得。其主要用途包括研究氢的反应机理和核现象,以及作为示踪原子进行人工加速核反应,在热核子反应中释放出大量能量,并作为一种潜在的重要能源。
上下游信息
-
下游产品
中文名称 英文名称 CAS号 化学式 分子量 —— Tritium Hydrogen Deuterium —— H2 5.0
反应信息
-
作为反应物:参考文献:名称:Pd(111)上钒氧化物纳米结构的模型反应研究。摘要:在Pd(111)上制备的超薄钒氧化物结构上,研究了氘的解吸以及氘与氧之间的水反应。钯样品是渗透源的一部分,因此能够通过主体将原子氘供应到样品表面。已经通过在氧气气氛下在UHV中进行电子束蒸发来制备不同的氧化钒膜。这些膜的结构是使用低能电子衍射和扫描隧道显微镜确定的。解吸和反应产物的平均平移能用飞行时间光谱仪测量。单层和亚单层VOx的最稳定相分别是特定的表面V2O3和VO相,分别为523和700K。较厚的薄膜以块状V2O3的形式生长。在所有情况下,脱附氘物种的平均翻译能量均对应于热值。与该能量分布的明显偏差可归因于来自气相的分子氘在各个钒氧化物膜上的不同吸附/解吸和/或容纳行为。水反应产物显示出稍高的平均转化能,表明较高的高能渗透氘对水的形成有较高的贡献。DOI:10.1063/1.2336770
-
作为产物:参考文献:名称:另一个史无前例的维兰德机理得到证实:过氧化氢,甲醛和氢氧化钠形成氢摘要:1923年,威兰和温勒报道,在分子氢产生具有在碱性溶液中甲醛的过氧化氢的反应中,自由氢原子(H 。)不参与。他们推测,双(羟甲基)过氧化物HOCH 2 OOCH 2 OH是中间体,它分解生成H 2和甲酸酯,提出了一种如今被认为是“令人信服的过程”的机理。从那时起,提出了其他几种(相互冲突的)“机制”。我们的NMR和拉曼光谱和动力学研究,尤其是氘动力学同位素效应(DKIE)的测定,现在证实,在这种依赖碱的反应中,H 2的两个H原子均源自CH 2甲醛的氢原子,而不是HOCH 2 OOCH 2 OH的OH基团或水。量子化学CBS-QB3和W1BD计算表明,H 2的释放通过协同过程进行,而HOCH 2 OOCH 2 OH的双重去质子化作用强烈促进了H 2的释放,从而排除了自由基途径。DOI:10.1002/anie.201800636
-
作为试剂:描述:2-萘甲醇 、 N,N-二甲基乙酰胺 在 copper diacetate 、 sodium hydride 、 氘 作用下, 以 甲苯 、 mineral oil 为溶剂, 110.0 ℃ 、100.0 kPa 条件下, 以56%的产率得到参考文献:名称:铜催化酰胺与醇的 α-烷基化借氢反应摘要:我们报告了第一个通过借氢策略铜催化乙酰胺与醇进行 α-烷基化的例子。在原位生成的铜颗粒的催化下,乙酰胺和各种取代的苯甲醇或烷基醇以良好的收率和优异的选择性转化为官能化酰胺。与之前的工作相比,该过程简单,使用市售的Cu(OAc) 2作为预催化剂,无需额外的配体或金属配合物,并且更容易。机理研究表明醛和α,β-不饱和酰胺是该反应的中间体,并且还揭示了铜在醇脱氢和C=C键氢化中的作用。DOI:10.1021/acs.joc.4c00404
文献信息
-
Efficient Water Reduction with sp<sup>3</sup> -sp<sup>3</sup> Diboron(4) Compounds: Application to Hydrogenations, H-D Exchange Reactions, and Carbonyl Reductions作者:Mathias Flinker、Hongfei Yin、René W. Juhl、Espen Z. Eikeland、Jacob Overgaard、Dennis U. Nielsen、Troels SkrydstrupDOI:10.1002/anie.201709685日期:2017.12.11demonstrated by conducting a series of selective reductions of alkynes and alkenes, and hydrogen–deuterium exchange reactions using two‐chamber reactors. Finally, as the water reduction reaction generates an intermediate borohydride species, a range of aldehydes and ketones were reduced by using water as the hydride source.
-
Ruthenium xantphos complexes in hydrogen transfer processes: reactivity and mechanistic studies作者:Araminta E. W. Ledger、Paul A. Slatford、John P. Lowe、Mary F. Mahon、Michael K. Whittlesey、Jonathan M. J. WilliamsDOI:10.1039/b813543f日期:——The in situ combination of [Ru(PPh3)3(CO)H2] with xantphos is catalytically active for the alkylation of alcohols with the ketonitriletBuC(O)CH2CN in a model oxidation–Knoevenagel–reduction process. The precursor complex [Ru(xantphos)(PPh3)(CO)H2] was isolated and reacted with stoichiometric amounts of PhCH2OH and PhCHO. Under these conditions, the alcohol is decarbonylated to afford [Ru(xantphos)(CO)2H2] and finally [Ru(xantphos)(CO)3], both of which prove to be less active for catalysis than the starting complex. The reactivity of the xantphos system contrasts with that of [Ru(dppp)(PPh3)(CO)H2], which is catalytically inactive for the Knoevenagel reaction and fails to show any stoichiometric reactivity with alcohols.在模型氧化-Knoevenagel-还原过程中,[Ru(PPh3)3(CO)H2] 与 xantphos 的原位组合对醇与 ketonitrile tBuC(O)CH2CN 的烷基化具有催化活性。前驱体复合物 [Ru(xantphos)(PPh3)(CO)H2] 被分离出来,并与当量的 PhCH2OH 和 PhCHO 反应。在这些条件下,醇脱羰生成 [Ru(xantphos)(CO)2H2],最终生成 [Ru(xantphos)(CO)3],这两者在催化活性上均不如起始复合物。xantphos 体系的反应性与 [Ru(dppp)(PPh3)(CO)H2] 形成对比,后者对 Knoevenagel 反应无催化活性,并且与醇没有化学计量反应性。
-
Ligand-Assisted Heterolytic Activation of Hydrogen and Silanes Mediated by Nitrosyl Rhenium Complexes作者:Angela Llamazares、Helmut W. Schmalle、Heinz BerkeDOI:10.1021/om010409c日期:2001.12.1Abstraction of the hydride in the dinitrosyl rhenium complexes [Re(H)(NO)2(PR3)2] (R = iPr (1a), Cy (1b)) affords the dinuclear saturated compounds [Re2(H)(μ,η2-NO)(NO)3(PR3)4][BAr4‘] (R = iPr, 2a; Cy, 2b) or the mononuclear unsaturated 16-electron derivatives [Re(NO)2(PR3)2][BAr4‘] (R = iPr, 3a; Cy, 3b). In complexes 2a,b the metal centers are connected via a nitrosyl−isonitrosyl linkage. Complexes 2在二亚硝酰基rh络合物[Re(H)(NO)2(PR 3)2 ](R = i Pr(1a),Cy(1b))中氢化物的提取提供了双核饱和化合物[Re 2(H)( μ,η 2 -NO)(NO)3(PR 3)4 ] [巴4 “](R =我PR,2A ; CY,图2b)或单核不饱和16电子衍生物[回复(NO)2(PR 3)2 ] [BAr 4 '](R = i Pr,3a; Cy,3b)。在络合物2a,b中,金属中心通过亚硝酰基-亚硝酰基连接。配合物2和3与经典的双电子供体配体(例如CH 3 CN,CO,C 6 H 5 CHO和THF)反应,还与H 2和HSiEt 3反应。在后两种情况下,实现了氢氢键或氢硅键的杂合断裂。络合物2a,b和3a,b在H 2 / D 2的催化加扰中具有活性。在非常温和的条件下提供高清效果。在四甲基哌啶作为碱的存在下,这些络合物与H 2的反应产生[Re(H)(NO)NOH
-
Reactions of a Triazacyclononane-Supported Tantalum−Lithium Bridging Alkylidene with Organic Substrates作者:Joseph A. R. Schmidt、John ArnoldDOI:10.1021/om020175c日期:2002.8.1The reactivity of a range of electrophilic organic substrates with a heterobimetallic tantalum−lithium bridging alkylidene [(Me3SiCH2)(ArN)Ta(μ-CHSiMe3)(μ-η1:η3-iPr2-tacn)Li, 3] is presented. Proton sources of widely varying acidity react to protonate the alkylidene ligand, leading to an interesting tantalum−lithium bridging hydride complex in the case of H2. The alkylidene 3 undergoes a series of
-
Hydrogenation/dehydrogenation of N-heterocycles catalyzed by ruthenium complexes based on multimodal proton-responsive CNN(H) pincer ligands作者:Práxedes Sánchez、Martín Hernández-Juárez、Nuria Rendón、Joaquín López-Serrano、Laura L. Santos、Eleuterio Álvarez、Margarita Paneque、Andrés SuárezDOI:10.1039/d0dt02326d日期:——Ru complexes based on lutidine-derived pincer CNN(H) ligands having secondary amine side donors are efficient precatalysts in the hydrogenation and dehydrogenation of N-heterocycles. Reaction of a Ru-CNN(H) complex with an excess of base produces the formation of a Ru(0) derivative, which is observed under catalytic conditions.
表征谱图
-
氢谱1HNMR
-
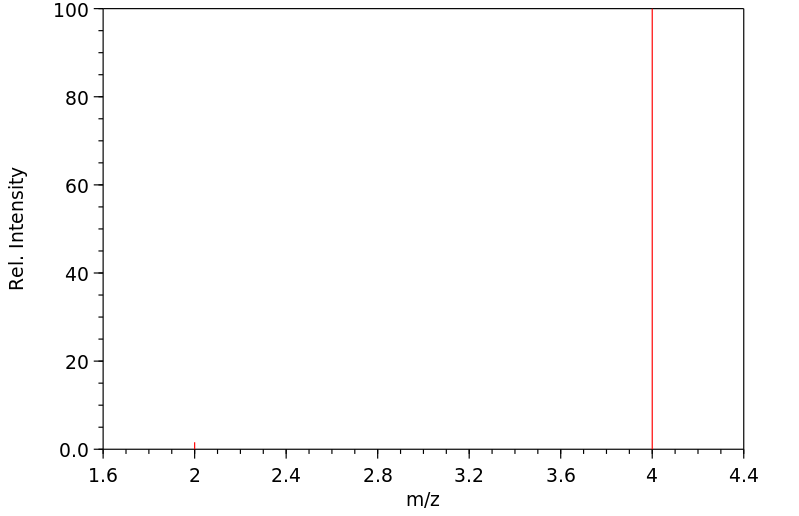
质谱MS
-
碳谱13CNMR
-
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息