3-[(3-Fluorophenyl)amino]cyclohex-2-en-1-one
中文名称
——
中文别名
——
英文名称
3-[(3-Fluorophenyl)amino]cyclohex-2-en-1-one
英文别名
3-(3-fluoroanilino)cyclohex-2-en-1-one
CAS
——
化学式
C12H12FNO
mdl
MFCD01109149
分子量
205.232
InChiKey
VSYILMIYVRAESQ-UHFFFAOYSA-N
BEILSTEIN
——
EINECS
——
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
计算性质
-
辛醇/水分配系数(LogP):2.3
-
重原子数:15
-
可旋转键数:2
-
环数:2.0
-
sp3杂化的碳原子比例:0.25
-
拓扑面积:29.1
-
氢给体数:1
-
氢受体数:3
反应信息
-
作为反应物:描述:2,6-二氟硝基苯 、 3-[(3-Fluorophenyl)amino]cyclohex-2-en-1-one 在 caesium carbonate 作用下, 以 二甲基亚砜 为溶剂, 以45%的产率得到6-fluoro-10-(3-fluorophenyl)phenazin-2(10H)-one参考文献:名称:烯胺酮与邻氟硝基苯的高度区域选择性和化学选择性[3 + 3]环化:安波沙芬酮及其N-氧化物的不同合成摘要:从烯胺酮与邻氟硝基苯的[3 + 3]环氧基化反应中发展出了一种碱促进的前所未有的策略,用于区域选择性和化学选择性发散性合成高度官能化的双氢呋喃酮及其N-氧化物。这种新颖的合成策略提供了另一种方法来构建长春黄酮,其氮氧化物在生物学和有机合成领域都具有重要意义。既定的协议探索了烯胺的环化范围,并扩展了基于硝基的环化的应用。DOI:10.1021/acs.orglett.1c00710
-
作为产物:参考文献:名称:烯胺酮的 NMR 第 3 部分 - 无环和环 N-芳基烯胺酮的 1H、13C 和 17O NMR 光谱研究:取代基效应和分子内氢键摘要:对位和间位取代的 4-芳基氨基戊-3-烯-2-酮(无环烯胺酮,1 和 2)和 3-芳基氨基环己-2-烯-1-酮(环烯胺酮,3和 4) 被报告。这些烯胺酮的 17O、13C 和 1H 位移值与间位和对位衍生物相关性中的 σm0 和 σp 常数以及相应苯胺的 pKa 值密切相关。还进行了双取代基参数分析。羰基的 17O 和 13C 化学位移与相应的 N-酰基苯胺化学位移的相关性表明,烯胺酮部分作为一个整体具有与 RCONH 基团相似的电子特性。烯胺酮的羰基 O 原子的 17O 位移值与其 1H 和 13C 数据密切相关。与 3 和 4 相比,观察到 1 和 2 对 O 原子的屏蔽为 33–45 ppm,分别。这归因于分子内氢键。© 1997 John Wiley & Sons, Ltd.DOI:10.1002/(sici)1097-458x(199705)35:5<311::aid-omr94>3.0.co;2-m
文献信息
-
Syntheses of N-Alkylated Carbazolones via Pd(OAc)2-Mediated Intramolecular Coupling of N-Substituted 3-(Arylamino)cyclohex-2-enones作者:Yunfei Du、Jianhui Huang、Wenying Bi、Xiliu Yun、Yanfeng Fan、Xiuxiang QiDOI:10.1055/s-0030-1259027日期:2010.12A variety of functionalized N-alkylated carbazolones were prepared via N-alkylation of 3-(arylamino)cyclohex-2-enones followed by an intramolecular oxidative coupling mediated by Pd(OAc)2 under an oxygen atmosphere. This approach adopts an inverted sequence, consisting of the conventional annulation and subsequent N-alkylation.
-
Organocatalytic Generation of o-Quinone Methides from Commonly Used o-Hydroxystyrenes at High Temperature for Enantioselective Cyclization作者:Qiong Wu、Man-Su Tu、Feng Shi、Man Tang、Jia-Jia ZhaoDOI:10.1055/s-0036-1588935日期:——organocatalysis from commonly used o-hydroxystyrenes undergo enantioselective cyclization with dimedone-derived enaminones, to form biologically important tetrahydroxanthenes in high yields and good enantioselectivities (up to 88% yield, 95:5 er). The reaction proceeds in chlorobenzene in the presence of a chiral phosphoric acid (CPA) at 110 °C. The reaction scope with regard to various ring-substituted o-hydroxystyrenes摘要 在有机催化下,在高温下由常用的邻羟基苯乙烯生成的邻醌醌与对二酮衍生的烯胺酮进行对映选择性环化反应,以高收率和良好的对映选择性(高达88%的产率,95:5 er)形成生物学上重要的四氢黄嘌呤。该反应在手性磷酸(CPA)的存在下于110°C在氯苯中进行。研究了关于各种环取代的邻羟基苯乙烯和各种N-芳基取代的烯胺酮的反应范围。另外,该反应还提供了构建手性四氢氧杂蒽骨架的有效方法。 在有机催化下,在高温下由常用的邻羟基苯乙烯生成的邻醌醌与对二酮衍生的烯胺酮进行对映选择性环化反应,以高收率和良好的对映选择性(高达88%的产率,95:5 er)形成生物学上重要的四氢黄嘌呤。该反应在手性磷酸(CPA)的存在下于110°C在氯苯中进行。研究了关于各种环取代的邻羟基苯乙烯和各种N-芳基取代的烯胺酮的反应范围。另外,该反应还提供了构建手性四氢氧杂蒽骨架的有效方法。
-
Efficient construction of C–N and C–S bonds in 2-iminothiazoles via cascade reaction of enaminones with potassium thiocyanate作者:Xue-Bing Chen、Xue-Quan Wang、Jia-Na Song、Qing-Li Yang、Chao Huang、Wei LiuDOI:10.1039/c7ob00306d日期:——A novel and highly efficient protocol has been developed for the regioselective synthesis of 2-iminothiazole derivatives with potential biochemical interest by the reaction of enaminones, potassium thiocyanate (KSCN), and N-bromo succinimide (NBS) under mild conditions. The reaction proceeds via the formation of α-bromo enaminones as a versatile intermediate followed by thiocyanation/intramolecular
-
Formal synthesis of 10‐Hydroxy‐6‐Aryldibenzo[b,g][1,8]Naphthyridin‐11(6H)‐ones from 2‐chloroquinolin‐3‐carbaldehydes and 3‐(Arylamino)cyclohexenones作者:Han‐Joo Lee、Joo‐Hyun Jeon、Jin‐Hee Kim、Hitesh B. Jalani、Jin‐Hyun JeongDOI:10.1002/jhet.4799日期:2024.5We have described herein a simple and formal synthesis of 10-Hydroxy-6-Aryldibenzo[b,g][1,8]naphthyridin-11(6H)-ones from 2-chloroquinolin-3-carbaldehydes and 3-(Arylamino)cyclohexenones. This protocol provides the formation of four rings including 1,8-naphthyridin under the mild conditions. Furthermore, the cyclohexanone part of the enaminone undergoes air oxidation provided the phenol ring is attached
表征谱图
-
氢谱1HNMR
-
质谱MS
-
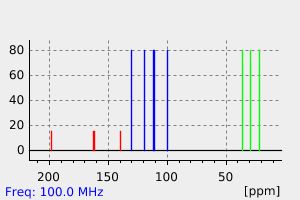
碳谱13CNMR
-
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息
同类化合物
(βS)-β-氨基-4-(4-羟基苯氧基)-3,5-二碘苯甲丙醇
(S,S)-邻甲苯基-DIPAMP
(S)-(-)-7'-〔4(S)-(苄基)恶唑-2-基]-7-二(3,5-二-叔丁基苯基)膦基-2,2',3,3'-四氢-1,1-螺二氢茚
(S)-盐酸沙丁胺醇
(S)-3-(叔丁基)-4-(2,6-二甲氧基苯基)-2,3-二氢苯并[d][1,3]氧磷杂环戊二烯
(S)-2,2'-双[双(3,5-三氟甲基苯基)膦基]-4,4',6,6'-四甲氧基联苯
(S)-1-[3,5-双(三氟甲基)苯基]-3-[1-(二甲基氨基)-3-甲基丁烷-2-基]硫脲
(R)富马酸托特罗定
(R)-(-)-盐酸尼古地平
(R)-(-)-4,12-双(二苯基膦基)[2.2]对环芳烷(1,5环辛二烯)铑(I)四氟硼酸盐
(R)-(+)-7-双(3,5-二叔丁基苯基)膦基7''-[((6-甲基吡啶-2-基甲基)氨基]-2,2'',3,3''-四氢-1,1''-螺双茚满
(R)-(+)-7-双(3,5-二叔丁基苯基)膦基7''-[(4-叔丁基吡啶-2-基甲基)氨基]-2,2'',3,3''-四氢-1,1''-螺双茚满
(R)-(+)-7-双(3,5-二叔丁基苯基)膦基7''-[(3-甲基吡啶-2-基甲基)氨基]-2,2'',3,3''-四氢-1,1''-螺双茚满
(R)-(+)-4,7-双(3,5-二-叔丁基苯基)膦基-7“-[(吡啶-2-基甲基)氨基]-2,2”,3,3'-四氢1,1'-螺二茚满
(R)-3-(叔丁基)-4-(2,6-二苯氧基苯基)-2,3-二氢苯并[d][1,3]氧杂磷杂环戊烯
(R)-2-[((二苯基膦基)甲基]吡咯烷
(R)-1-[3,5-双(三氟甲基)苯基]-3-[1-(二甲基氨基)-3-甲基丁烷-2-基]硫脲
(N-(4-甲氧基苯基)-N-甲基-3-(1-哌啶基)丙-2-烯酰胺)
(5-溴-2-羟基苯基)-4-氯苯甲酮
(5-溴-2-氯苯基)(4-羟基苯基)甲酮
(5-氧代-3-苯基-2,5-二氢-1,2,3,4-oxatriazol-3-鎓)
(4S,5R)-4-甲基-5-苯基-1,2,3-氧代噻唑烷-2,2-二氧化物-3-羧酸叔丁酯
(4S,4''S)-2,2''-亚环戊基双[4,5-二氢-4-(苯甲基)恶唑]
(4-溴苯基)-[2-氟-4-[6-[甲基(丙-2-烯基)氨基]己氧基]苯基]甲酮
(4-丁氧基苯甲基)三苯基溴化磷
(3aR,8aR)-(-)-4,4,8,8-四(3,5-二甲基苯基)四氢-2,2-二甲基-6-苯基-1,3-二氧戊环[4,5-e]二恶唑磷
(3aR,6aS)-5-氧代六氢环戊基[c]吡咯-2(1H)-羧酸酯
(2Z)-3-[[(4-氯苯基)氨基]-2-氰基丙烯酸乙酯
(2S,3S,5S)-5-(叔丁氧基甲酰氨基)-2-(N-5-噻唑基-甲氧羰基)氨基-1,6-二苯基-3-羟基己烷
(2S,2''S,3S,3''S)-3,3''-二叔丁基-4,4''-双(2,6-二甲氧基苯基)-2,2'',3,3''-四氢-2,2''-联苯并[d][1,3]氧杂磷杂戊环
(2S)-(-)-2-{[[[[3,5-双(氟代甲基)苯基]氨基]硫代甲基]氨基}-N-(二苯基甲基)-N,3,3-三甲基丁酰胺
(2S)-2-[[[[[((1S,2S)-2-氨基环己基]氨基]硫代甲基]氨基]-N-(二苯甲基)-N,3,3-三甲基丁酰胺
(2S)-2-[[[[[[((1R,2R)-2-氨基环己基]氨基]硫代甲基]氨基]-N-(二苯甲基)-N,3,3-三甲基丁酰胺
(2-硝基苯基)磷酸三酰胺
(2,6-二氯苯基)乙酰氯
(2,3-二甲氧基-5-甲基苯基)硼酸
(1S,2S,3S,5S)-5-叠氮基-3-(苯基甲氧基)-2-[(苯基甲氧基)甲基]环戊醇
(1S,2S,3R,5R)-2-(苄氧基)甲基-6-氧杂双环[3.1.0]己-3-醇
(1-(4-氟苯基)环丙基)甲胺盐酸盐
(1-(3-溴苯基)环丁基)甲胺盐酸盐
(1-(2-氯苯基)环丁基)甲胺盐酸盐
(1-(2-氟苯基)环丙基)甲胺盐酸盐
(1-(2,6-二氟苯基)环丙基)甲胺盐酸盐
(-)-去甲基西布曲明
龙蒿油
龙胆酸钠
龙胆酸叔丁酯
龙胆酸
龙胆紫-d6
龙胆紫