仲丁基亚硝酸酯 | 924-43-6
中文名称
仲丁基亚硝酸酯
中文别名
——
英文名称
sec-butyl nitrite
英文别名
2-butyl nitrite;butan-2-yl nitrite
CAS
924-43-6
化学式
C4H9NO2
mdl
MFCD00043489
分子量
103.121
InChiKey
NFGNZNFBQAGBJA-UHFFFAOYSA-N
BEILSTEIN
——
EINECS
——
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
物化性质
-
沸点:67.85°C
-
密度:0.8726
-
保留指数:542
计算性质
-
辛醇/水分配系数(LogP):1.4
-
重原子数:7
-
可旋转键数:2
-
环数:0.0
-
sp3杂化的碳原子比例:1.0
-
拓扑面积:38.7
-
氢给体数:0
-
氢受体数:3
安全信息
-
危险等级:3.1
-
危险品标志:Xn,F
-
危险类别码:R20/22,R11
-
海关编码:2920909090
-
包装等级:II
-
危险类别:3.1
-
危险品运输编号:UN 2351
-
储存条件:库房应保持通风、低温和干燥,并将该物品与其他还原剂及食品原料分开存放。
SDS
制备方法与用途
类别:易燃液体
毒性分级:高毒
急性毒性:
- 口服 - 小鼠 LD50: 423 毫克/公斤
- 吸入 - 小鼠 LC50: 1753 ppm(1小时)
爆炸物危险特性:氧化剂;潜在爆炸物
可燃性危险特性:遇热、明火或还原剂燃烧时会燃烧;受热分解后排出有毒氮氧化物烟雾
储运特性:
- 库房应保持通风、低温和干燥
- 避免与还原剂及食品原料混存
灭火剂:水、泡沫、干粉
反应信息
-
作为反应物:参考文献:名称:Wojcik-Pastuszka; Jodkowski, Polish Journal of Chemistry, 2009, vol. 83, # 1, p. 131 - 143摘要:DOI:
-
作为产物:描述:参考文献:名称:Rate constants for the decomposition of 2-butoxy radicals and their reaction with NO and O2摘要:利用激光光解/激光诱导荧光技术研究了 2-丁氧基自由基的反应性。研究了三个反应:(i) 在 0.03 < p < 0.4 bar 的氦气总压力和 295-348 K 之间的五个温度下,用同样的技术测量了与 NO 反应的速率常数。(ii) 在室温和 0.131 巴氦气条件下测得 O2 的速率常数:k2 = (9 ± 2) × 10-15 cm3 s-1。由于 O2 对 2-丁氧基荧光有明显的淬灭作用,因此无法在更大的温度范围内进行实验:kq,O2 = (4 ± 1) × 10-11 cm3 s-1。(iii) 在 0.01 < p < 0.8 bar 的氦气总压和 291-348 K 的四种温度下单分子分解的温度和压力依赖性。2 × 10-8 exp(-35.9 kJ mol-1/RT) cm3 s-1,k3,∞ = 1.1 × 1014 exp(-53.6 kJ mol-1/RT) s-1,F3,c = 0.87 - T/870 K。我们预计这些速率常数的不确定性为 ±30%。这些结果与之前的预测(C. Fittschen, H. Hippler and B. Viskolcz, Phys.Chem.Phys., 2000, 2, 1677-1683 (); R. Méreau, M.-T.Rayez, F. Caralp and J.-C.Rayez, Phys.Chem.Phys., 2000, 2, 3765 ()) .DOI:10.1039/b405134c
-
作为试剂:描述:参考文献:名称:芳族叔胺和亚硝酸正丁酯摘要:在各种实验条件下,亚硝酸烷基酯,特别是亚硝酸正丁酯与叔芳族胺之间的反应迅速产生了N-脱烷基化-N-亚硝化,环硝化,ipso取代的产物,有时还产生了这些过程的组合。在进行亚硝化的过程中,氨基醚被检测为最终产物和中间体。根据实验证据,对某些观察到的行为建议了反应途径,而其他替代方法则被放弃。DOI:10.1016/s0040-4020(01)86768-5
文献信息
-
Relative-rate study of thermal decomposition of the 2-butoxyl radical in the temperature range 280–313 KElectronic supplementary information (ESI) available: See http://www.rsc.org/suppdata/cp/b1/b111474c/作者:H. G. Libuda、O. Shestakov、J. Theloke、F. ZabelDOI:10.1039/b111474c日期:2002.5.29The competition between thermal decomposition (kdis) and reaction with O2 (kO2) has been studied for the 2-butoxyl radical in a newly built 210 L photoreactor constructed of quartz. 2-Butoxyl radicals were generated by continuous 254 nm photolysis of 2-butoxyl iodide in the presence of O2 and NO, using N2 as a buffer gas. Reaction educts and products were analysed by long-path (29 m) IR absorption using an FTIR spectrometer. The ratio kdis/kO2 was derived from the product ratios of acetaldehyde and butanone, corrected for small amounts of side products. At 280, 298, and 313 K and a total pressure of 1 bar (Mâ=âO2â+âN2), kdis/kO2 was determined at O2 partial pressures between 100 and 1000 mbar. At all temperatures, there was a systematic increase of (kdis/kO2)effââ¡â(Î[CH3CHO]corrâÃâ[O2]) / (2âÃâÎ[CH3C(O)CH2CH3]) with the partial pressure of O2 which possibly is the result of an additional O2 independent source of acetaldehyde (â8% of the 2-butoxyl radicals reacting by either of the two competing pathways at 298 K, 1 bar). Pressure-dependence studies between 100 and 1000 mbar support the hypothesis that the additional acetaldehyde originates from the formation of 6â10% chemically activated 2-butoxyl radicals in the temperature range 280â313 K. Correction of (kdis/kO2)eff for the O2 independent yield of acetaldehyde results in kdis/kO2â=â(6.8â±â1.4)âÃâ1017, (2.3â±â0.5)âÃâ1018, and (5.5â±â1.1)âÃâ1018 molecule cmâ3 at 279.8, 298.2, and 313.5 K, respectively, leading to the Arrhenius expression kdis/kO2â=â(2.0â±â0.5)âÃâ1026exp(â45.4 kJ molâ1/RT) molecule cmâ3 at a total pressure of 1 bar. This temperature dependence of kdis/kO2 implies that, depending on temperature, either thermal decomposition or reaction with O2 is the major loss process of 2-butoxyl radicals under the conditions of the lower troposphere. Using literature values for kO2, kdisâ=â3.9âÃâ1012âexp(â47.1 kJ molâ1/RT) sâ1 is derived for a total pressure of 1 bar (Mâ=âN2â+âO2), which compares very favourably with a recent theoretical estimate (ab initioâ+âRRKM) by Somnitz and Zellner (H. Somnitz and R. Zellner, Phys. Chem. Chem. Phys., 2000, 2, 1907).在由石英制成的新建210升光反应器中,对2-丁氧基自由基的分解(kdis)与O2反应(kO2)的竞争进行了研究。2-丁氧基自由基是在存在O2和NO的情况下,通过持续的254纳米光解2-丁氧基碘化物产生的,使用N2作为缓冲气体。反应物和产物通过使用傅里叶变换红外光谱仪的长路径(29米)红外吸收进行分析。根据乙醛和丁酮的产品比例,修正了少量副产物的影响,得到了kdis/kO2的比例。在280、298和313 K以及总压力为1巴(M=O2+N2)的条件下,kdis/kO2在O2的分压介于100到1000毫巴之间被确定。在所有温度下,(kdis/kO2)eff≡(Δ[CH3CHO]corr×[O2])/(2×Δ[CH3C(O)CH2CH3])随O2分压的增加有系统性的增加,这可能是由于来自O2独立来源的乙醛的额外贡献(在298 K,1巴的条件下,大约8%的2-丁氧基自由基通过这两种竞争路径中的任何一种反应)。在100到1000毫巴的压力依赖性研究支持了这样一个假设,即额外的乙醛来源于在280到313 K的温度范围内形成的化学激活的2-丁氧基自由基,其比例为6到10%。修正(kdis/kO2)eff对于O2独立产生的乙醛的产率,得到了kdis/kO2=(6.8±1.4)×1017,(2.3±0.5)×1018,和(5.5±1.1)×1018分子cm-3在279.8,298.2,和313.5 K,分别,导致Arrhenius表达式kdis/kO2=(2.0±0.5)×1026exp(-45.4 kJ mol-1/RT)分子cm-3在总压力为1巴。这个kdis/kO2的温度依赖性意味着,取决于温度,在较低对流层的条件下,要么是热分解,要么是与O2反应是2-丁氧基自由基的主要损失过程。使用文献中的kO2值,对于总压力为1巴(M=N2+O2),导出kdis=3.9×1012exp(-47.1 kJ mol-1/RT) s-1,这与Somnitz和Zellner的最近理论估计(从头计算+RRKM)非常吻合。
-
Formation of organic nitro-compounds in flowing H2O2+ NO2+ N2+ organic vapour systems. Part 2.—H2O2+ NO2+ N2+ alkane system作者:Donald L. Baulch、Ian M. Campbell、Jonathan M. ChappelDOI:10.1039/f19848000609日期:——The principal products from the surface-initiated reactions in flowing mixtures of H2O2, NO2, N2 and RH, where RH = ethane, propane, n-butane and n-pentane, have been identified as the nitroalkane, alkyl nitrite and alkyl nitrate. The product yields have been measured; in the case of propane the variation of the yields with total gas pressure has also been studied.
-
Formation of organic nitro-compounds in flowing H2O2+ NO2+ N2+ organic vapour systems. Part 3.—Effects of O2 addition on H2O2+ NO2+ N2+ alkane systems作者:Donald L. Baulch、Ian M. Campbell、Jonathan M. ChappelDOI:10.1039/f19848000617日期:——The effects of oxygen on the product distribution from the surface-initiated reactions in flowing mixtures of H2O2, NO2, N2 and RH, where RH = ethane, propane, n-butane and n-pentane, at 298 K have been studied. In the absence of O2, the principal products are the corresponding nitroalkane, alkyl nitrite and alkyl nitrate. In the presence of sufficiently large concentrations of O2, the predominant
-
Use of Perfluorocarboxylic Acids To Trick Cytochrome P450BM3 into Initiating the Hydroxylation of Gaseous Alkanes作者:Norifumi Kawakami、Osami Shoji、Yoshihito WatanabeDOI:10.1002/anie.201007975日期:2011.5.27It has long been believed that the fatty acid hydroxylase wild‐type P450BM3 is unable to oxidize gaseous alkanes. However, the simple addition of a perfluorocarboxylic acid as a dummy substrate to initiate the P450BM3 catalytic cycle enabled the efficient hydroxylation of butane and propane (see picture).
-
Gas-phase reactions of hydroxyl radicals with alkyl nitrite vapours in H2O2+ NO2+ CO mixtures作者:Gary J. Audley、Donald L. Baulch、Ian M. Campbell、Des J. Waters、Gillian WatlingDOI:10.1039/f19827800611日期:——The yields of CO2 from the chain reaction in H2O2+ NO2+ CO + alkyl nitrite mixtures, in which OH is the chain carrier and alkyl nitrites induce a chain termination step, have been used to deduce rate constants (ks) for OH attack on alkyl nitrites (RONO) in the vapour phase at ambient temperatures. Values of ks/109 dm3 mol–1 s–1 as a function of R were determined as follows: 0.71 ± 0.12 (CH3), 1.15H 2 O 2 + NO 2 + CO +亚硝酸烷基酯混合物中链反应的CO 2收率可用来推导速率常数(k s,其中OH是链载体,而亚硝酸烷基酯诱导了链终止步骤。),以防止在环境温度下气相中的OH侵蚀亚硝酸烷基酯(RONO)。确定k s / 10 9 dm 3 mol –1 s -1作为R的函数的值如下:0.71±0.12(CH 3),1.15±0.23(C 2 H 5),1.56±0.32(nC 3H 7),3.41±1.48(nC 4 H 9),3.89±0.58(sec-C 4 H 9),3.47±0.52(iC 4 H 9),0.91±0.15(tC 4 H 9),全部基于k s =(1.63±0.16)×10 9 dm 3 mol –1 s –1对于OH +正丁烷。从R = CH 3到tC 4 H 9的k s的小幅增加被认为支持最近的假设,即至少对于R = CH,H吸收和NO吸收途径均起作用。3。
表征谱图
-
氢谱1HNMR
-
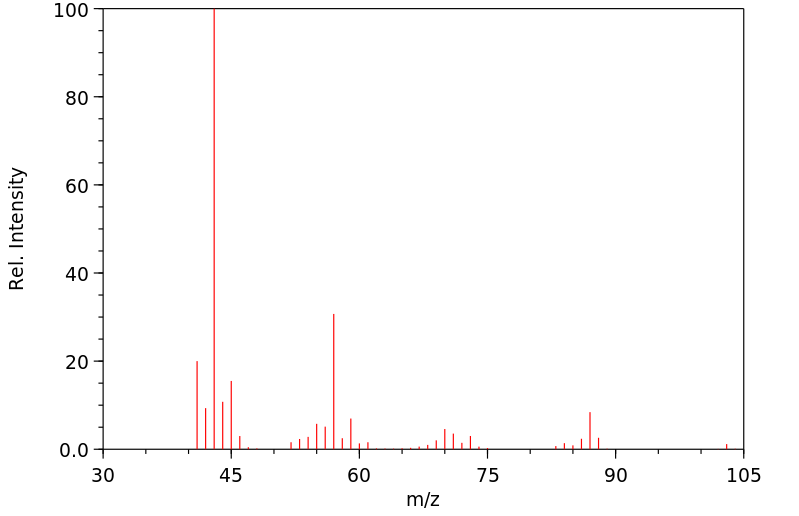
质谱MS
-
碳谱13CNMR
-
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息
同类化合物
(乙腈)二氯镍(II)
(R)-(-)-α-甲基组胺二氢溴化物
(N-(2-甲基丙-2-烯-1-基)乙烷-1,2-二胺)
(4-(苄氧基)-2-(哌啶-1-基)吡啶咪丁-5-基)硼酸
(11-巯基十一烷基)-,,-三甲基溴化铵
鼠立死
鹿花菌素
鲸蜡醇硫酸酯DEA盐
鲸蜡硬脂基二甲基氯化铵
鲸蜡基胺氢氟酸盐
鲸蜡基二甲胺盐酸盐
高苯丙氨醇
高箱鲀毒素
高氯酸5-(二甲氨基)-1-({(E)-[4-(二甲氨基)苯基]甲亚基}氨基)-2-甲基吡啶正离子
高氯酸2-氯-1-({(E)-[4-(二甲氨基)苯基]甲亚基}氨基)-6-甲基吡啶正离子
高氯酸2-(丙烯酰基氧基)-N,N,N-三甲基乙铵
马诺地尔
马来酸氢十八烷酯
马来酸噻吗洛尔EP杂质C
马来酸噻吗洛尔
马来酸倍他司汀
顺式环己烷-1,3-二胺盐酸盐
顺式氯化锆二乙腈
顺式吡咯烷-3,4-二醇盐酸盐
顺式双(3-甲氧基丙腈)二氯铂(II)
顺式3,4-二氟吡咯烷盐酸盐
顺式1-甲基环丙烷1,2-二腈
顺式-二氯-反式-二乙酸-氨-环己胺合铂
顺式-二抗坏血酸(外消旋-1,2-二氨基环己烷)铂(II)水合物
顺式-N,2-二甲基环己胺
顺式-4-甲氧基-环己胺盐酸盐
顺式-4-环己烯-1.2-二胺
顺式-4-氨基-2,2,2-三氟乙酸环己酯
顺式-3-氨基环丁烷甲腈盐酸盐
顺式-2-羟基甲基-1-甲基-1-环己胺
顺式-2-甲基环己胺
顺式-2-(苯基氨基)环己醇
顺式-2-(苯基氨基)环己醇
顺式-2-(氨基甲基)-1-苯基环丙烷羧酸盐酸盐
顺式-1,3-二氨基环戊烷
顺式-1,2-环戊烷二胺二盐酸盐
顺式-1,2-环戊烷二胺
顺式-1,2-环丁腈
顺式-1,2-双氨甲基环己烷
顺式--N,N'-二甲基-1,2-环己二胺
顺式-(R,S)-1,2-二氨基环己烷铂硫酸盐
顺式-(2-氨基-环戊基)-甲醇
顺-2-戊烯腈
顺-1,3-环己烷二胺
顺-1,3-双(氨甲基)环己烷