2-Benzamidoacetate
中文名称
——
中文别名
——
英文名称
2-Benzamidoacetate
英文别名
——
CAS
——
化学式
C9H8NO3-
mdl
——
分子量
178.16
InChiKey
QIAFMBKCNZACKA-UHFFFAOYSA-M
BEILSTEIN
——
EINECS
——
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
计算性质
-
辛醇/水分配系数(LogP):1
-
重原子数:13
-
可旋转键数:2
-
环数:1.0
-
sp3杂化的碳原子比例:0.11
-
拓扑面积:69.2
-
氢给体数:1
-
氢受体数:3
反应信息
-
作为反应物:描述:参考文献:名称:Enzymatic activity of Campylobacter jejuni hippurate hydrolase摘要:空肠弯曲杆菌的髙尿酸酯水解酶在大肠杆菌中以六组氨酸标签融合蛋白的形式表达。纯化的重组酶的特征有助于了解髙尿酸酯水解酶的结构和活性。重组酶的天然分子质量为193±11 kDa,还原分子质量为42.4±0.8 kDa,每个酶亚基分子含有1.98±0.68个锌原子,表明它是一种具有两个相关锌离子的同源四聚体。该酶是一种金属羧肽酶,对银、铜和亚铁离子敏感,在pH 7.5和50°C时表现出最佳活性。它可在体外水解羧肽酶底物,对N-苯甲酰连接的小脂肪族氨基酸表现出最高活性。该酶结构中很大一部分由高度有序的α-螺旋和β-片层序列组成。将髙尿酸酯水解酶的氨基酸序列与具有相似活性的相关酶的氨基酸序列进行比对,发现了几种保守氨基酸,它们可能参与酶的催化或金属离子结合。重组酶的定点突变表明,Asp76、Aps104、Glu134、Glu135、His161和His356位点对于酶的催化活性非常重要。DOI:10.1093/protein/gzi071
-
作为产物:描述:参考文献:名称:丙氨酸,谷氨酸和丝氨酸作为甘氨酸N-酰基转移酶的氨基酸底物的用途。摘要:研究了甘氨酸N-酰基转移酶与苯甲酰基辅酶A与脂肪族和酸性氨基酸的缀合以及后一组的酰胺。使用电喷雾电离串联质谱(ESI-MS-MS)研究了牛和人肝脏的苯甲酰氨基酸结合。牛甘氨酸N-酰基转移酶催化苯甲酰辅酶A与Gly(Km(Gly)= 6.2 mM),Asn(Km(Asn)= 129 mM),Gln(Km(Gln)= 353 mM),Ala(Km(Ala )= 1573 mM),Glu(Km(Glu)= 1148 mM)以及Ser处于顺序机制中。在人类形式的情况下,检测到与Gly(Km(Gly)= 6.4 mM),Ala(Km(Ala)= 997 mM)和Glu结合。这些替代缀合物的存在没有明显抑制牛甘氨酸N-酰基转移酶活性。考虑到形成这些结合物的水平相对较低,在体内正常条件下,它们不太可能对酰基氨基酸结合产生重大影响。然而,它们在代谢疾病状态下对酰基-氨基酸缀合的累积贡献可能证明对升高的酰基-CoA的解毒具有有益的贡献。DOI:10.1002/(sici)1099-0461(2000)14:2<102::aid-jbt6>3.0.co;2-h
文献信息
-
Enzymatic Characterization and Elucidation of the Catalytic Mechanism of a Recombinant Bovine Glycine<i>N</i>-Acyltransferase作者:Christoffel P. S. Badenhorst、Maritza Jooste、Alberdina A. van DijkDOI:10.1124/dmd.111.041657日期:2012.2Glycine conjugation, a phase II detoxification process, is catalyzed by glycine N -acyltransferase (GLYAT; E.C. 2.3.1.13). GLYAT detoxifies various xenobiotics, such as benzoic acid, and endogenous organic acids, such as isovaleric acid, which makes GLYAT important in the management of organic acidemias in humans. We cloned the open reading frame encoding the bovine ortholog of GLYAT from bovine liver mRNA into the bacterial expression vector pColdIII. The recombinant enzyme was expressed, partially purified, and enzymatically characterized. Protein modeling was used to predict Glu226 of bovine GLYAT to be catalytically important. This was assessed by constructing an E226Q mutant and comparing its enzyme kinetics to that of the wild-type recombinant bovine GLYAT. The Michaelis constants for benzoyl-CoA and glycine were determined and were similar for wild-type recombinant GLYAT, E226Q recombinant GLYAT, and GLYAT present in bovine liver. At pH 8.0, the E226Q mutant GLYAT had decreased activity, which could be compensated for by increasing the reaction pH. This suggested a catalytic mechanism in which Glu226 functions to deprotonate glycine, facilitating nucleophilic attack on the acyl-CoA. The recombinant bovine GLYAT enzyme, combined with this new understanding of its active site and reaction mechanism, could be a powerful tool to investigate the functional significance of GLYAT sequence variations. Eventually, this should facilitate investigations into the impact of known and novel sequence variations in the human GLYAT gene.甘氨酸缀合是 II 期解毒过程,由甘氨酸 N-酰基转移酶 (GLYAT;E.C. 2.3.1.13) 催化。 GLYAT 可以解毒各种外源性物质(例如苯甲酸)和内源性有机酸(例如异戊酸),这使得 GLYAT 在人类有机酸血症的治疗中发挥着重要作用。我们将牛肝脏 mRNA 中编码 GLYAT 的牛直系同源物的开放阅读框克隆到细菌表达载体 pColdIII 中。表达、部分纯化重组酶并进行酶学表征。使用蛋白质模型来预测牛 GLYAT 的 Glu226 具有重要的催化作用。这是通过构建 E226Q 突变体并将其酶动力学与野生型重组牛 GLYAT 的酶动力学进行比较来评估的。测定了苯甲酰辅酶A和甘氨酸的米氏常数,并且与野生型重组GLYAT、E226Q重组GLYAT和牛肝脏中存在的GLYAT相似。在 pH 8.0 时,E226Q 突变体 GLYAT 的活性降低,这可以通过提高反应 pH 值来补偿。这表明 Glu226 具有使甘氨酸去质子化的催化机制,促进对酰基辅酶 A 的亲核攻击。重组牛 GLYAT 酶,结合对其活性位点和反应机制的新认识,可能成为研究 GLYAT 序列变异功能意义的有力工具。最终,这将有助于研究人类 GLYAT 基因中已知和新的序列变异的影响。
-
Purification to Homogeneity of Mitochondrial Acyl CoA: Glycine N-Acyltransferase from Human Liver作者:Y.R. Mawal、I.A. QureshiDOI:10.1006/bbrc.1994.2817日期:1994.12Mitochondrial acyl CoA:glycine N-acyl transferase (ACGNAT) was purified to homogeneity from adult human liver. It was found to be a monomer of 30 kD, having a pI of 6.8. ACGNAT retained 47% of enzymatic activity at 100 mM NaCl concentration, whereas 21% of the activity was retained with KCl and 32% with K3PO4 at 100 mM concentration as compared to the control. The stability studies revealed no change线粒体酰基辅酶A:甘氨酸N-酰基转移酶(ACGNAT)从成年人类肝脏中纯化至同质。发现它是30kD的单体,pI为6.8。与对照相比,ACGNAT在100 mM NaCl浓度下保留了47%的酶活性,而在100 mM浓度下,使用KCl保留了21%的酶活性,使用K3PO4保留了32%的酶活性。稳定性研究表明,在4摄氏度下长达72小时,25摄氏度下4个小时以及在37摄氏度下1个小时的活性没有变化。人ACGNAT的苯甲酰基CoA,水杨酰基CoA,异戊酰基CoA和辛酰基CoA的Km值分别为57.9、83.7、124和198 mM,相应的Vmax值分别为17.1、10.1、7.64和3.3μmol/ min / mg蛋白质。
-
Nandi D.L.; Lucas S.V.; Webster L.T. Jr., J Biol Chem, 1979, 0021-9258, 7230-7作者:Nandi D.L.、Lucas S.V.、Webster L.T. Jr.DOI:——日期:——
-
[40] Benzoyl-CoA: Amino acid and phenylacetyl-CoA: Amino acid N-acyltransferases作者:Leslie T. WebsterDOI:10.1016/s0076-6879(81)77042-3日期:——
表征谱图
-
氢谱1HNMR
-
质谱MS
-
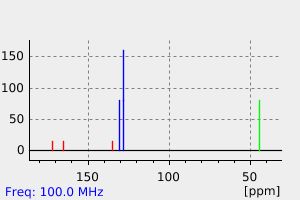
碳谱13CNMR
-
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息
同类化合物
(βS)-β-氨基-4-(4-羟基苯氧基)-3,5-二碘苯甲丙醇
(S,S)-邻甲苯基-DIPAMP
(S)-(-)-7'-〔4(S)-(苄基)恶唑-2-基]-7-二(3,5-二-叔丁基苯基)膦基-2,2',3,3'-四氢-1,1-螺二氢茚
(S)-盐酸沙丁胺醇
(S)-3-(叔丁基)-4-(2,6-二甲氧基苯基)-2,3-二氢苯并[d][1,3]氧磷杂环戊二烯
(S)-2,2'-双[双(3,5-三氟甲基苯基)膦基]-4,4',6,6'-四甲氧基联苯
(S)-1-[3,5-双(三氟甲基)苯基]-3-[1-(二甲基氨基)-3-甲基丁烷-2-基]硫脲
(R)富马酸托特罗定
(R)-(-)-盐酸尼古地平
(R)-(-)-4,12-双(二苯基膦基)[2.2]对环芳烷(1,5环辛二烯)铑(I)四氟硼酸盐
(R)-(+)-7-双(3,5-二叔丁基苯基)膦基7''-[((6-甲基吡啶-2-基甲基)氨基]-2,2'',3,3''-四氢-1,1''-螺双茚满
(R)-(+)-7-双(3,5-二叔丁基苯基)膦基7''-[(4-叔丁基吡啶-2-基甲基)氨基]-2,2'',3,3''-四氢-1,1''-螺双茚满
(R)-(+)-7-双(3,5-二叔丁基苯基)膦基7''-[(3-甲基吡啶-2-基甲基)氨基]-2,2'',3,3''-四氢-1,1''-螺双茚满
(R)-(+)-4,7-双(3,5-二-叔丁基苯基)膦基-7“-[(吡啶-2-基甲基)氨基]-2,2”,3,3'-四氢1,1'-螺二茚满
(R)-3-(叔丁基)-4-(2,6-二苯氧基苯基)-2,3-二氢苯并[d][1,3]氧杂磷杂环戊烯
(R)-2-[((二苯基膦基)甲基]吡咯烷
(R)-1-[3,5-双(三氟甲基)苯基]-3-[1-(二甲基氨基)-3-甲基丁烷-2-基]硫脲
(N-(4-甲氧基苯基)-N-甲基-3-(1-哌啶基)丙-2-烯酰胺)
(5-溴-2-羟基苯基)-4-氯苯甲酮
(5-溴-2-氯苯基)(4-羟基苯基)甲酮
(5-氧代-3-苯基-2,5-二氢-1,2,3,4-oxatriazol-3-鎓)
(4S,5R)-4-甲基-5-苯基-1,2,3-氧代噻唑烷-2,2-二氧化物-3-羧酸叔丁酯
(4S,4''S)-2,2''-亚环戊基双[4,5-二氢-4-(苯甲基)恶唑]
(4-溴苯基)-[2-氟-4-[6-[甲基(丙-2-烯基)氨基]己氧基]苯基]甲酮
(4-丁氧基苯甲基)三苯基溴化磷
(3aR,8aR)-(-)-4,4,8,8-四(3,5-二甲基苯基)四氢-2,2-二甲基-6-苯基-1,3-二氧戊环[4,5-e]二恶唑磷
(3aR,6aS)-5-氧代六氢环戊基[c]吡咯-2(1H)-羧酸酯
(2Z)-3-[[(4-氯苯基)氨基]-2-氰基丙烯酸乙酯
(2S,3S,5S)-5-(叔丁氧基甲酰氨基)-2-(N-5-噻唑基-甲氧羰基)氨基-1,6-二苯基-3-羟基己烷
(2S,2''S,3S,3''S)-3,3''-二叔丁基-4,4''-双(2,6-二甲氧基苯基)-2,2'',3,3''-四氢-2,2''-联苯并[d][1,3]氧杂磷杂戊环
(2S)-(-)-2-{[[[[3,5-双(氟代甲基)苯基]氨基]硫代甲基]氨基}-N-(二苯基甲基)-N,3,3-三甲基丁酰胺
(2S)-2-[[[[[((1S,2S)-2-氨基环己基]氨基]硫代甲基]氨基]-N-(二苯甲基)-N,3,3-三甲基丁酰胺
(2S)-2-[[[[[[((1R,2R)-2-氨基环己基]氨基]硫代甲基]氨基]-N-(二苯甲基)-N,3,3-三甲基丁酰胺
(2-硝基苯基)磷酸三酰胺
(2,6-二氯苯基)乙酰氯
(2,3-二甲氧基-5-甲基苯基)硼酸
(1S,2S,3S,5S)-5-叠氮基-3-(苯基甲氧基)-2-[(苯基甲氧基)甲基]环戊醇
(1S,2S,3R,5R)-2-(苄氧基)甲基-6-氧杂双环[3.1.0]己-3-醇
(1-(4-氟苯基)环丙基)甲胺盐酸盐
(1-(3-溴苯基)环丁基)甲胺盐酸盐
(1-(2-氯苯基)环丁基)甲胺盐酸盐
(1-(2-氟苯基)环丙基)甲胺盐酸盐
(1-(2,6-二氟苯基)环丙基)甲胺盐酸盐
(-)-去甲基西布曲明
龙蒿油
龙胆酸钠
龙胆酸叔丁酯
龙胆酸
龙胆紫-d6
龙胆紫