无水氯化铬(Ⅱ) | 10049-05-5
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
物化性质
-
熔点:824 °C(lit.)
-
沸点:1120°C (estimate)
-
密度:2.9 g/mL at 25 °C(lit.)
-
溶解度:溶于H2O
-
暴露限值:a/nm
-
物理描述:Chromous chloride appears as a white crystalline solid. The primary hazard is the threat to the environment. Immediate steps must be taken to prevent its spread to the environment. It is used to make other chemicals and as an oxygen absorbent.
-
颜色/状态:Lustrous needles or fused, fibrous mass
-
气味:Odorless
-
蒸汽压力:Essentially zero (except water of crystallization)
-
稳定性/保质期:
-
分解:When heated to decomposition it emits toxic vapors of /chromium/.
计算性质
-
辛醇/水分配系数(LogP):1.38
-
重原子数:3
-
可旋转键数:0
-
环数:0.0
-
sp3杂化的碳原子比例:0.0
-
拓扑面积:0
-
氢给体数:0
-
氢受体数:0
ADMET
安全信息
-
TSCA:Yes
-
危险品标志:Xn
-
安全说明:S26,S36
-
危险类别码:R36/37/38,R22
-
WGK Germany:3
-
海关编码:2827 39 85
-
危险品运输编号:UN3260
-
危险类别:8
-
RTECS号:GB5250000
-
包装等级:III
-
危险标志:GHS07
-
危险性描述:H302,H315,H319,H335
-
危险性防范说明:P261,P305 + P351 + P338
-
储存条件:请将产品存放在常温、密闭、避光、通风和干燥的地方。
SDS
模块 1. 化学品
1.1 产品标识符
: 氯化铬(II)
产品名称
1.2 鉴别的其他方法
无数据资料
1.3 有关的确定了的物质或混合物的用途和建议不适合的用途
仅用于研发。不作为药品、家庭或其它用途。
模块 2. 危险性概述
2.1 GHS-分类
急性毒性, 经口 (类别 4)
皮肤刺激 (类别 2)
眼睛刺激 (类别 2A)
特异性靶器官系统毒性(一次接触) (类别 3)
2.2 GHS 标记要素,包括预防性的陈述
象形图
警示词 警告
危险申明
H302 吞咽有害。
H315 造成皮肤刺激。
H319 造成严重眼刺激。
H335 可能引起呼吸道刺激。
警告申明
预防
P261 避免吸入粉尘/烟/气体/烟雾/蒸气/喷雾.
P264 操作后彻底清洁皮肤。
P270 使用本产品时不要进食、饮水或吸烟。
P271 只能在室外或通风良好之处使用。
P280 穿戴防护手套/ 眼保护罩/ 面部保护罩。
响应
P301 + P312 如果吞下去了:
如感觉不适,呼救解毒中心或看医生。如吞咽:如感觉不适,呼叫解毒中
心或就医。
P302 + P352 如皮肤接触:用大量肥皂和水清洗。
P304 + P340 如吸入: 将患者移到新鲜空气处休息,并保持呼吸舒畅的姿势。
P305 + P351 + P338 如与眼睛接触,用水缓慢温和地冲洗几分钟。如戴隐形眼镜并可方便地取
出,取出隐形眼镜,然后继续冲洗.
P312 如感觉不适,呼救中毒控制中心或医生.
P321 具体治疗(见本标签上提供的急救指导)。
P330 漱口。
P332 + P313 如发生皮肤刺激:求医/ 就诊。
P337 + P313 如仍觉眼睛刺激:求医/就诊。
P362 脱掉沾染的衣服,清洗后方可重新使用。
储存
P403 + P233 存放于通风良的地方。 保持容器密闭。
P405 存放处须加锁。
处置
P501 将内容物/ 容器处理到得到批准的废物处理厂。
2.3 其它危害物 - 无
模块 3. 成分/组成信息
3.1 物 质
: Cl2Cr
分子式
: 122.90 g/mol
分子量
组分 浓度或浓度范围
Chromium dichloride
-
化学文摘登记号(CAS 10049-05-5
No.) 233-163-3
EC-编号
模块 4. 急救措施
4.1 必要的急救措施描述
一般的建议
请教医生。 向到现场的医生出示此安全技术说明书。
吸入
如果吸入,请将患者移到新鲜空气处。 如呼吸停止,进行人工呼吸。 请教医生。
皮肤接触
用肥皂和大量的水冲洗。 请教医生。
眼睛接触
用大量水彻底冲洗至少15分钟并请教医生。
食入
切勿给失去知觉者通过口喂任何东西。 用水漱口。 请教医生。
4.2 主要症状和影响,急性和迟发效应
咳嗽, 呼吸短促, 头痛, 恶心, 呕吐
4.3 及时的医疗处理和所需的特殊处理的说明和指示
无数据资料
模块 5. 消防措施
5.1 灭火介质
灭火方法及灭火剂
用水雾,抗乙醇泡沫,干粉或二氧化碳灭火。
5.2 源于此物质或混合物的特别的危害
氯化氢气体, 铬的氧化物
5.3 给消防员的建议
如必要的话,戴自给式呼吸器去救火。
5.4 进一步信息
无数据资料
模块 6. 泄露应急处理
6.1 作业人员防护措施、防护装备和应急处置程序
使用个人防护用品。 避免粉尘生成。 避免吸入蒸气、烟雾或气体。 保证充分的通风。
人员疏散到安全区域。 避免吸入粉尘。
6.2 环境保护措施
不要让产品进入下水道。
6.3 泄漏化学品的收容、清除方法及所使用的处置材料
收集和处置时不要产生粉尘。 扫掉和铲掉。 放入合适的封闭的容器中待处理。
6.4 参考其他部分
丢弃处理请参阅第13节。
模块 7. 操作处置与储存
7.1 安全操作的注意事项
避免接触皮肤和眼睛。 避免形成粉尘和气溶胶。
在有粉尘生成的地方,提供合适的排风设备。一般性的防火保护措施。
7.2 安全储存的条件,包括任何不兼容性
贮存在阴凉处。 使容器保持密闭,储存在干燥通风处。
7.3 特定用途
无数据资料
模块 8. 接触控制和个体防护
8.1 容许浓度
最高容许浓度
没有已知的国家规定的暴露极限。
8.2 暴露控制
适当的技术控制
根据良好的工业卫生和安全规范进行操作。 休息前和工作结束时洗手。
个体防护设备
眼/面保护
带有防护边罩的安全眼镜符合 EN166要求请使用经官方标准如NIOSH (美国) 或 EN 166(欧盟)
检测与批准的设备防护眼部。
皮肤保护
戴手套取 手套在使用前必须受检查。
请使用合适的方法脱除手套(不要接触手套外部表面),避免任何皮肤部位接触此产品.
使用后请将被污染过的手套根据相关法律法规和有效的实验室规章程序谨慎处理. 请清洗并吹干双手
所选择的保护手套必须符合EU的89/686/EEC规定和从它衍生出来的EN 376标准。
完全接触
联合国运输名称: 丁腈橡胶
最小的层厚度 0.11 mm
溶剂渗透时间: 480 min
测试过的物质Dermatril® (KCL 740 / Z677272, 规格 M)
飞溅保护
联合国运输名称: 丁腈橡胶
最小的层厚度 0.11 mm
溶剂渗透时间: 480 min
测试过的物质Dermatril® (KCL 740 / Z677272, 规格 M)
, 测试方法 EN374
如果以溶剂形式应用或与其它物质混合应用,或在不同于EN
374规定的条件下应用,请与EC批准的手套的供应商联系。
这个推荐只是建议性的,并且务必让熟悉我们客户计划使用的特定情况的工业卫生学专家评估确认才可.
这不应该解释为在提供对任何特定使用情况方法的批准.
身体保护
全套防化学试剂工作服, 防护设备的类型必须根据特定工作场所中的危险物的浓度和数量来选择。
呼吸系统防护
如须暴露于有害环境中,请使用P95型(美国)或P1型(欧盟 英国
143)防微粒呼吸器。如需更高级别防护,请使用OV/AG/P99型(美国)或ABEK-P2型 (欧盟 英国 143)
防毒罐。
呼吸器使用经过测试并通过政府标准如NIOSH(US)或CEN(EU)的呼吸器和零件。
模块 9. 理化特性
9.1 基本的理化特性的信息
a) 外观与性状
形状: 粉末
颜色: 灰色
b) 气味
无数据资料
c) 气味阈值
无数据资料
d) pH值
无数据资料
e) 熔点/凝固点
熔点/凝固点: 824 °C - lit.
f) 沸点、初沸点和沸程
无数据资料
g) 闪点
不适用
h) 蒸发速率
无数据资料
i) 易燃性(固体,气体)
无数据资料
j) 高的/低的燃烧性或爆炸性限度 无数据资料
k) 蒸气压
无数据资料
l) 蒸汽密度
无数据资料
m) 密度/相对密度
2.9 g/cm3 在 25 °C
n) 水溶性
无数据资料
o) n-辛醇/水分配系数
无数据资料
p) 自燃温度
无数据资料
q) 分解温度
无数据资料
r) 粘度
无数据资料
模块 10. 稳定性和反应活性
10.1 反应性
无数据资料
10.2 稳定性
无数据资料
10.3 危险反应
无数据资料
10.4 应避免的条件
无数据资料
10.5 不相容的物质
氧化剂
10.6 危险的分解产物
其它分解产物 - 无数据资料
模块 11. 毒理学资料
11.1 毒理学影响的信息
急性毒性
半数致死剂量 (LD50) 经口 - 大鼠 - 1,870 mg/kg
皮肤刺激或腐蚀
无数据资料
眼睛刺激或腐蚀
无数据资料
呼吸道或皮肤过敏
无数据资料
生殖细胞突变性
无数据资料
致癌性
IARC:
此产品中没有大于或等于 0。1%含量的组分被 IARC鉴别为可能的或肯定的人类致癌物。
生殖毒性
无数据资料
特异性靶器官系统毒性(一次接触)
吸入 - 可能引起呼吸道刺激。
特异性靶器官系统毒性(反复接触)
无数据资料
吸入危险
无数据资料
潜在的健康影响
吸入 吸入可能有害。 引起呼吸道刺激。
摄入 误吞对人体有害。
皮肤 通过皮肤吸收可能有害。 造成皮肤刺激。
眼睛 造成严重眼刺激。
接触后的征兆和症状
咳嗽, 呼吸短促, 头痛, 恶心, 呕吐
附加说明
化学物质毒性作用登记: GB5250000
模块 12. 生态学资料
12.1 生态毒性
对水蚤和其他水生无脊 半数致死浓度(LC50) - 大型蚤 (水蚤) - 21.531 mg/l - 48 h
椎动物的毒性
12.2 持久性和降解性
无数据资料
12.3 潜在的生物累积性
无数据资料
12.4 土壤中的迁移性
无数据资料
12.5 PBT 和 vPvB的结果评价
无数据资料
12.6 其它不良影响
无数据资料
模块 13. 废弃处置
13.1 废物处理方法
产品
将剩余的和不可回收的溶液交给有许可证的公司处理。
联系专业的拥有废弃物处理执照的机构来处理此物质。
与易燃溶剂相溶或者相混合,在备有燃烧后处理和洗刷作用的化学焚化炉中燃烧
受污染的容器和包装
按未用产品处置。
模块 14. 运输信息
14.1 联合国危险货物编号
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.2 联合国运输名称
欧洲陆运危规: 非危险货物
国际海运危规: 非危险货物
国际空运危规: 非危险货物
14.3 运输危险类别
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.4 包裹组
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.5 环境危险
欧洲陆运危规: 否 国际海运危规 国际空运危规: 否
海洋污染物(是/否): 否
14.6 对使用者的特别提醒
无数据资料
模块 15 - 法规信息
N/A
模块16 - 其他信息
N/A
制备方法与用途
氯化铬,化学式为CrCl₃。分子量158.36,为深绿色结晶粉末,易溶于水和乙醇,不溶于乙醚。与水长时间沸腾后形成绿色溶液,加热分解时会变成三氧化二铬。在氯气流中升华,400℃下与四氯化碳共热可得到动力学惰性的紫色无水物。六水合物有深绿、浅绿和紫三种变体,在水中变为深绿和紫混合物,但在DMF、乙醇等有机溶剂中呈现墨绿色。
高温下由三氧化二铬与碳粉的混合物在氯气作用或盐酸与氢氧化铬反应制得。主要用于制取其他铬盐、媒染剂、颜料及镀铬等领域。
结构特性氯化铬是较硬的路易斯酸,含d³构型三价铬,在配体置换反应中惰性。可通过加入少量还原剂(如锌/盐酸)将其还原为亚铬化合物,再通过氯桥发生电子转移生成相应的配合物,并恢复部分活性Cr(II)。
化学性质又名三氯化铬,紫色三方晶体,相对密度2.76 (15/4℃),在950℃升华并在1300℃以上开始离解。六水合物为深绿色晶体,潮解性,相对密度1.84(7.5/4℃),熔点83℃;十水合物是绿色粉末,相对密度1.76。三种物质均溶于水和乙醇而不溶于乙醚,在空气中灼烧后变为三氧化二铬。
通过在600℃下氯气与氧化铬碳混合物或盐酸氢氧化铬反应制备。用于分析试剂、织物媒染剂、烯烃聚合催化剂,以及其他铬盐的制备和镀铬溶液原料等用途。
用途主要用于制铬盐、镀铬及作为媒染剂。可将末端烯烃高效转化成反式碘代环丙烷,并用于合成乙烯低聚反应所需的高活性预催化剂。在氢作用下与其他金属卤化物气相共还原生成精细的金属互化物,用作热电性、磁性和抗氧化性的结构材料或化合物。
生产方法-
无水三氯化铬在干燥氯气或氯化氢气流中于800℃升华精制。低温时先升华的杂质(如三氯化铁)可清除,使用25mm直径、长500mm的一端封闭石英管或超硬质玻璃管作为反应器,在出口附近拉成缩颈以便封口。硅橡胶塞开两个孔,并插入导气和排气管。加热至500℃后减压干燥。将反应管横放,加入氯化铬并封闭。
-
方法一:10克锌粉、0.8克氯化汞与10毫升水及0.5毫升浓盐酸混合激烈振荡5分钟后倾出上层清液留下锌汞齐粉。另加20毫升水和2毫升浓盐酸,通入二氧化碳气体后分批加入5克氯化铬得到蓝黑色溶液。
-
方法二:5克六水合氯化铬溶于含有2.0毫升浓盐酸的35毫升绝对乙醇中,在二氧化碳气存在下过滤到装有锌汞齐粉的Jones还原管中,所得溶液封存于内含1克锌汞齐粉的玻璃瓶。
有毒物质
毒性分级中毒
急性毒性口服 - 大鼠 LD₅₀: 1870 毫克/公斤
可燃性危险特性可燃烧;火场产生有毒含铬化合物烟雾。
储运特性低温库房,通风、干燥环境储存运输。
灭火剂 职业标准TWA 0.5 毫克(铬)/立方米。
上下游信息
反应信息
-
作为反应物:描述:无水氯化铬(Ⅱ) 、 2-(N,N-dimethylaminomethyl)phenyllithium 以 四氢呋喃 、 甲苯 、 正戊烷 为溶剂, 生成 bis(2-dimethylaminomethylphenyl)chromium参考文献:名称:2-Dialkylaminobenzyl and 2-dialkylaminomethylphenyl derivatives of摘要:过渡金属化合物的化学式为M.sup.1 A.sub.3(1),其中M.sup.1是钪、钇、铬或稀土金属,A是2-二烷基氨基苯甲基或2-二烷基氨基甲基苯基,或其低烷基衍生物,M.sup.2 A.sub.2(2),其中M.sup.2是铬或钼,M.sup.3 A.sub.4(3),其中M.sup.3是钛、锆或铪,可作为配位催化剂的组分用于烯烃聚合。化学式为LiA的锂化合物是制备上述化合物所用的中间体。所有上述化合物也可用作氧气清除剂。公开号:US04057565A1
-
作为产物:参考文献:名称:摘要:DOI:
-
作为试剂:描述:碘仿 、 (2Z)-2-[(3'aS,7'aS)-7'a-methylspiro[1,3-dioxolane-2,5'-2,3,3a,4,6,7-hexahydroindene]-1'-ylidene]propanal 在 无水氯化铬(Ⅱ) 作用下, 以76%的产率得到(1Z,3aS,7aS)-1-(4-iodobut-3-en-2-ylidene)-7a-methyloctahydrospiro[indene-5,2'-[1,3]dioxolane]参考文献:名称:Synthesis of BC-ring model of globostellatic acid X methyl ester, an anti-angiogenic substance from marine sponge摘要:Concise synthesis of BC-ring model compounds of 13E, 17E-globostellatic acid X methyl ester, an anti-angiogenic triterpene derivative from Indonesian marine sponge, was achieved through ynolate olefination and allylic oxidation as key steps. The model compound 5, which was synthesized within 10 reaction steps from commercially available Hajos-Parrish ketone, showed anti-proliferative activity against HUVECs with moderate selectivity. (C) 2008 Elsevier Ltd. All rights reserved.DOI:10.1016/j.bmcl.2008.05.018
文献信息
-
Therapeutic compounds申请人:——公开号:US20040102435A1公开(公告)日:2004-05-27Compounds of the formula (I) for use as an estrogen receptor-&bgr;-selective ligand are described wherein: X is O or S; and R 1 , R 3 R 6 are as described in the specification. The use of these compounds in treating Alzheimer's disease, anxiety disorders, depressive disorders, osteoporosis, cardiovascular disease, rheumatoid arthritis and prostate cancer is described; as are processes for making them.
-
Alpha substituted carboxylic acids申请人:Su Guo Wei公开号:US20050187266A1公开(公告)日:2005-08-25Alpha substituted carboxylic acids of formula (I): wherein R 1 and R 2 are as defined in the specification and R 3 is wherein Y, Ar 1 , Ar 2 , Ar 3 , R 4 , R 5 , R 6 , R 7 , R 8 , R 9 , R 9a , R 10 , R 11 , R 12 , R 17 , ring A, and p are as defined in the specification; pharmaceutical compositions containing effective amounts of said compounds or their salts are useful for treating PPAR, specifically PPAR α/γ related disorders, such as diabetes, dyslipidemia, obesity and inflammatory disorders.
-
9.alpha.-hydroxy-17-methylene steroids, process for their preparation申请人:Gist-Brocades N.V.公开号:US05194602A1公开(公告)日:1993-03-16New 9.alpha.-hydroxy-17-methylene steroids are prepared by the introduction of a substituted 17-methylene group in 9.alpha.-hydroxyandrost-4-ene-3, 17-dione. The resulting compounds are useful starting compounds in the synthesis of corticosteroids.
-
Process for trimerization申请人:Union Carbide Corporation公开号:US04668838A1公开(公告)日:1987-05-26A process for the trimerization of an olefin selected from the group consisting of ethylene, propylene, 1-butene, and mixtures thereof comprising passing the olefin in contact with a catalyst comprising the reaction product of (i) a chromium compound, which will provide active catalytic species under trimerization conditions; (ii) a hydrocarbyl aluminum hydrolyzed with about 0.8 to about 1.1 moles of water per mole of aluminum compound; and (iii) a donor ligand selected from the group consisting of hydrocarbyl isonitriles, amines, and ethers wherein the aluminum to chromium mole ratio is in the range of up to about 200 to one and the ligand to chromium mole ratio is in the range of up to about 100 to one.
-
Cr complexes and their use for the polymerization of alpha-olefins申请人:——公开号:US20040044149A1公开(公告)日:2004-03-04The invention concerns a chromium complex corresponding to formula (I) wherein: each X is, independently, selected from the group of halogen, alkoxide, aryloxide, amide, phosphide, hydride, hydrocarbyl or substituted hydrocarbyl; each L is, independently, a neutral elecron donor group which stabilizes the complex; n is 2 or 3; p is a number from 0 to 3; R1, R2, R3, R4 and R5 are, independently, hydrogen, hydrocarbyl, substituted hydrocarbyl; R6 and R7 are, independently, substituted ary groups; and its use for the polymerization of alpha-olefins.
表征谱图
-
氢谱1HNMR
-
质谱MS
-
碳谱13CNMR
-
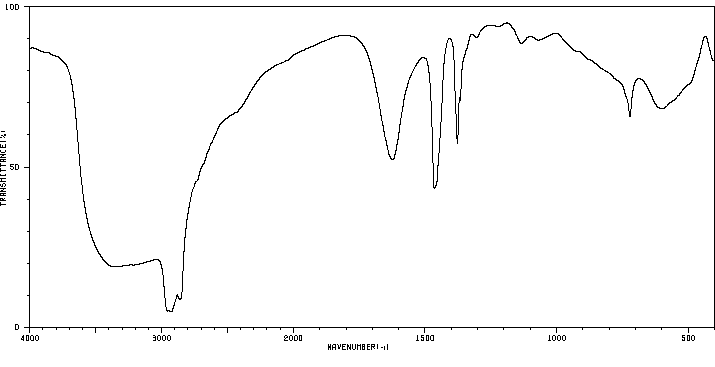
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息