3-phenyl-4-(1-phenylmethylidene)-5-isoxazolone | 36298-61-0
中文名称
——
中文别名
——
英文名称
3-phenyl-4-(1-phenylmethylidene)-5-isoxazolone
英文别名
4-benzylidene-3-phenylisoxazol-5(4H)-one;3-Phenyl-4-benzalisoxazolin-5-one;4-benzylidene-3-phenyl-1,2-oxazol-5-one
CAS
36298-61-0
化学式
C16H11NO2
mdl
——
分子量
249.269
InChiKey
DBPNBHOCUSFGKI-UHFFFAOYSA-N
BEILSTEIN
——
EINECS
——
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
物化性质
-
沸点:386.5±45.0 °C(Predicted)
-
密度:1.16±0.1 g/cm3(Predicted)
计算性质
-
辛醇/水分配系数(LogP):3.9
-
重原子数:19
-
可旋转键数:2
-
环数:3.0
-
sp3杂化的碳原子比例:0.0
-
拓扑面积:38.7
-
氢给体数:0
-
氢受体数:3
安全信息
-
海关编码:2934999090
SDS
上下游信息
-
上游原料
中文名称 英文名称 CAS号 化学式 分子量 3-苯基-5-异噁唑酮 3-phenyl-4H-isoxazol-5-one 1076-59-1 C9H7NO2 161.16 -
下游产品
中文名称 英文名称 CAS号 化学式 分子量 —— 3-phenyl-4-(3-phenylallylidene)isoxazol-5(4H)-one —— C18H13NO2 275.307
反应信息
-
作为反应物:描述:3-phenyl-4-(1-phenylmethylidene)-5-isoxazolone 在 ferrous(II) sulfate heptahydrate 、 scandium tris(trifluoromethanesulfonate) 、 sodium nitrite 作用下, 以 二氯甲烷 、 水 、 溶剂黄146 为溶剂, 反应 22.5h, 生成 methyl 3,5-diphenylpent-4-ynoate参考文献:名称:亚烷基异恶唑-5-酮的软碳亲核试剂的迈克尔加成:β分支羰基化合物的不同条目。摘要:通过利用亚烷基异恶唑-5-酮作为主要结构单元,开发了一种新的,发散的合成β-支化(和线性)羰基化合物的策略。获得的收率范围从良好到优异,因此使得所述方法成为构建此类分子的有吸引力的选择。DOI:10.1021/acs.orglett.5b01004
-
作为产物:描述:参考文献:名称:Fast and Efficient Synthesis of 4-Arylidene-3-phenylisoxazol-5-ones摘要:报道了在回流乙醇中,通过羟胺、乙基苯甲酰乙酸酯和芳香醛的三组分反应,在DABCO存在下,方便且易于合成4-芳基亚甲基-3-苯基异噁唑-5-酮。DOI:10.1155/2012/562138
文献信息
-
Facile and expedient synthesis of α,β-unsaturated isoxazol-5(4H)-ones under mild conditions作者:Fatemeh Ghorbani、Hamzeh Kiyani、Seied Ali PourmousaviDOI:10.1007/s11164-019-03999-7日期:2020.1three-component cyclocondensation of aryl/heteroaryl aldehydes, hydroxylamine hydrochloride, and β -ketoesters toward the synthesis of α , β -unsaturated isoxazol-5(4 H )-ones under green conditions. The reaction yielded the corresponding heterocycles at room temperature in relatively shorter reaction times. It merits mentioning that the mild conditions allow the synthesis of several α , β -unsaturated isoxazol-5(4
-
<i>cis</i>-Selective, Enantiospecific Addition of Donor–Acceptor Cyclopropanes to Activated Alkenes: An Iodination/Michael-Cyclization Cascade作者:Nils L. Ahlburg、Peter G. Jones、Daniel B. WerzDOI:10.1021/acs.orglett.0c02210日期:2020.8.21biologically interesting scaffolds, including barbiturates and isoxazolones. Mechanistic investigations were undertaken to explain the unusual diastereoselectivity and enantiospecificity; these suggest an iodination/Michael-cyclization cascade.
-
A convergent approach to functionalised alkynes作者:Jean Boivin、Sylvain Huppé、Samir Z ZardDOI:10.1016/s0040-4039(96)02015-1日期:1996.11Knoevenagel type condensation of 4-unsubstituted isoxazolinones with ketones or aldehydes followed by Michael addition of a nucleophile — hydride, cyanide, or phosphite— and exposure of the adduct to sodium nitrite/aqueous acetic acid and ferrous sulfate gives variously functionalised alkynes.
-
Regioselective Catalytic Asymmetric C-Alkylation of Isoxazolinones by a Base-Free Palladacycle-Catalyzed Direct 1,4-Addition作者:Tina Hellmuth、Wolfgang Frey、René PetersDOI:10.1002/anie.201410933日期:2015.2.23asymmetric alkylations of isoxazolinones forming all‐C‐substituted quaternary stereocenters. The present studies were driven by the question of how to control the regioselectivity in the competition of different nucleophilic positions. The investigation of a direct 1,4‐addition uncovered that a sterically demanding palladacycle catalyst directs the reactivity in the absence of a base nearly exclusively to
-
Reaction of 4-arylmethylene-3-phenylisoxazolones and 4-arylmethylene-1,3-diphenylpyrazolones with enamines and nucleophilic heterocycles作者:David C. Cook、Alexander LawsonDOI:10.1039/p19740001112日期:——4-Arylmethylene-3-phenylisoxazolones (1) and 4-arylmethylene-1,3-diphenylpyrazolones (2) were treated with enamines (8), 3-phenylisoxazol-5(4H)-one (4), 1,3-diphenylpyrazol-5(4H)-one (6), and 2-phenyloxazol-5(4H)-one (3). The enamines were β-alkylated to give 1:1 adducts (9) and (10). The reaction of (1) with (6) and (2) with (4) gave symmetrical benzylidenedi-isoxazolones and -pyrazolones (7). 2-
表征谱图
-
氢谱1HNMR
-
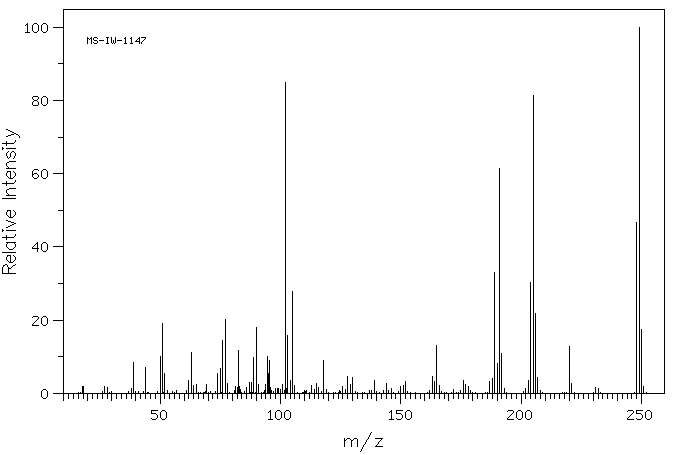
质谱MS
-
碳谱13CNMR
-
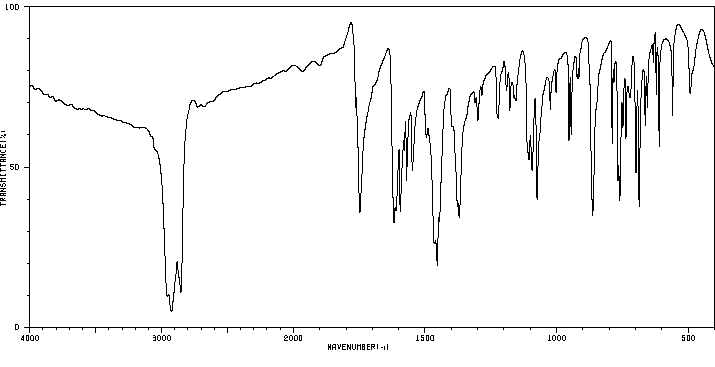
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息
同类化合物
(4S,4''S)-2,2''-环亚丙基双[4-叔丁基-4,5-二氢恶唑]
香豆素-6-羧酸
顺式-3a,5,6,6a-四氢-3-(1-甲基乙基)-4H-环戊二烯并[d]异恶唑
锌离子载体IV
钐(III) 离子载体 II
苯,1-(2E)-2-丁烯-1-基-2-氟-
苯,(2,2-二氟乙烯基)-
聚二硫二噻唑烷
缩胆囊肽9
绕丹酸钠
盐(1:?)5'-尿苷酸,钠
甲酰乙内脲
甲巯咪唑
甲基羟甲基油基噁唑啉
甲基5-羟基-3,5-二甲基-4,5-二氢-1H-吡唑-1-羧酸酯
甲基5-甲基-4,5-二氢-1H-吡唑-3-羧酸酯
甲基5-甲基-4,5-二氢-1H-吡唑-1-羧酸酯
甲基5-氰基-4,5-二氢-1,2-恶唑-3-羧酸酯
甲基5-乙炔基-4,5-二氢-1H-吡唑-3-羧酸酯
甲基5-(羟基甲基)-4,5-二氢-1,2-恶唑-3-羧酸酯
甲基4-甲基-5-氧代-4,5-二氢-1H-吡唑-3-羧酸酯
甲基4-甲基-4,5-二氢-1H-吡唑-3-羧酸酯
甲基4-乙炔基-4,5-二氢-1H-吡唑-3-羧酸酯
甲基4,5-二氮杂螺[2.4]庚-5-烯-6-羧酸酯
甲基4,5-二氢-5-乙基-1H-吡唑-1-羧酸酯
甲基3-甲基-4,5-二氢-1,2-恶唑-4-羧酸酯
甲基(E)-3-[6-[1-羟基-1-(4-甲基苯基)-3-(1-吡咯烷基)丙基]-2-吡啶基]丙烯酰酸酯
甲基(5-氧代-4,5-二氢-1,2-恶唑-3-基)乙酸酯
环戊二烯并[d]咪唑-2,5(1H,3H)-二硫酮
环己羧酸,3-氨基-2-甲氧基-,甲基酯,(1S,2S,3S)-
溶剂黄93
溴化1-十六烷基-3-甲基咪唑
溴化1-十二烷基-2,3-二甲基咪唑
泰比培南酯中间体
泰比培南酯中间体
氨甲酸,[4,5-二氢-4-(碘甲基)-2-噻唑基]-,1,1-二甲基乙基酯(9CI)
氨基甲硫酸,[2-[[(2-羰基-1-咪唑烷基)硫代甲基]氨基]乙基]-,O-甲基酯
异噻唑,4,5-二氯-2,5-二氢-2-辛基-
希诺米啉
四氟硼酸二氢1,3-二(叔-丁基)-4,5--1H-咪唑正离子
四唑硝基紫
噻唑烷-2,4-二酮-2-缩氨基脲
噻唑丁炎酮
噻唑,4,5-二氢-4-(1-甲基乙基)-,(S)-
噁唑,4,5-二氢-4,4-二甲基-2-(5-甲基-2-呋喃基)-
噁唑,2-庚基-4,5-二氢-
咪唑烷基脲
吡嗪,2,3-二氢-5,6-二甲基-2-丙基-
叔-丁基3-羟基-1,4,6,7-四氢吡唑并[4,3-c]吡啶-5-羧酸酯
双吡唑啉酮