3-benzyl-1-phenyl-5-pyrazolone | 26645-09-0
中文名称
——
中文别名
——
英文名称
3-benzyl-1-phenyl-5-pyrazolone
英文别名
5-benzyl-2-phenyl-4H-pyrazol-3-one
CAS
26645-09-0
化学式
C16H14N2O
mdl
——
分子量
250.3
InChiKey
YAKFVICLDYQJRX-UHFFFAOYSA-N
BEILSTEIN
——
EINECS
——
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
物化性质
-
熔点:135-136 °C
-
沸点:445.7±24.0 °C(Predicted)
-
密度:1.15±0.1 g/cm3(Predicted)
计算性质
-
辛醇/水分配系数(LogP):2.9
-
重原子数:19
-
可旋转键数:3
-
环数:3.0
-
sp3杂化的碳原子比例:0.12
-
拓扑面积:32.7
-
氢给体数:0
-
氢受体数:2
反应信息
-
作为反应物:参考文献:名称:含多药基双螺三杂环支架的不对称构建和人类羧基酯酶1抑制剂的鉴定。摘要:开发了新型4-异硫氰酸根并吡唑酮和伊斯汀衍生的酮亚胺的催化不对称[3 + 2]环化反应,以高收率提供了多种引人入胜的双螺三杂环产品,具有出色的非对映选择性和对映选择性。该双螺环产物的手性亚砜衍生物被认为是人羧化酶1抑制剂的有前途的产物,并且两种对映异构体之间活性的显着差异强调了这种不对称过程的重要性。DOI:10.1021/acs.orglett.8b01316
-
作为产物:参考文献:名称:BERTHOLD, R.摘要:DOI:
文献信息
-
Zinc chloride catalyzed stereoselective construction of spiropyrazolone tetrahydroquinolines via tandem [1,5]-hydride shift/cyclization sequence作者:Tuan Zhao、Huanrui Zhang、Longchen Cui、Jingping Qu、Baomin WangDOI:10.1039/c5ra18471a日期:——A zinc chloride catalyzed tandem 1,5-hydride shift/cyclization process to form spiropyrazolone terahydroquinoline derivatives is developed. A series of new spiropyrazolone derivatives were obtained in good to high yields with good to excellent diastereoselectivities (up to 95% yield, >95 : 5 dr). Additionally, the spiropyrazolone derivatives could be converted into the corresponding novel spriopyrazolines
-
New Series of Antiprion Compounds: Pyrazolone Derivatives Have the Potent Activity of Inhibiting Protease-Resistant Prion Protein Accumulation作者:Ayako Kimata、Hidehiko Nakagawa、Ryo Ohyama、Tomoko Fukuuchi、Shigeru Ohta、Takayoshi Suzuki、Naoki MiyataDOI:10.1021/jm070688r日期:2007.10.1To find effective antiprion compounds, we synthesized and evaluated various pyrazolone derivatives. Seven of 19 compounds showed inhibition of PrP-res accumulation and the remarkably active compound 13 showed an IC50 value of 3 nM in both ScN2a and F3 cell lines. Findings from studies on physicochemical and biochemical properties suggest that the action mechanism of these compounds does not correlate
-
Synthesis of pyranopyrazoles with a chiral quaternary carbon stereocenter <i>via</i> copper-catalyzed enantioselective [3 + 3] cycloaddition作者:Meihui Wang、Bo Li、Baihui Gong、Hequan Yao、Aijun LinDOI:10.1039/d1cc07058d日期:——A copper-catalyzed enantioselective [3 + 3] cycloaddition of propargyl carbonates and pyrazolones has been disclosed. This reaction provided an efficient route to synthesize pyranopyrazoles containing a chiral quaternary carbon stereocenter in good yields with good to excellent enantioselectivities. In addition, the hydroxyl group in the products could be conveniently transformed into a variety of
-
Enantioselective Synthesis of Spirorhodanine-Pyran Derivatives via Organocatalytic [3 + 3] Annulation Reactions between Pyrazolones and Rhodanine-Derived Ketoesters作者:Dong-Sheng Ji、Yong-Chun Luo、Xiu-Qin Hu、Peng-Fei XuDOI:10.1021/acs.orglett.9b04571日期:2020.2.7A series of novel biselectrophilic β,γ-unsaturated α-ketoesters were designed and synthesized from rhodanine. Under the catalysis of chiral squaramides, the enantioselective [3 + 3] annulation reaction of these novel ketoesters with pyrazolones was developed. This reaction offers an efficient method for the synthesis of chiral 2'-thioxo-5,6-dihydrospiro[pyrano[2,3-c]pyrazole-4,5'-thiazolidin]-4'-ones
-
An Organocatalytic Asymmetric Friedel–Crafts Addition/Fluorination Sequence: Construction of Oxindole–Pyrazolone Conjugates Bearing Vicinal Tetrasubstituted Stereocenters作者:Xiaoze Bao、Baomin Wang、Longchen Cui、Guodong Zhu、Yuli He、Jingping Qu、Yuming SongDOI:10.1021/acs.orglett.5b02470日期:2015.11.6A highly efficient and practical one-pot sequential process, consisting of an organocatalytic enantioselective Friedel–Crafts-type addition of 4-nonsubstituted pyrazolones to isatin-derived N-Boc ketimines and a subsequent diastereoselective fluorination of the pyrazolone moiety, is developed. This reaction sequence delivers novel oxindole–pyrazolone adducts featuring vicinal tetrasubstituted stereocenters
表征谱图
-
氢谱1HNMR
-
质谱MS
-
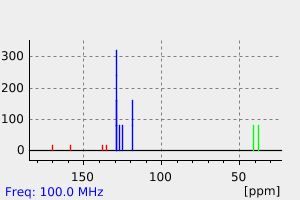
碳谱13CNMR
-
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息
同类化合物
(4S,4''S)-2,2''-环亚丙基双[4-叔丁基-4,5-二氢恶唑]
香豆素-6-羧酸
顺式-3a,5,6,6a-四氢-3-(1-甲基乙基)-4H-环戊二烯并[d]异恶唑
锌离子载体IV
钐(III) 离子载体 II
苯,1-(2E)-2-丁烯-1-基-2-氟-
苯,(2,2-二氟乙烯基)-
聚二硫二噻唑烷
缩胆囊肽9
绕丹酸钠
盐(1:?)5'-尿苷酸,钠
甲酰乙内脲
甲巯咪唑
甲基羟甲基油基噁唑啉
甲基5-羟基-3,5-二甲基-4,5-二氢-1H-吡唑-1-羧酸酯
甲基5-甲基-4,5-二氢-1H-吡唑-3-羧酸酯
甲基5-甲基-4,5-二氢-1H-吡唑-1-羧酸酯
甲基5-氰基-4,5-二氢-1,2-恶唑-3-羧酸酯
甲基5-乙炔基-4,5-二氢-1H-吡唑-3-羧酸酯
甲基5-(羟基甲基)-4,5-二氢-1,2-恶唑-3-羧酸酯
甲基4-甲基-5-氧代-4,5-二氢-1H-吡唑-3-羧酸酯
甲基4-甲基-4,5-二氢-1H-吡唑-3-羧酸酯
甲基4-乙炔基-4,5-二氢-1H-吡唑-3-羧酸酯
甲基4,5-二氮杂螺[2.4]庚-5-烯-6-羧酸酯
甲基4,5-二氢-5-乙基-1H-吡唑-1-羧酸酯
甲基3-甲基-4,5-二氢-1,2-恶唑-4-羧酸酯
甲基(E)-3-[6-[1-羟基-1-(4-甲基苯基)-3-(1-吡咯烷基)丙基]-2-吡啶基]丙烯酰酸酯
甲基(5-氧代-4,5-二氢-1,2-恶唑-3-基)乙酸酯
环戊二烯并[d]咪唑-2,5(1H,3H)-二硫酮
环己羧酸,3-氨基-2-甲氧基-,甲基酯,(1S,2S,3S)-
溶剂黄93
溴化1-十六烷基-3-甲基咪唑
溴化1-十二烷基-2,3-二甲基咪唑
泰比培南酯中间体
泰比培南酯中间体
氨甲酸,[4,5-二氢-4-(碘甲基)-2-噻唑基]-,1,1-二甲基乙基酯(9CI)
氨基甲硫酸,[2-[[(2-羰基-1-咪唑烷基)硫代甲基]氨基]乙基]-,O-甲基酯
异噻唑,4,5-二氯-2,5-二氢-2-辛基-
希诺米啉
四氟硼酸二氢1,3-二(叔-丁基)-4,5--1H-咪唑正离子
四唑硝基紫
噻唑烷-2,4-二酮-2-缩氨基脲
噻唑丁炎酮
噻唑,4,5-二氢-4-(1-甲基乙基)-,(S)-
噁唑,4,5-二氢-4,4-二甲基-2-(5-甲基-2-呋喃基)-
噁唑,2-庚基-4,5-二氢-
咪唑烷基脲
吡嗪,2,3-二氢-5,6-二甲基-2-丙基-
叔-丁基3-羟基-1,4,6,7-四氢吡唑并[4,3-c]吡啶-5-羧酸酯
双吡唑啉酮