ventiloquinone L | 84018-45-1
中文名称
——
中文别名
——
英文名称
ventiloquinone L
英文别名
(1R,3S)-9-hydroxy-7-methoxy-1,3-dimethyl-3,4-dihydro-1H-benzo[g]isochromene-5,10-dione
CAS
84018-45-1;139067-50-8
化学式
C16H16O5
mdl
——
分子量
288.3
InChiKey
RNGGDQGPILKTQU-JGVFFNPUSA-N
BEILSTEIN
——
EINECS
——
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
计算性质
-
辛醇/水分配系数(LogP):2.2
-
重原子数:21
-
可旋转键数:1
-
环数:3.0
-
sp3杂化的碳原子比例:0.38
-
拓扑面积:72.8
-
氢给体数:1
-
氢受体数:5
上下游信息
-
上游原料
中文名称 英文名称 CAS号 化学式 分子量 —— ventiloquinone-L dimethyl ether 56678-12-7 C17H18O5 302.327
反应信息
-
作为产物:描述:(S)-tert-butyldimethyl(pent-4-yn-2-yloxy)silane 在 盐酸 、 四丁基氟化铵 、 三氯化硼 、 sodium hydride 、 [双(三氟乙酰氧基)碘]苯 作用下, 以 四氢呋喃 、 乙醚 、 二氯甲烷 、 水 、 乙腈 、 苯 为溶剂, 反应 29.75h, 生成 ventiloquinone L参考文献:名称:立体选择性合成(−)-1- Epi -ventiloquinone L和(+)-ventiloquinone L,这是基数的主要成分3 †摘要:立体选择性合成(-)-1- Epi -ventiloquinone L和(+)-ventiloquinone L(红衣主教3已经描述过了。该合成以7个步骤完成,分别具有(-)-1- Epi- ventiloquinone L和(+)-ventiloquinone L的总产率为10.5%和13%。关键步骤包括将卡宾5与炔6进行Dötz苯环环化反应,得到取代的萘部分,以及oxa-Pictet-Spengler反应以安装1,3-二甲基吡喃部分。DOI:10.1039/c2ob25453k
文献信息
-
Biomimetic studies towards the cardinalins: synthesis of (+)-ventiloquinone L and an unusual dimerisation作者:Jonathan Sperry、Jimmy J. P. Sejberg、Frank M. Stiemke、Margaret A. BrimbleDOI:10.1039/b905077a日期:——Studies towards the biomimetic synthesis of cardinalin 3 are described. Despite the successful enantioselective synthesis of the monomeric pyranonaphthoquinone ventiloquinone L, it subsequently failed to undergo a proposed biomimetic homodimerisation to cardinalin 3 using a range of oxidants. However, treatment of a related naphthopyran with cerium ammonium nitrate (CAN) facilitated a tandem biaryl
-
Synthesis of Pyran and Pyranone Natural Products作者:Christopher Donner、Melvyn Gill、Leonie TewierikDOI:10.3390/90600498日期:——An overview of the synthesis of the fungal metabolites (+)-dermolactone, (–)- semixanthomegnin, (+)- and (–)-mellein, (–)-ochratoxin α, (–)-(1R,3S)-thysanone, the enantiopure ventiloquinones L, E and G, and 8-desmethyleleutherin from a common chiral intermediate, is presented. Further methodology leading potentially toward extended quinones such as (3S,3'S)-xylindein is also outlined.综述了真菌代谢物 (+)-dermolactone, (-)- semixanthomegnin, (+)- and (-)-mellein, (-)-ochratoxin α, (-)-(1R,3S)-thysanone, 对映体纯 ventiloquinones L, E 和 G 以及 8-desmethyleleutherin 的合成。此外,还概述了进一步研究扩展醌(如 (3S,3'S)-xylindein)的方法。
-
Total synthesis of enantiopure 1,3-dimethylpyranonaphthoquinones including ventiloquinones E, G, L and eleutherin作者:Leonie M. Tewierik、Christian Dimitriadis、Christopher D. Donner、Melvyn Gill、Brendan WillemsDOI:10.1039/b607366b日期:——A new synthetic approach to enantiopure pyranonaphthoquinones is described. (S)-Mellein 10, prepared in 6 steps from (S)-propylene oxide 16, is converted stereospecifically to the (1R,3S)-dimethylpyran 15. The pyran 15 is then converted to the benzoquinone 14, which undergoes regiospecific Diels-Alder reactions with a variety of oxygenated butadienes to give pyranonaphthoquinones including ventiloquinones
表征谱图
-
氢谱1HNMR
-
质谱MS
-
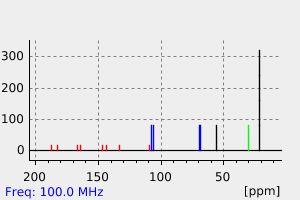
碳谱13CNMR
-
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息
同类化合物
黄麦格霉素
镰刀菌素甲醚
芦替菌素
脱氢胆碱
红葱醌
紫黄素
灰色菌素B
异红葱乙素
富仑菌素 B
乳醌霉素A
七尾霉素C
七尾霉素
O-乙基镰红菌素
N-(乙酰氧基)-N-((4-甲基苯基)甲氧基)苯酰胺
N-(4,5-二氢-1,3-噻唑-2-基)-2,4-二甲氧基苯酰胺
9-羟基-7-甲氧基-3-甲基-1H-苯并[g]异苯并吡喃-5,10-二酮
7,9-二羟基-3-甲基-1H-苯并[g]异苯并吡喃-5,10-二酮
3-羟基-3,4-二氢-1H-苯并[g]异苯并吡喃-5,10-二酮
3-溴噻吩
3,9-二羟基-7-甲氧基-3-甲基-1,4-二氢苯并[g]异苯并吡喃-5,10-二酮
3,7,9-三羟基-3-甲基-1,4-二氢苯并[g]异苯并吡喃-5,10-二酮
3,4-二氢-3-羟基-7,9-二甲氧基-3-甲基-1H-萘并[2,3-c]吡喃-5,10-二酮
2-甲基溴丁烷
2-[((1S,3R)-9-hydroxy-1-methyl-5,10-dioxo-3,4-dihydro-1H-benzo[g]isochromen-3-yl]acetate甲基]
1H-萘并[2,3-c]吡喃-6,9-二酮,3,4-二氢-8,10-二羟基-7-甲氧基-1,3-二甲基-,(1R,3S)-
1H-萘并[2,3-c]吡喃-6,9-二酮,3,4-二氢-5,10-二羟基-7-甲氧基-1,3-二甲基-,(1R,3S)-
1H-氮杂卓,2-[(4-乙氧苯基)甲基]六氢-
10-羟基-8-[(2R,4S,5R)-5-羟基-4-(羟基甲基)-1,3-二恶烷-2-基]-3-甲基-7-(2-氧代丙基)-1-丙基-1H-苯并[g]异苯并吡喃-6,9-二酮
1,5,10-三羟基-7-甲氧基-3-甲基-1H-苯并[g]异苯并吡喃-6,9-二酮
(5R,3aR,11bR)-4'alpha-乙酰氧基-3',3a,4',5',6',11b-六氢-3'alpha,7-二羟基-6'beta-甲基螺[5H-呋喃并[3,2-b]萘并[2,3-d]吡喃-5,2'-[2H]吡喃]-2,6,11(3H)-三酮
(3aR-(3aalpha,5alpha,11balpha))-3,3a,5,11b-四氢-8-羟基-7-甲氧基-5-甲基-2H-呋喃并(3,2-b)萘并(2,3-d)吡喃-2,6,11-三酮
(1RS,2SR,3SR,4SR)-1,2,3,4-tetrahydro-1,2,3,8-tetrahydroxy-4-methoxy-2-methyl-9,10-anthraquinone
dimethyl 1-(((1R,3R)-9-methoxy-1-methyl-5,10-dioxo-3,4,5,10-tetrahydro-1H-benzo[g]isochromen-3-yl)methyl)-1H-1,2,3-triazole-4,5-dicarboxylate
1-methoxy-3-(4-methylphenyl)-1H-benzo[g]isochromene-5,10-dione
3-isopropyl-1-methoxy-1H-benzo[g]isochromene-5,10-dione
Methyl (1-hydroxy-5,10-dioxo-3,4,5,10-tetrahydronaphtho[2,3-C]pyran-3-yl) ketone
1-methoxy-3-methyl-1H-benzo[g]isochromene-5,10-dione
3-aceto-5,10-dioxo-3,4,5,10-tetrahydro-1H-naphtho-[2,3-c]-pyran
(10-Hydroxy-8-methoxy-1-methyl-6,9-dioxo-3,4,6,9-tetrahydro-1H-benzo[g]isochromen-3-yl)-acetic acid methyl ester
4-(1,4-dioxo-1,4-dihydro-naphthalen-2-yl)-1,3-dihydroanthra[2,3-c]furan-5,10-dione
4-(1,4-Dioxonaphthalen-2-yl)-1,3-dihydrobenzo[f][2]benzofuran-5,8-dione
Desacetyl-β-naphthocyclinon
4-(3,6-Dioxocyclohexa-1,4-dien-1-yl)-1,3-dihydronaphtho[3,2-f][2]benzofuran-5,10-dione
3-(4-bromophenyl)-1-methoxy-1H-benzo[g]isochromene-5,10-dione
(8,10-dihydroxy-1-methyl-6,9-dioxo-3,4,6,9-tetrahydro-1H-benzo[g]isochromen-3-yl)-acetic acid methyl ester
4-(3,6-dioxa-cyclohexa-1,4-dienyl)-1,3-dihydro-naptho[2,3-c]furan-5,8-dione
(1S,3S)-3,4,5,10-tetrahydro-9-hydroxy-7-methoxy-1-methyl-5,10-dioxo-1H-naphtho[2,3-c]pyran-3-acetic acid
(1S,3S)-3,4,5,10-tetrahydro-9-hydroxy-3-(2-hydroxyethyl)-7-methoxy-1-methyl-5,10-dioxo-1H-naphtho[2,3-c]pyran