herbarumin I | 297174-24-4
中文名称
——
中文别名
——
英文名称
herbarumin I
英文别名
Izfxfvsoqmezkb-mnfmdyebsa-;(2R,3S,4S,5E)-3,4-dihydroxy-2-propyl-2,3,4,7,8,9-hexahydrooxecin-10-one
CAS
297174-24-4
化学式
C12H20O4
mdl
——
分子量
228.288
InChiKey
IZFXFVSOQMEZKB-MNFMDYEBSA-N
BEILSTEIN
——
EINECS
——
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
物化性质
-
沸点:399.0±42.0 °C(Predicted)
-
密度:1.106±0.06 g/cm3(Predicted)
计算性质
-
辛醇/水分配系数(LogP):1.1
-
重原子数:16
-
可旋转键数:2
-
环数:1.0
-
sp3杂化的碳原子比例:0.75
-
拓扑面积:66.8
-
氢给体数:2
-
氢受体数:4
上下游信息
-
上游原料
中文名称 英文名称 CAS号 化学式 分子量 —— (2R,3S,4S,5E)-4-hydroxy-3-phenylmethoxy-2-propyl-2,3,4,7,8,9-hexahydrooxecin-10-one 1237507-24-2 C19H26O4 318.413 —— (8R,9R)-8-hydroxy-7-oxo-9-propyl-5-nonen-9-olide 952410-03-6 C12H18O4 226.273 —— (E)-(3aR,4R,11aS)-2,2-Dimethyl-4-propyl-3a,4,7,8,9,11a-hexahydro-1,3,5-trioxa-cyclopentacyclodecen-6-one 343764-45-4 C15H24O4 268.353 —— (8S,9S,10R,E)-8,9-bis(benzyloxy)-10-propyl-3,4,5,8,9,10-hexahydro-2H-oxecin-2-one 1175535-33-7 C26H32O4 408.538 —— (R)-1-((4R,5S)-2,2-dimethyl-5-vinyl-1,3-dioxolan-4-yl)butyl hex-5-enoate 343764-44-3 C17H28O4 296.407 —— (2R,3R,4S,5E)-3,4-bis[[tert-butyl(dimethyl)silyl]oxy]-2-propyl-2,3,4,7,8,9-hexahydrooxecin-10-one 444987-70-6 C24H48O4Si2 456.814 -
下游产品
中文名称 英文名称 CAS号 化学式 分子量 —— (8R,9R)-8-hydroxy-7-oxo-9-propyl-5-nonen-9-olide 952410-03-6 C12H18O4 226.273
反应信息
-
作为反应物:描述:herbarumin I 在 manganese(IV) oxide 作用下, 以 二氯甲烷 为溶剂, 反应 12.0h, 以84%的产率得到(8R,9R)-8-hydroxy-7-oxo-9-propyl-5-nonen-9-olide参考文献:名称:含氨基羰基基团的Hoveyda-Grubbs型配合物用于合成草本素I和司康内酯A的催化活性研究摘要:已经研究了含有四个氨基羰基的“回旋镖”型闭环复分解催化剂对十元内酯的催化活性,并与 Grubbs I 和 II 以及 Hoveyda-Grubbs 催化剂进行了很好的比较。发现其活性优于上述三种闭环复分解催化剂,并提示了草本素 I 和 stagonolide A 的新型立体选择性全合成。DOI:10.1055/s-0029-1219807
-
作为产物:描述:2,3-O-异亚丙基-D-核糖酸 gamma-内酯 在 奎宁环 、 吡啶 、 盐酸 、 4-二甲氨基吡啶 、 copper(I) bromide dimethylsulfide complex 、 (Cy3P)2(Cl)2Ru=(3-Ph-inden-1-yliden) 、 二异丁基氢化铝 、 N,N'-二环己基碳二亚胺 作用下, 以 四氢呋喃 、 二氯甲烷 为溶剂, 生成 herbarumin I参考文献:名称:植物毒性内酯 Herbarumin I 和 II 的全合成以及 Pinolidoxin 拼图的基于合成的解决方案摘要:基于闭环复分解 (RCM) 作为形成中等大小环的关键步骤,描述了一种有效除草 10 元内酯家族的简明方法。这包括 Herbarumin I (1) 和 II (2) 的第一次全合成,以及 pinolidoxin 系列的几种可能的大环内酯的合成。将它们的光谱和分析数据与天然产物的光谱和分析数据进行比较,使我们能够建立 pinolidoxin 的立体结构,pinolidoxin 是一种诱导苯丙氨酸解氨酶 (PAL) 活性的强效抑制剂,如图 46 所示。然而,这一发现表明以前关于这种植物毒性剂的相对和绝对立体化学的研究是不正确的。从制备的角度来看,一个重要的方面是 RCM 反应的立体化学结果可以通过催化剂的选择来控制。因此,使用钌茚叉配合物16总是产生相应的(E)-烯烃,而带有N-杂环卡宾配体的第二代催化剂17提供具有良好选择性的异构(Z)-烯烃。该过程被认为反映了环化反应的动力学与热力学控制,DOI:10.1021/ja020238i
文献信息
-
Total synthesis of (+)-herbarumin I via intermolecular Nozaki–Hiyama–Kishi reaction作者:Adão Aparecido Sabino、Ronaldo A PilliDOI:10.1016/s0040-4039(02)00359-3日期:2002.4The phytotoxin herbarumin I, isolated from Phoma herbarum, was stereoselectively synthesized in 17 steps and 6% yield from l-arabinose featuring the intermolecular Nozaki–Hiyama–Kishi coupling and modified Yamaguchi macrolactonization as key steps.分离自植物标本的植物毒素植物标本I以17个步骤立体选择性地合成,并以分子间Nozaki–Hiyama–Kishi偶联和修饰的Yamaguchi大内酯化为关键步骤,以l-阿拉伯糖合成了6%的收率。
-
Stereoselective synthesis of the phytotoxic nonenolide herbarumin-I from l-ascorbic acid作者:K. Nagaiah、D. Sreenu、R. Srinivasa Rao、J.S. YadavDOI:10.1016/j.tetlet.2007.07.191日期:2007.10A stereoselective synthesis of herbarumin-I in 22% overall yield, starting from l-ascorbic acid derived (S)-2,3-O-isopropylidine glyceraldehyde as a chiral template is reported. Stereoselective allylation and vinylation to control the required stereogenic centres and macrolactonisation followed by a ring-closing metathesis (RCM) are the key steps.
-
Enantioselective total synthesis of the phytotoxic lactone herbarumin I作者:Alois Fürstner、Karin RadkowskiDOI:10.1039/b101148k日期:——A concise total synthesis of the potent herbicide herbarumin I (1) is presented based on an (E)-selective RCM reaction forging the 10-membered ring of this macrolide.一种简洁的全合成方法用于合成有效的除草剂herbarumin I (1),该方法基于选择性(E) RCM反应,构建了该大环化合物的10元环。
-
A Stereoselective Aldol Approach for the Total Synthesis of Herbarumin I and Stagonolide A作者:P. Srihari、G. Maheswara Rao、R. Srinivasa Rao、J. YadavDOI:10.1055/s-0029-1218775日期:2010.7A stereoselective total synthesis of phytotoxic compounds herbarumin I and stagonolide A has been achieved utilizing Crimmin’s protocol for non-Evans anti-aldol approach and a ring-closing olefin metathesis reaction as the key steps. macrolide - phytotoxic - Evans aldol - olefin metathesis利用Crimmin的非埃文斯抗羟醛方法和闭环烯烃复分解反应的关键步骤,已经完成了植物毒性化合物Herbarumin I和Stagonolide A的立体选择性全合成。 大环内酯类-植物毒性-埃文斯羟醛-烯烃复分解
-
Conformational Behavior and Absolute Stereostructure of Two Phytotoxic Nonenolides from the Fungus Phoma herbarum作者:José Fausto Rivero-Cruz、Genoveva Garcı́a-Aguirre、Carlos M. Cerda-Garcı́a-Rojas、Rachel MataDOI:10.1016/s0040-4020(00)00469-5日期:2000.7Bioactivity-directed fractionation of extracts from the fungus Phoma herbarum led to the isolation of two new phytotoxic nonenolides: (7S,8S,9R)-7,8-dihydroxy-9-propyl-5-nonen-9-olide (1) and (2R,7S,8S,9R)-2,7,8-trihydroxy-9-propyl-5-nonen-9-olide (2), which were named herbarumins I and II, respectively. The stereostructures were elucidated by spectroscopic methods and a combination of molecular modeling
表征谱图
-
氢谱1HNMR
-
质谱MS
-
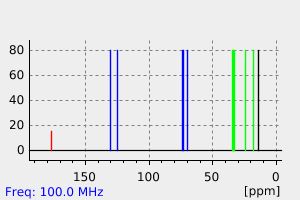
碳谱13CNMR
-
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息
同类化合物
胰岛素原(cattle),29-[N6-[[2-(甲磺酰)乙氧基]羰基]-L-赖氨酸]-59-[N6-[[2-(甲磺酰)乙氧基]羰基]-L-赖氨酸]-(9CI)
十氢-2,7-苯并二氧杂环癸烷-3,6-二酮
二环<3.3.0>-2-氧杂-5-(2-丙烯基)-1-辛烯
乙烯邻苯二甲酸酯
[(E,1R)-1-[(2R,4Z,7S,8R)-7-溴-8-乙基-3,6,7,8-四氢-2H-氧杂环辛三烯-2-基]己-3-烯-5-炔基]乙酸酯
[(2R,3S,4E,6R,7S)-6,7-二羟基-2-甲基-10-氧代-2,3,6,7,8,9-六氢氧杂环辛三烯-3-基] (E)-丁-2-烯酸酯
6,7-二氢-5aH-氧杂环丁烷并[3,2-d][1,3]苯并二氧戊环
5-氧杂-10-氮杂三环[5.3.1.03,8]十一碳-1(10),2,6,8-四烯
3-氧杂二环[3.3.1]壬-6-烯-9-酮
3,4,5,6-四氢-2,7-苯并二氧杂环癸烷e-1,8-二酮
17-苯基-18,19,20-三去甲-前列腺素F2-alpha1,15-内酯
10-(乙酰氧基)-4,5,6,7-四氢-2H-1-苯并氧杂环辛三烯-2,8(3H)-二酮
1-(2,3,4,5-四氢-1,6-苯并二噁辛英-8-基)丙烷-1-酮
1,2-环己烷二甲酸1-甲基-1,2-乙二基酯
(S)-5-烯丙基-2-氧杂双环[3.3.0]辛-8-烯
(R)-5-烯丙基-2-氧杂双环[3.3.0]辛-8-烯
(7Z)-2-(3-溴丙-1,2-二烯基)-5-(1-溴丙基)-3,3a,5,6,9,9a-六氢-2H-呋喃并[3,2-b]氧杂环辛三烯
(7E)-4,7-二羟基-10-甲基-3,4,5,6,9,10-六氢氧杂环辛三烯-2-酮
(6Z)-10-甲基-3,4,5,8,9,10-六氢-2H-氧杂环辛三烯-2-酮
(5Z,8S)-3-氯-2-[(E)-戊-2-烯-4-炔基]-8-[(E)-丙-1-烯基]-3,4,7,8-四氢-2H-氧杂环辛三烯
(4Z)-3,6-二氢-2,7-苯并二氧杂环癸烷e-1,8-二酮
(4S,5Z,7S,8S,10R)-4,7,8-三羟基-10-甲基-3,4,7,8,9,10-六氢氧杂环辛三烯-2-酮
(4R,5R,6Z,8S,10R)-4,5,8-三羟基-10-甲基-3,4,5,8,9,10-六氢氧杂环辛三烯-2-酮
(2R,5Z)-8a-[(R)-1-溴丙基]-3a-氯-3,4,7,8-四氢-2a-[(Z)-2-戊烯-4-炔基]-2H-氧杂环辛三烯
8-Chlor-1,6-benzodioxocin
2,2,6-Trifluoro-4-phenyl-3-trifluoromethyl-2H-pyran
2,3,4,5,6,7-Hexahydro-1-benzoxonin
aspinolide C
4-deutero-4,5-dihydro-2H-benzo[b]oxocin-6(3H)-one
3-Carbethoxy-4-bromo-5,6-dihydro-2-pyron
(E,8S,13S)-8,13-diisopropyl-5,8,9,12,13,16-hexahydro-6,15-dioxa-benzocyclotetradecene-7,14-dione
(1S,7Z,10R,11S)-11-t-butyldimethylsolyloxy-4-oxabicyclo[8.3.0]tridec-7-en-3-one
(Z)-2-Methyl-3a,4,5,6,7,9a-hexahydro-cycloocta[b]furan-3-carboxylic acid ethyl ester
(5R,8S,9R,10S,E)-5,8,9-trihydroxy-10-methyl-3,4,5,8,9,10-hexahydro-2H-oxecin-2-one
19,21-Dimethyl-4,15-dioxa-bicyclo[16.2.2]docosa-1(21),18(22),19-triene-3,16-dione
(1S,4aR,8aS)-1,4,4a,8a-Tetrahydro-naphthalen-1-ol
5-methyl-2-oxo-2H-cyclohepta[b]furan-3-carboxylic acid methyl ester
trans,trans-2,3;10,11-Dibenzo-1,4,9,12-tetraoxa-cyclohexadecatetraen-(2,6,10,14)
1-C-(4-O-acetyl-2,3,6-trideoxy-β-L-erytro-hex-2-en-pyranosyl)-3-bromopentane
2,2,2-Trichloro-acetimidic acid (2S,3S,6R)-2-methoxy-6-methyl-3,6-dihydro-2H-pyran-3-yl ester
1-C-(4-O-acetyl-2,3,6-trideoxy-α-L-erytro-hex-2-en-pyranosyl)-5-bromopentane
(3,4-dihydro-1H-2-benzopyran-7-yl)methanesulfonylchloride
methyl 2,3-C-(2-butene-1,4-diyl)-2,3-dideoxy-α,β-D-talofuranoside
3-oxobicyclo<7.3.1>-trideca-1(12),9(10)-diene-(ZZ)-12-carboxylic acid
(3aS,5S,6R,8aR)-6-Hydroxy-5-methyl-3,3a,4,5,6,8a-hexahydro-cyclohepta[b]furan-2-one
(Z)-3-butyl-6,7,8,9-tetrahydrooxonin-2(5H)-one
3,6-dihydro-4-methyl-2H-1-benzoxocine
18,20-Dimethyl-4,14-dioxa-bicyclo[15.2.2]henicosa-1(20),17(21),18-triene-3,15-dione
3-butyl-5,6,7,8,9,10-hexahydro-2H-oxecin-2-one