钛白粉 | 864179-42-0
物质功能分类
分子结构分类
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
物化性质
-
熔点:1840 °C
-
沸点:2900 °C
-
密度:4.26 g/mL at 25 °C(lit.)
-
闪点:368°C
-
物理描述:Titanium dioxide is an odorless white powder. Tasteless. pH 7.5. Occurs in three crystalline forms. (NTP, 1992)
-
颜色/状态:White, tetragonal crystals
-
气味:Odorless
-
味道:TASTELESS
-
溶解度:less than 1 mg/mL at 68° F (NTP, 1992)
-
蒸汽压力:0 mm Hg at 68 °F Essentially (NTP, 1992)
-
折光率:INDEX OF REFRACTION: 2.616; 2.903
计算性质
-
辛醇/水分配系数(LogP):-0.24
-
重原子数:3
-
可旋转键数:0
-
环数:0.0
-
sp3杂化的碳原子比例:0.0
-
拓扑面积:34.1
-
氢给体数:0
-
氢受体数:2
ADMET
安全信息
-
TSCA:Yes
制备方法与用途
对氧化钛最常见的担忧之一是它可能是一种致癌剂。癌症与该物质之间的联系最早可以追溯到1985年的一项研究,当时大鼠在两年内暴露于高浓度的氧化钛后,出现了肺癌的情况。然而,并非所有专家都相信这项研究的结果。国际癌症研究机构于2006年发表的研究表明,缺乏足够的证据证明氧化钛会导致癌症。尽管如此,该物质仍被归类为潜在的人类致癌物。
化学性质氧化钛是一种白色粉末,具有板钛型、锐钛型和金红石型三种晶型,其中工业上主要利用的是后两种类型。金红石型的相对密度约为4.26,熔点在1830~1850℃之间;而锐钛型的相对密度约为3.84。氧化钛化学性质相当稳定,不溶于水、有机酸和弱无机酸,但可溶于浓硫酸、碱液及氢氟酸中。其折射率分别为:金红石型为2.70,锐钛型为2.55。这种物质具有优异的颜料性能且无毒。
用途氧化钛在多种工业领域都有广泛应用:
- 在涂料工业中用作白色颜料和瓷器釉药。
- 用于造纸工业,可以提高纸张的可印性和不透明度,作为涂料和填料使用。
- 在冶炼工业中,可用于制备海绵钛、钛铁合金及硬质合金等。
- 还可以用作绝缘体、电焊条、搪瓷材料以及合成纤维、塑料、橡胶、印刷、染料等行业中的原料。此外,在化妆品工业中也可用作填充剂和食品添加剂。
将钛铁矿粉碎至一定细度,再与浓硫酸进行反应生成块状固相物。用水浸取后,得到含有硫酸氧钛、硫酸亚铁及大量杂质的钛液。通过沉降去除杂质,并冷冻分离除去硫酸亚铁。添加晶种促使硫酸氧钛水解生成偏钛酸(即水合二氧化钛),经漂洗,在800~1000℃下煅烧得到二氧化钛,直接作为产品使用或继续后处理。 反应方程式如下: [ \text{TiO}_2\cdot\text{FeO} + 2\text{H}_2\text{SO}_4 \rightarrow \text{TiOSO}_4 + \text{FeSO}_4 + 2\text{H}_2\text{O} ] [ \text{TiOSO}_4 + 2\text{H}_2\text{O} \rightarrow \text{TiO}_2\cdot\text{H}_2\text{O}\downarrow + \text{H}_2\text{SO}_4 ] [ \text{TiO}_2\cdot\text{H}_2\text{O} \rightarrow \text{TiO}_2 + \text{H}_2\text{O} ]
氯化法将金红石或高钛渣原料粉碎至一定粒度,与焦炭混合,在900℃的流化床中进行氯化反应生成四氯化钛。经过净化后,加入晶型转化剂,并在1300℃左右条件下进行氧化反应得到二氧化钛,再通过过滤、洗涤、干燥和粉碎得到成品。 反应方程式如下: [ 3\text{TiO}_2 + 4\text{C} + 6\text{Cl}_2 \rightarrow 3\text{TiCl}_4 + 2\text{CO} + 2\text{CO}_2 ] [ \text{TiCl}_4 + \text{O}_2 \rightarrow \text{TiO}_2 + 2\text{Cl}_2 ]
上下游信息
反应信息
-
作为反应物:描述:氧化钛(IV),金红石 以 gaseous matrix 为溶剂, 生成 钛白粉参考文献:名称:钛氧化物与水分子的反应。矩阵隔离FTIR和密度泛函研究摘要:通过基质隔离红外和密度泛函理论计算研究了二氧化钛与水分子的反应。在固态氩气中,二氧化钛分子与水反应,在退火时自发形成OTi(OH)2分子。计算了沿着TiO 2 + H 2 O→OTi(OH)2反应路径的势能面。尽管预计二氧化钛与水的络合物是稳定的,但由于低能垒和高水解反应放热性,未观察到该络合物。还提供了形成OTi-OH 2复合物的证据。DOI:10.1016/s0009-2614(01)00675-3
-
作为产物:描述:四氯化钛 生成 氧化钛(IV),金红石参考文献:名称:TOYAMA, SIGEHKI;NAKAMURA, MASAAKI, KEHMIKARU EHNDZINIYARINGU, 33,(1988) N, S. 130-135摘要:DOI:
-
作为试剂:描述:苯酐 在 盐酸 、 氧化钛(IV),金红石 、 硫酸 、 硝酸 、 一水合肼 、 tin(ll) chloride 、 sodium hydroxide 作用下, 以 水 为溶剂, 反应 4.25h, 生成 4-aminophthalic acid hydrazide参考文献:名称:一种高产率异鲁米诺发光试剂的制备方法摘要:本发明公开了一种高产率异鲁米诺发光试剂的制备方法,步骤(1)采用微波制备方法,反应时间为5min,微波法能够加快反应的速度,步骤(2)反应液一次抽滤结束后,取出倒入0.2kg冰水中,搅拌,抽滤,重复洗涤抽滤4次,多次抽洗能够提高产品的纯度,步骤(2)4‑硝基邻苯二甲酰亚胺产品最后用300mL分析纯即无水乙醇重结晶得到精产品,用该种乙醇作为提取剂能够提高产品的纯度,步骤(3)中使用的水合肼的纯度为85%,一般工业水合肼的纯度为40‑80%,本发明采用更高纯度的水合肼能够提高产品的产率,步骤(4)冷却温度为零下3℃,该温度下产品迅速析晶,这样能够保证产品的纯度以及产率。公开号:CN106083732A
文献信息
-
Preparation of methyl methacrylate by reaction of methyl propionate and申请人:BASF Aktiengesellschaft公开号:US04336403A1公开(公告)日:1982-06-22Methyl methacrylate is prepared by reacting methyl propionate and methanol at 200.degree.-550.degree. C. over a catalyst mixture which has a condensing action and is capable of dehydrogenating methanol to formaldehyde.
-
Process for the production of aryl carbonates申请人:Bayer AG公开号:US05527942A1公开(公告)日:1996-06-18Carbonates with aromatic ester groups can be produced by reaction of aromatic monohydroxy compounds with phosgene or with chloroformic acid esters of aromatic monohydroxy compounds, working at a temperature in the range of 50.degree. to 350.degree. C. in presence of oxides of the metals of Group IV B of the Mendeleeff periodic table as heterogeneous catalysts.
-
——作者:DOI:——日期:——
-
BUKEJXANOV N. R.; CYBOPOB B. V., TR. IN-TA XIM. HAYK AN KAZSSR, 1980, 51, 3-15作者:BUKEJXANOV N. R.、 CYBOPOB B. V.DOI:——日期:——
-
ARATA KAZUSHI; TANABE KOZO, BULL. CHEM. SOC. JAP., 1980, 53, NO 2, 299-303作者:ARATA KAZUSHI、 TANABE KOZODOI:——日期:——
表征谱图
-
氢谱1HNMR
-
质谱MS
-
碳谱13CNMR
-
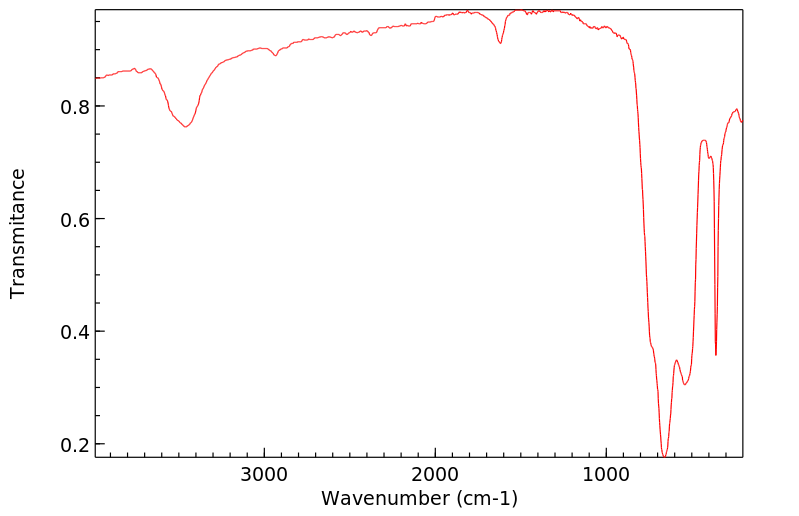
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息