氢氧化钠 | 1310-73-2
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
物化性质
-
熔点:681 °C(lit.)
-
沸点:1390°C
-
密度:1.515 g/mL at 20 °C
-
蒸气密度:<1 (vs air)
-
闪点:176-178°C
-
溶解度:H2O:1 Mat 20 °C,透明,无色
-
最大波长(λmax):λ: 260 nm Amax: 0.015λ: 280 nm Amax: 0.01
-
介电常数:57.5(25℃)
-
暴露限值:TLV-TWA air 2 mg/m3 (OSHA); ceiling 2 mg/m3 (ACGIH) and 2 mg/m3/15 min (NIOSH).
-
物理描述:Sodium hydroxide solution appears as a colorless liquid. More dense than water. Contact may severely irritate skin, eyes, and mucous membranes. Toxic by ingestion. Corrosive to metals and tissue.
-
颜色/状态:White, orthogonal crystals
-
气味:... Odorless ...
-
味道:Detection - the minimum physical intensity detection by a subject where he or she is not required to identify the stimulus but just detect the existence of the stimulus - in water: 8.00X10-3 mol/L.
-
蒸汽压力:1.82X10-21 mm Hg at 25 °C /extrapolated/
-
稳定性/保质期:
CONTAINERS OF LYE MUST BE TIGHTLY CLOSED TO PREVENT CONVERSION TO SODIUM CARBONATE BY CARBON DIOXIDE OF AIR.
-
自燃温度:Not flammable (USCG, 1999)
-
分解:When heated to decomposition it emits toxic fumes of /sodium oxide/.
-
粘度:4.0 cP at 350 °C
-
腐蚀性:Very corrosive (caustic) to ... aluminum metal in presence of moisture
-
燃烧热:SRP4: Non-combustible
-
汽化热:175 kJ/mol at 1388 °C
-
表面张力:At 18 °C: 74.35 dynes/cm (2.72 wt%), 75.85 dynes/cm (5.66 wt%), 83.05 dynes/cm (16.66 wt%), 96.05 dynes/cm (30.56 wt%), 101.05 dynes/cm (35.90 wt%)
-
聚合:SRP4: Not polymerized
-
折光率:Refractive index at 589.4 nm: 1.433 at 320 °C; 1.421 at 420 °C
-
解离常数:SRP4: Completely dissociated
-
pH:Strongly alkaline (1 % solution)
计算性质
-
辛醇/水分配系数(LogP):0.6
-
重原子数:1
-
可旋转键数:0
-
环数:0.0
-
sp3杂化的碳原子比例:1.0
-
拓扑面积:0
-
氢给体数:0
-
氢受体数:0
ADMET
安全信息
-
职业暴露限值:Ceiling: 2 mg/m3
-
TSCA:Yes
-
危险等级:8
-
立即威胁生命和健康浓度:10 mg/m3
-
危险品标志:C
-
安全说明:S24/25,S26,S36/37/39,S37/39,S45
-
危险类别码:R35
-
WGK Germany:1
-
海关编码:2815110000
-
危险品运输编号:UN 1824 8/PG 2
-
危险类别:8
-
RTECS号:TT2975000
-
包装等级:II
-
危险标志:GHS05
-
危险性描述:H290,H314
-
危险性防范说明:P260,P280,P303 + P361 + P353,P304 + P340 + P310,P305 + P351 + P338 + P310
SDS
制备方法与用途
纯的无水氢氧化钠为白色半透明,结晶状固体。有强烈的腐蚀性,有吸水性,可用作干燥剂,但是,不能干燥二氧化硫、二氧化碳和氯化氢气体。且在空气中易潮解,氢氧化钠极易溶于水,溶解度随温度的升高而增大,溶解时能放出大量的热,288K时其饱和溶液浓度可达16.4mol/L(1:1)。它的水溶液有涩味和滑腻感,溶液呈强碱性,具备碱的一切通性。市售烧碱有固态和液态两种:纯固体烧碱呈白色,有块状、片状、棒状、粒状,质脆;纯液体烧碱为无色透明液体。氢氧化钠还易溶于乙醇、甘油;但不溶于乙醚、丙酮、液氨。对纤维、皮肤、玻璃、陶瓷等有腐蚀作用,溶解或浓溶液稀释时会放出热量;与无机酸发生中和反应也能产生大量热,生成相应的盐类;与金属铝和锌、非金属硼和硅等反应放出氢;与氯、溴、碘等卤素发生歧化反应。能从水溶液中沉淀金属离子成为氢氧化物;能使油脂发生皂化反应,生成相应的有机酸的钠盐和醇,这是去除织物上的油污的原理。

氢氧化钠的用途十分广泛,在化学实验中,除了用做试剂以外,由于它有很强的吸湿性,还可用做碱性干燥剂。烧碱在国民经济中有广泛应用,许多工业部门都需要烧碱。使用烧碱最多的部门是化学药品的制造,其次是造纸、炼铝、炼钨、人造丝、人造棉和肥皂制造业。另外,在生产染料、塑料、药剂及有机中间体,旧橡胶的再生,制金属钠、水的电解以及无机盐生产中,制取硼砂、铬盐、锰酸盐、磷酸盐等,也要使用大量的烧碱。工业用氢氧化钠应符合国家标准 GB 209-2006;工业用离子交换膜法氢氧化钠应符合国家标准 GB/T 11199-89;化纤用氢氧化钠应符合国家标准 GB 11212-89;食用氢氧化钠应符合国家标准 GB 5175-85。
在工业上,氢氧化钠通常称为烧碱,或叫火碱、苛性钠。这是因为较浓的氢氧化钠溶液溅到皮肤上,会腐蚀表皮,造成烧伤。它对蛋白质有溶解作用,有强烈刺激性和腐蚀性(由于其对蛋白质有溶解作用,与酸烧伤相比,碱烧伤更不容易愈合)。用0.02%溶液滴入兔眼,可引起角膜上皮损伤。小鼠腹腔内LD50: 40 mg/kg,兔经口LDLo: 500 mg/kg。粉尘刺激眼和呼吸道,腐蚀鼻中隔;溅到皮肤上,尤其是溅到粘膜,可产生软痂,并能渗入深层组织,灼伤后留有瘢痕;溅入眼内,不仅损伤角膜,而且可使眼睛深部组织损伤,严重者可致失明;误服可造成消化道灼伤,绞痛、粘膜糜烂、呕吐血性胃内容物、血性腹泻,有时发生声哑、吞咽困难、休克、消化道穿孔,后期可发生胃肠道狭窄。由于强碱性,对水体可造成污染,对植物和水生生物应予以注意。
氢氧化钠溶解度曲线数据
温度 0 10 20 30 40 50 60 70 80 90 100
溶解度g 42 51 109 119 129 145 174 299 314 329 347
来源:《兰氏化学手册》
氢氧化钠在乙醇中的溶解度?
很小,如果是95%乙醇还可以溶解一小部分,无水乙醇基本不溶。不同温度(℃)时每100毫升水中的溶解克数:
98g/10℃;109g/20℃;119g/30℃;129g/40℃;174g/60℃正常情况:2NaOH+CO2=Na2CO3+H2O
二氧化碳反过量时:Na2CO3+CO2+H2O=2NaHCO31,在烧瓶中加入a克水(或a毫升),在另一烧瓶中称取无水硫酸铜b克(要足量)
2,将一定质量的NaOH固体溶解在这a克水中
3,在得到的溶液中通入适量(不能过量,以免生成碳酸氢钠)经过干燥的二氧化碳
4,得到的生成物拿去加热蒸发水分(烧瓶口加单孔塞)
5,蒸发出来的水气通入原来称取的b克无水硫酸铜中,直到原有的溶液蒸干为止
6,称取吸水变兰的硫酸铜重量,设为c克
如果c-b>a说明反应过程中生成了水。1,过滤海水
2,加入过量氢氧化钠,去除钙、镁离子,过滤Ca+2OH=Ca(OH)2(微溶)Mg+2OH=Mg(OH)2↓
3,加入过量氯化钡,去除硫酸根离子,过滤Ba+SO4(2-)=BaSO4↓
4,加入过量碳酸钠,去除钙离子、过量钡离子,过滤Ca+CO3=CaCO3↓Ba+CO3=BaCO3↓
5,加入适量盐酸,去除过量碳酸根离子2H+CO3=CO2↑+H2O
6,加热驱除二氧化碳
7,送入离子交换塔,进一步去除钙、镁离子
8,电解2NaCl+2H2O=(通电)H2↑+Cl2↑+2NaOH氢氧化钠(NaOH),是做冷制手工皂的最主要的原料之一,氢氧化钠是有等级之分的。大致可以分为:“工业级”和“试剂级”(化学纯、分析纯)。
“工业级”与“试剂级”的最大差别在于氢氧化钠的纯度,“试剂级”的氢氧化钠纯度会比“工业级”纯度更高,一般“工业级”纯度多在98%或者更低,“试剂级”则可以达到99%以上;试剂级因为含较少的其他物质如铁、镁、氯、铝、钾、氮、砷、硫酸、碳酸钠等,这样使用上比较不会影响化学反应后的结果,而工业级则含较多以上的物质。
在溶解氢氧化钠时,“试剂级”也比较不会有呛鼻的味道;此外,纯度越高,相对的价钱也会更贵。
大的原则是,哪个等级都是可以的,不计较这点成本,就选用高纯度的“试剂级”,化学纯、分析纯的都可以,如果要降低成本就选用纯度较低的“工业级”,计算时折算出不纯的部份。
通常实验室使用试剂级的化学试剂,纯度高的有化学纯、分析纯,分析纯纯度很高。根据不同的实验要求选择不同化学试剂等级,当然等级越高价格也越高。
工业级是供应工业上使用。但工业级不一定就不好,像NaOH这种大宗在使用的原料,一般纯度都很高,可达99%以上。剩下不到1%的不纯物大部分是食盐。其余的微量元素对皂的影响是微乎其微。
工业级当然不适合做微量的仪器分析使用,微量的不纯物就可能导致分析上的失误,但合成皂皂是不成问题的。
重要的是,必须要确认NaOH的纯度以利正确的计量,很多是分装的,一定要清楚其含量,就不至产生因NaOH过量使刺激性增加或NaOH量不足使皂化不足成品易酸败的问题.比较起来,油品的选择就更显重要了。因为作皂时,很多人习惯于添加一些其它物质,其纯度更差,所以可以不需计较这1~2%的NaOH的不纯物。用工业级的NaOH便宜,而且使用起来并没有问题,所以做皂使用此等级的NaOH就可以了。试样的水溶液能离解出OH-,呈强碱性反应。
4%试样液的钠试验(IT-28)应呈阳性。试样液的制备 用已知质量的称量瓶,迅速称取固体试样38g士1g或液体试样50g,称准至0.01g,放入100ml烧杯中,用水溶解后移入1000ml容量瓶中,加水稀释至接近刻度,冷却至室温后定容并摇匀。
测定步骤 取试样液50m1,注入250ml具塞三角瓶中,加入10%氯化钡溶液(V/V,使用前以酚酞为指示剂,用氢氧化钠溶液调至微红色)10ml,再加酚酞试液(TS-167)2~3滴,在磁力搅拌下,用1mol/L盐酸标准溶液密闭滴定至溶液呈微红色终点。式中 c——盐酸标准溶液浓度,mol/L
m——试样量,g;
V——盐酸标准溶液的耗用量,m1;
0.040——每毫摩尔氢氧化钠量,g。LD orally in rabbits: 500 mg/kg (10% soln) (Fazekas)GB 2760—96:加工助剂,GMP。
FAO/WHO(1984):人造奶油(按GMP);奶油及乳清奶油,最高用量2g/kg(以无水物计,仅用于调节Ph)。
氢氧化钠可用于造纸、纤维素浆粕的生产;用于肥皂、合成洗涤剂、合成脂肪酸的生产以及动植物油脂的精炼。纺织印染工业用作棉布退浆剂、煮炼剂和丝光剂。化学工业用于生产硼砂、氰化钠、甲酸、草酸、苯酚等。石油工业用于精炼石油制品,并用于油田钻井泥浆中。此外烧碱还用于生产氧化铝、金属锌和金属铜的表面处理以及玻璃、搪瓷、制革、医药、染料和农药方面。食品级产品在食品工业上用做酸中和剂,可作柑橘、桃子等的去皮剂,以及脱色剂、脱臭剂。
工业上生产烧碱的方法有苛化法和电解法两种。苛化法按原料不同分为纯碱苛化法和天然碱苛化法;电解法可分为隔膜电解法和离子交换膜法。
①纯碱苛化法将纯碱、石灰分别经化碱制成纯碱溶液、化灰制成石灰乳,于99~101℃进行苛化反应,苛化液经澄清、蒸发浓缩至40%以上,制得液体烧碱。将浓缩液进一步熬浓固化,制得固体烧碱成品。苛化泥用水洗涤,洗水用于化碱。其
Na2CO3+Ca(OH)2→2NaOH+CaCO3
②天然碱苛化法 天然碱经粉碎、溶解(或者碱卤)、澄清后加人石灰乳在95~100℃进行苛化,苛化液经澄清、蒸发浓缩至NaOH浓度46%左右、清液冷却、析盐后进一步熬浓.制得固体烧碱成品。苛化泥用水洗涤,洗水用于溶解天然碱。其
Na2CO3+Ca(OH)2→2NaOH+CaCO3↓
NaHCO3+Ca(OH)2→NaOH+CaCO3↓+H2O
③隔膜电船法将原盐化盐后加入纯碱、烧碱、氯化钡精制剂除去钙、镁、硫酸根离子等杂质,再于澄清槽中加入聚丙烯酸钠或苛化麸皮以加速沉淀,砂滤后加入盐酸中和,盐水经预热后送去电解,电解液经预热、蒸发、分盐、冷却,制得液体烧碱,进一步熬浓即得固体烧碱成品。盐泥洗水用于化盐。其
2NaCl+2H2O[电解] →2NaOH+Cl2↑+H2↑
④离子交换膜法将原盐化盐后按传统的办法进行盐水精制,把一次精盐水经微孔烧结碳素管式过滤器进行过滤后,再经螫合离子交换树脂塔进行二次精制,使盐水中钙、镁含量降到0.002%以下,将二次精制盐水电解,于阳极室生成氯气,阳极室盐水中的Na+通过离子膜进入阴极室与阴极室的0H生成氢氧化钠,H+直接在阴极上放电生成氢气。电解过程中向阳极室加入适量的高纯度盐酸以中和返迁的OH-,阴极室中应加入所需纯水。在阴极室生成的高纯烧碱浓度为30%~32%(质量),可以直接作为液碱产品,也可以进一步熬浓,制得周体烧碱成品。其
2NaCl+2H2O→2NaOH+H2↑+Cl2↑
反应信息
-
作为反应物:描述:参考文献:名称:[EN] SULFONAMIDE DERIVATIVES AS ANTIPSYCHOTIC AGENTS
[FR] DERIVES DE SULFONAMIDE UTILISES COMME AGENTS ANTIPSYCHOTIQUES摘要:该发明提供了以下结构的化合物(I),其中A和B分别代表基团-(CH2)m-和-(CH2)n-;R1代表C1-6烷基;R2代表氢、卤素、羟基、氰基、硝基、羟基C1-6烷基、三氟甲基、三氟甲氧基、C1-6烷基、C1-6烷氧基、-(CH2)pC3-6环烷基、-(CH2)pOC3-6环烷基、-COC1-6烷基、-SO2C1-6烷基、-SOC1-6烷基、-S-C1-6烷基、-CO2C1-6烷基、-CO2NR4R5、-SO2NR4R5、-(CH2)pNR4R5、-(CH2)pNR4COR5、一个可选择取代的芳基、一个可选择取代的杂芳基或一个可选择取代的杂环烷基;R3代表氢或C1-6烷基;Ar1代表一个可选择取代的杂芳基;Ar2代表一个可选择取代的苯基或一个可选择取代的杂芳基;Y代表一个键、-O-、-C1-6烷基-、-CR6R7X-、-XCR6R7-、-NR8CO-或-CONR8-;X代表氧、硫、-SO-或-SO2-;R4和R5分别独立地代表氢或C1-6烷基,或者与它们连接的氮或其他原子一起形成一个氮杂环烷基环或一个氧代取代的氮杂环烷基环;R6和R7分别独立地代表氢、C1-6烷基或氟;R8代表氢或C1-6烷基;m和n独立地代表从1和2中选择的整数;p独立地代表从0、1、2和3中选择的整数;或其药学上可接受的盐、溶剂或药学上可接受的衍生物。这些化合物在治疗中很有用,特别是作为抗精神病药物。公开号:WO2004031181A1 -
作为产物:参考文献:名称:Gas phase kinetics of the reactions of NaO with H2, D2, H2O, and D2O摘要:The gas phase reactions of the NaO radical with H2, D2, H2O, and D2O were studied in a flow tube reactor at room temperature. The reaction of NaO with H2 has two exothermic product channels, NaOH+H and Na+H2O. Both channels were observed and the Na formation channel produces some Na in the 32P state. The rate constants for the abstraction channel for H2 and D2 reactants are (2.6±1.0)×10−11 and (1.1×0.4)×10−11 cm3 molecule−1 s−1 at 296±2 K. The reaction of NaO with H2O was shown to be second order and the products are assumed to be NaOH and OH. The rate constants for H2O and D2O reactants are (2.2±0.4)×10−10 and (1.2±0.2)×10−10 cm3 molecule−1 s−1 at 298±1 K. The measured NaO+H2O rate constant is compared to the predicted collision rate constant from a model based on the large attractive dipole–dipole force between NaO and H2O. The role of these reactions in mesospheric Na chemistry is briefly discussed.DOI:10.1063/1.453726
-
作为试剂:描述:N-(4-氯-3-甲基-5-异恶唑基)-2-[(2-甲基-4,5-亚甲二氧基苯基)乙酰]噻吩-3-磺酰胺 在 盐酸羟胺 、 氢氧化钠 作用下, 以 水 、 甲醇 为溶剂, 反应 0.41h, 以70%的产率得到N-(4-chloro-3-methyl-5-isoxazolyl)-2-[3,4-(methylenedioxy)-6-methyl]phenylhydroxyimino-3-thiophenesulfonamide参考文献:名称:N-aryl thienyl-, furyl-, and pyrrolyl-sulfonamides and derivatives thereof that modulate the activity of endothelin摘要:提供了噻吩基、呋喃基和吡咯基磺酰胺以及用于调节或改变内皮素肽家族活性的方法。特别是,提供了N-(异恶唑基)噻吩磺酰胺、N-(异恶唑基)呋喃磺酰胺和N-(异恶唑基)吡咯磺酰胺以及使用这些磺酰胺通过将受体与磺酰胺接触来抑制内皮素肽与内皮素受体结合的方法。还提供了通过施用有效量的一个或多个这些磺酰胺或其前药来治疗内皮素介导的疾病的方法,这些磺酰胺或其前药抑制或增加内皮素的活性。公开号:US06342610B2
文献信息
-
Determination of the absolute third-order rate constant for the reaction between Na + OH + He by time-resolved molecular resonance-fluorescence spectroscopy, OH(A<sup>2</sup>∑<sup>+</sup>–X<sup>2</sup>Π), coupled with steady atomic fluorescence spectroscopy, Na(3<sup>2</sup>P<sub>J</sub>– 3<sup>2</sup>S<sub>1/2</sub>)作者:David Husain、John M. C. Plane、Chen Cong XiangDOI:10.1039/f29848001619日期:——signal averaging. Na(3 2S1/2) was monitored in the steady mode using atomic resonance fluorescence at λ= 589 nm [Na(3 2PJ)–Na(3 2S1/2)] coupled with phase-sensitive detection. The following absolute third-order rate constant (T= 653 K) was obtained: k1(Na + OH + He)=(1.07 ± 0.21)× 10–30 cm6 molecule–2 s–1. Quantitative extrapolation to high temperatures using the unimolecular reaction rate theory developed我们提出了Na + OH + He→NaOH + He反应的绝对三阶速率常数的第一个直接测量值。OH(X 2 Π)通过H的重复脉冲照射而产生的2通过的CaFø蒸气2个在他的存在下和过量从热管烤箱衍生原子钠的光学器件和一个缓慢的流动系统的,包括一部分,在动力学上等同于静态系统。基态OH通过时间分辨分子共振荧光在监测λ = 307纳米[OH(阿2 Σ + - X 2以下使用预触发光电倍增门控,光子计数光激发和,(0,0)Π)]信号平均。钠(32 š 1/2)中的溶液在使用原子共振荧光稳定模式在监测λ = 589nm处的[Na(3 2 P Ĵ)-Na(3 2 š 1/2)]加上相敏检测。得到以下绝对的三阶速率常数( T = 653 K): k 1(Na + OH + He)=(1.07±0.21)×10 –30 cm 6分子–2 s –1。使用Tröe开发的单分子反应速率理论对高温进行定量外推可得出结果k
表征谱图
-
氢谱1HNMR
-
质谱MS
-
碳谱13CNMR
-
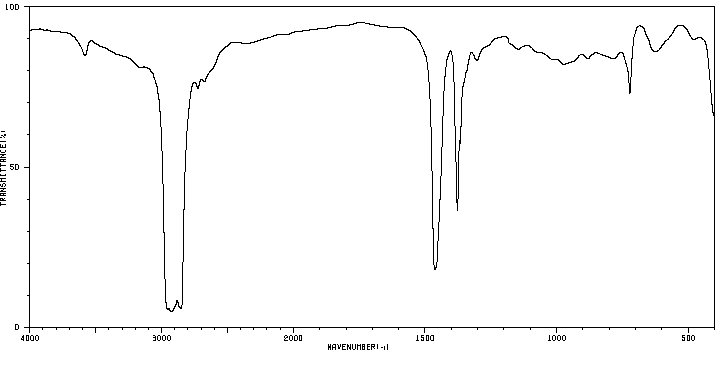
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息