3-甲基-2-恶唑烷酮 | 19836-78-3
中文名称
3-甲基-2-恶唑烷酮
中文别名
3-甲基-2-噁唑烷酮
英文名称
3-methyl-2-oxo-1,3-oxazolidine
英文别名
3-methyl-2-oxazolidinone;3-methyloxazolidin-2-one;N-methyl-2-oxazolidinone;3-methyl-2-oxazolidone;2-Oxazolidinone, 3-methyl-;3-methyl-1,3-oxazolidin-2-one
CAS
19836-78-3
化学式
C4H7NO2
mdl
——
分子量
101.105
InChiKey
VWIIJDNADIEEDB-UHFFFAOYSA-N
BEILSTEIN
——
EINECS
——
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
物化性质
-
熔点:15 °C(lit.)
-
沸点:87-90 °C1 mm Hg(lit.)
-
密度:1.17 g/mL at 25 °C(lit.)
-
闪点:>230 °F
-
介电常数:79.299999999999997
计算性质
-
辛醇/水分配系数(LogP):-0.1
-
重原子数:7
-
可旋转键数:0
-
环数:1.0
-
sp3杂化的碳原子比例:0.75
-
拓扑面积:29.5
-
氢给体数:0
-
氢受体数:2
安全信息
-
WGK Germany:3
-
RTECS号:RQ3550000
-
海关编码:2934999090
-
危险性防范说明:P233,P260,P261,P264,P271,P280,P302+P352,P304,P304+P340,P305+P351+P338,P312,P321,P332+P313,P337+P313,P340,P362,P403,P403+P233,P405,P501
-
危险性描述:H315,H319,H335
-
储存条件:存放于惰性气体中,避免与空气接触。
SDS
模块 1. 化学品
1.1 产品标识符
: 3-甲基-2-噁唑烷酮
产品名称
1.2 鉴别的其他方法
无数据资料
1.3 有关的确定了的物质或混合物的用途和建议不适合的用途
仅用于研发。不作为药品、家庭或其它用途。
模块 2. 危险性概述
2.1 GHS-分类
根据全球协调系统(GHS)的规定,不是危险物质或混合物。
2.3 其它危害物 - 无
模块 3. 成分/组成信息
3.1 物 质
: C4H7NO2
分子式
: 101.10 g/mol
分子量
无
模块 4. 急救措施
4.1 必要的急救措施描述
吸入
如果吸入,请将患者移到新鲜空气处。 如呼吸停止,进行人工呼吸。
皮肤接触
用肥皂和大量的水冲洗。
眼睛接触
用水冲洗眼睛作为预防措施。
食入
切勿给失去知觉者通过口喂任何东西。 用水漱口。
4.2 主要症状和影响,急性和迟发效应
据我们所知,此化学,物理和毒性性质尚未经完整的研究。
4.3 及时的医疗处理和所需的特殊处理的说明和指示
无数据资料
模块 5. 消防措施
5.1 灭火介质
灭火方法及灭火剂
用水雾,抗乙醇泡沫,干粉或二氧化碳灭火。
5.2 源于此物质或混合物的特别的危害
碳氧化物, 氮氧化物
5.3 给消防员的建议
如必要的话,戴自给式呼吸器去救火。
5.4 进一步信息
无数据资料
模块 6. 泄露应急处理
6.1 作业人员防护措施、防护装备和应急处置程序
避免吸入蒸气、烟雾或气体。
6.2 环境保护措施
不要让产品进入下水道。
6.3 泄漏化学品的收容、清除方法及所使用的处置材料
放入合适的封闭的容器中待处理。
6.4 参考其他部分
丢弃处理请参阅第13节。
模块 7. 操作处置与储存
7.1 安全操作的注意事项
一般性的防火保护措施。
7.2 安全储存的条件,包括任何不兼容性
贮存在阴凉处。 使容器保持密闭,储存在干燥通风处。
打开了的容器必须仔细重新封口并保持竖放位置以防止泄漏。
7.3 特定用途
无数据资料
模块 8. 接触控制和个体防护
8.1 容许浓度
最高容许浓度
没有已知的国家规定的暴露极限。
8.2 暴露控制
适当的技术控制
常规的工业卫生操作。
个体防护设备
眼/面保护
请使用经官方标准如NIOSH (美国) 或 EN 166(欧盟) 检测与批准的设备防护眼部。
皮肤保护
戴手套取 手套在使用前必须受检查。
请使用合适的方法脱除手套(不要接触手套外部表面),避免任何皮肤部位接触此产品.
使用后请将被污染过的手套根据相关法律法规和有效的实验室规章程序谨慎处理. 请清洗并吹干双手
所选择的保护手套必须符合EU的89/686/EEC规定和从它衍生出来的EN 376标准。
身体保护
防渗透的衣服, 防护设备的类型必须根据特定工作场所中的危险物的浓度和数量来选择。
呼吸系统防护
不需要对呼吸系统保护.对少量挥发请采用美国OV/AG (US)标准类型的 或欧洲ABEK (EU EN
14387)标准类型的呼吸器过滤器.
呼吸器使用经过测试并通过政府标准如NIOSH(US)或CEN(EU)的呼吸器和零件。
模块 9. 理化特性
9.1 基本的理化特性的信息
a) 外观与性状
形状: 液体
颜色: 淡黄
b) 气味
无数据资料
c) 气味阈值
无数据资料
d) pH值
无数据资料
e) 熔点/凝固点
熔点/凝固点: 15 °C - lit.
f) 沸点、初沸点和沸程
87 - 90 °C 在 1 hPa - lit.
g) 闪点
113 °C - 闭杯
h) 蒸发速率
无数据资料
i) 易燃性(固体,气体)
无数据资料
j) 高的/低的燃烧性或爆炸性限度 无数据资料
k) 蒸气压
无数据资料
l) 蒸汽密度
无数据资料
m) 密度/相对密度
1.17 g/mL 在 25 °C
n) 水溶性
无数据资料
o) n-辛醇/水分配系数
无数据资料
p) 自燃温度
无数据资料
q) 分解温度
无数据资料
r) 粘度
无数据资料
模块 10. 稳定性和反应活性
10.1 反应性
无数据资料
10.2 稳定性
无数据资料
10.3 危险反应
无数据资料
10.4 应避免的条件
无数据资料
10.5 不相容的物质
强氧化剂
10.6 危险的分解产物
其它分解产物 - 无数据资料
模块 11. 毒理学资料
11.1 毒理学影响的信息
急性毒性
半数致死剂量 (LD50) 经口 - 大鼠 - 8,342 mg/kg
半数致死剂量 (LD50) 经皮 - 兔子 - 12,636 mg/kg
皮肤刺激或腐蚀
无数据资料
眼睛刺激或腐蚀
无数据资料
呼吸道或皮肤过敏
无数据资料
生殖细胞致突变性
无数据资料
致癌性
IARC:
此产品中没有大于或等于 0。1%含量的组分被 IARC鉴别为可能的或肯定的人类致癌物。
生殖毒性
无数据资料
特异性靶器官系统毒性(一次接触)
无数据资料
特异性靶器官系统毒性(反复接触)
无数据资料
吸入危险
无数据资料
潜在的健康影响
吸入 吸入可能有害。 可能引起呼吸道刺激。
摄入 如服入是有害的。
皮肤 通过皮肤吸收可能有害。 可能引起皮肤刺激。
眼睛 可能引起眼睛刺激。
接触后的征兆和症状
据我们所知,此化学,物理和毒性性质尚未经完整的研究。
附加说明
化学物质毒性作用登记: RQ3550000
模块 12. 生态学资料
12.1 生态毒性
无数据资料
12.2 持久性和降解性
无数据资料
12.3 潜在的生物累积性
无数据资料
12.4 土壤中的迁移性
无数据资料
12.5 PBT 和 vPvB的结果评价
无数据资料
12.6 其它不良影响
无数据资料
模块 13. 废弃处置
13.1 废物处理方法
产品
将剩余的和不可回收的溶液交给有许可证的公司处理。
受污染的容器和包装
按未用产品处置。
模块 14. 运输信息
14.1 联合国危险货物编号
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.2 联合国运输名称
欧洲陆运危规: 非危险货物
国际海运危规: 非危险货物
国际空运危规: 非危险货物
14.3 运输危险类别
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.4 包裹组
欧洲陆运危规: - 国际海运危规: - 国际空运危规: -
14.5 环境危险
欧洲陆运危规: 否 国际海运危规 国际空运危规: 否
海洋污染物(是/否): 否
14.6 对使用者的特别提醒
无数据资料
模块 15 - 法规信息
N/A
模块16 - 其他信息
N/A
上下游信息
-
上游原料
中文名称 英文名称 CAS号 化学式 分子量 2-唑烷酮 dimethylenecyclourethane 497-25-6 C3H5NO2 87.0782 2-(N-Boc-N-甲基氨基)乙醇 methyl(2-hydroxyethyl)carbamic acid tert-butyl ester 57561-39-4 C8H17NO3 175.228 -
下游产品
中文名称 英文名称 CAS号 化学式 分子量 —— 3-methyl-2,4-oxazolidinedione 14422-90-3 C4H5NO3 115.089 3-甲基-1,3-噁唑啉 3-methyl-1,3-oxazolidine 27970-32-7 C4H9NO 87.1216
反应信息
-
作为反应物:描述:3-甲基-2-恶唑烷酮 在 (tBuPNN)Ru(CO)HCl 、 potassium tert-butylate 、 氢气 作用下, 以 四氢呋喃 为溶剂, 135.0 ℃ 、6.0 MPa 条件下, 反应 19.0h, 以100%的产率得到N-甲基-2-羟基乙胺参考文献:名称:Combining Low-Pressure CO2 Capture and Hydrogenation To Form Methanol摘要:This paper describes a novel approach to CO2 hydrogenation, in which CO2, capture with aminoethanols at low pressure is coupled with hydrogenation of the captured product, oxazolidinone, directly to MeOH. In particular, (2-methylamino)ethanol or valinol captures CO, at 1-3 bar in the presence of catalytic Cs2CO3 to give the corresponding oxazolidinones in up to 65-70 and 90-95% yields, respectively. Efficient hydrogenation of oxazolidinones was achieved using PNN pincer Ru catalysts to give the corresponding aminoethanol (up to 95-100% yield) and MeOH (up to 78-92% yield). We also have shown that both CO2 capture and oxazolidinone hydrogenation can be performed in the same reaction mixture using a simple protocol that avoids intermediate isolation or purification steps. For example, CO2, can be captured by valinol at 1 bar with Cs2CO3 catalyst followed by 4-isopropyl-2-oxazolidinone hydrogenation in the presence of a bipy-based pincer Ru catalyst to produce MeOH in 50% yield after two steps.DOI:10.1021/acscatal.5b00194
-
作为产物:描述:参考文献:名称:N-Carbamylamino Alcohols as the Precursors of Oxazolidinones via Nitrosation-Deamination Reaction摘要:以 N-亚硝基化合物为中间体,通过亚硝酸处理从 N-氨基甲酰氨基醇有效地制备了噁唑烷酮。以 dl-苯丙氨酸为起点,利用 d-海因酶催化的 5-苄基海因在动态动力学解析条件下的对映选择性水解,随后利用带有 N-氨甲酰氨基官能团的中间体还原成上述环化反应的前体,开发出了一条制备 (R)-4-benzyloxazolidinone 的新途径。DOI:10.1055/s-2000-6508
-
作为试剂:描述:硫酸二乙酯 、 enolate potassique de l'acetylacetate d'ethyle 在 3-甲基-2-恶唑烷酮 作用下, 以 四氢呋喃 为溶剂, 反应 24.0h, 生成 3-乙氧基-顺式-巴豆酸乙酯 、 3-乙氧基-2-丁烯酸乙酯 、 2-乙基乙酰乙酸乙酯参考文献:名称:固体支持物:六甲基磷酸三酰胺,-吡咯烷酮等-烷基恶唑烷酮摘要:在带有-吡咯烷酮-NP)或-恶唑烷酮(-NO)部分的聚合物的存在下,乙酰乙酸乙酯的烯醇钾的Et 2 SO 4的乙基化速率提高。这取决于聚合物骨架的性质。烯醇醚的C / O烷基化以及E / Z比率说明了烯酸酯与聚合物内部相关阳离子的相互作用:效率为:-HMPA> -NP -NO,尽管有所不同在反应速率上观察到顺序:-HMPA>-NO> -NP。因此,该测试反应比亲核取代速率增强的研究提供了更多有关所涉及的不同相互作用的信息。DOI:10.1016/0040-4020(82)85033-3
文献信息
-
A new class of nitrosoureas. I. Synthesis and antitumor activity of 1-(2-chloroethyl)-3,3-disubstituted-1-nitrosoureas having a hydroxyl group at the .BETA.-position of the substituents.作者:KENJI TSUJIHARA、MASAKATSU OZEKI、TAMIO MORIKAWA、YOSHIHISA ARAIDOI:10.1248/cpb.29.2509日期:——1-(2-Chloroethyl)-3, 3-disubstituted-1-nitrosoureas (5a-m), a new class of nitrosoureas, were synthesized and tested for antitumor activities against leukemia L1210 and Ehrlich ascites carcinoma. The nitrosoureas (5e-k) having a hydroxyl group at the β-position of the substituents showed remarkable antitumor activities. In particular, 1-(2-chloroethyl)-3, 3-bis (2-hydroxyethyl)-1-nitrosourea (5k) had excellent activities and showed 5 and 16 times greater therapeutic ratios than 1-(2-chloroethyl)-3-cyclohexyl-1-nitrosourea against leukemia L1210 and Ehrlich ascites carcinoma, respectively. These nitrosoureas (5e-k) appear to be activated nonenzymatically by attack of the hydroxyl group on the carbonyl group to give the oxazolidinones (6) and chloroethyl diazohydroxide (7) without generation of the isocyanates (8).
-
Spiro-fused 2-alkoxy-2-amino-Δ<sup>3</sup>-1,3,4-oxadiazolines. Synthesis and thermolysis to corresponding aminooxycarbenes作者:Philippe Couture、John WarkentinDOI:10.1139/v97-153日期:1997.9.1undergo thermolysis in benzene at 90 °C with first-order rate constants of (1.6–50) × 10−5 s−1. The dependence of these rate constants on the nature of the substituents present on the oxadiazoline ring is consistent with a mechanism involving a carbonyl ylide intermediate. Substituents on N of the oxazolidine or tetrahydro-1,3-oxazine moieties play a major role in determining the fragmentation pathways
-
Magnesium-Catalyzed Mild Reduction of Tertiary and Secondary Amides to Amines作者:Nicole L. Lampland、Megan Hovey、Debabrata Mukherjee、Aaron D. SadowDOI:10.1021/acscatal.5b01038日期:2015.7.2information on catalyst activation in hand, tertiary amides are selectively reduced to amines in good yield when catalytic amounts of ToMMgMe are added to a mixture of amide and excess HBpin. In addition, secondary amides are reduced in the presence of 10 mol % ToMMgMe and 4 equiv of HBpin. Functional groups such as cyano, nitro, and azo remain intact under the mild reaction conditions. In addition, kinetic experiments报道了酰胺催化加氢硼化以将其脱氧为胺的第一个实例。该转化采用了富含地球的镁基催化剂。叔酰胺和仲酰胺在频哪醇硼烷(HBpin)和催化量的To M MgMe(To M =三(4,4-二甲基-2-恶唑啉基)苯基硼酸酯)存在下于室温还原为胺。如催化实验中底物和HBpin的浓度和添加顺序的影响所揭示的,在该系统中催化剂的引发和形成是复杂的。由To M MgMe和HBpin形成的To M MgH 2 Bpin被排除为可能的催化相关物种,因为它与N发生了反应,N-二甲基苯甲酰胺,分别通过C–N和C–C键裂解途径提供Me 2 NBpin和PhBpin。在该反应中,仅以低收率形成催化产物苄基二甲基胺。或者,To M MgMe与N,N-二甲基苯甲酰胺的反应在24小时内缓慢分解为To M MgMe,并且该相互作用也被排除为催化相关步骤。总之,这些数据表明,To M MgMe的催化活化需要HBpin和酰胺,以及To
-
Design, synthesis and antimalarial evaluation of novel thiazole derivatives作者:José María Bueno、Miguel Carda、Benigno Crespo、Ana Carmen Cuñat、Cristina de Cozar、María Luisa León、J. Alberto Marco、Nuria Roda、Juan F. Sanz-CerveraDOI:10.1016/j.bmcl.2016.07.010日期:2016.8ongoing search for compounds with antimalarial activity, we prepared a series of thiazole analogs and conducted a SAR study analyzing their in vitro activities against the chloroquine-sensitive Plasmodium falciparum 3D7 strain. The results indicate that modifications of the N-aryl amide group linked to the thiazole ring are the most significant in terms of in vitro antimalarial activity, leading to compounds
-
Synthesis and kinetics of disassembly for silyl-containing ethoxycarbonyls using fluoride ions作者:Eugene Camerino、Grant C. Daniels、James H. Wynne、Erick B. IezziDOI:10.1039/c7ra07876e日期:——series of silyl-containing ethoxycarbonates and ethoxycarbamates on electron poor anilines and phenols were synthesized and their kinetics of disassembly determined in real-time upon exposure to fluoride ion sources at room temperature. The results provide a greater understanding of stability and kinetics for silyl-containing protecting groups that eliminate volatile molecules upon removal, which will
表征谱图
-
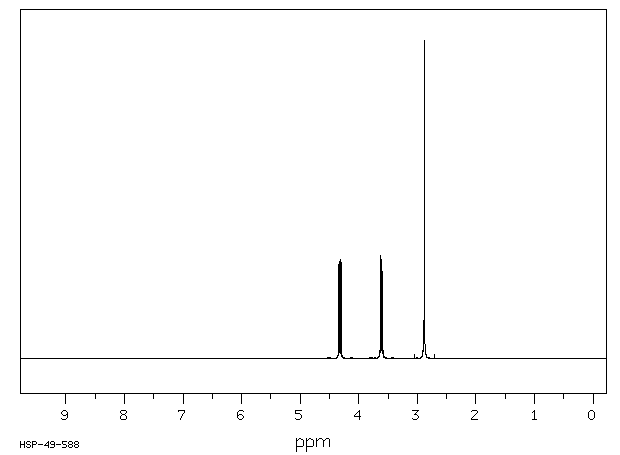
氢谱1HNMR
-
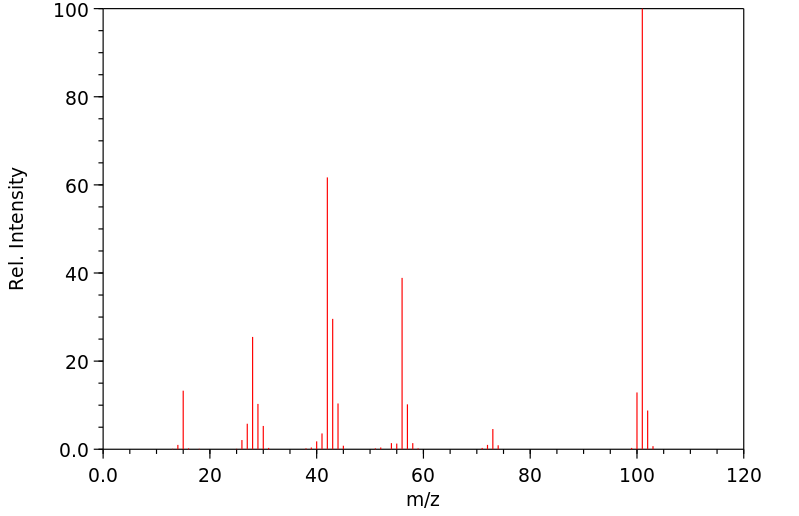
质谱MS
-
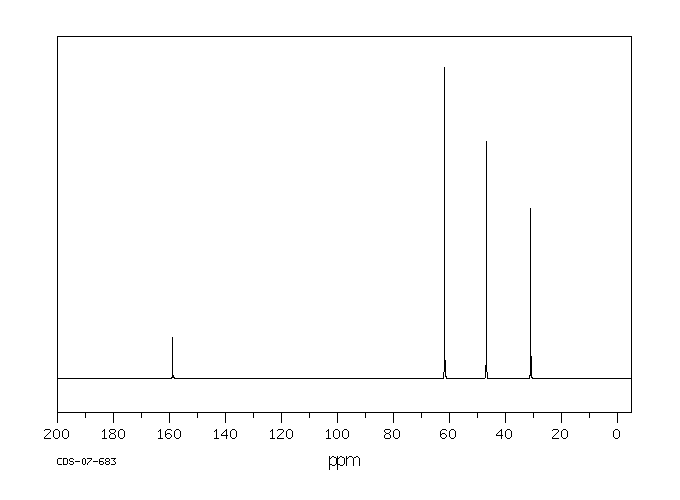
碳谱13CNMR
-
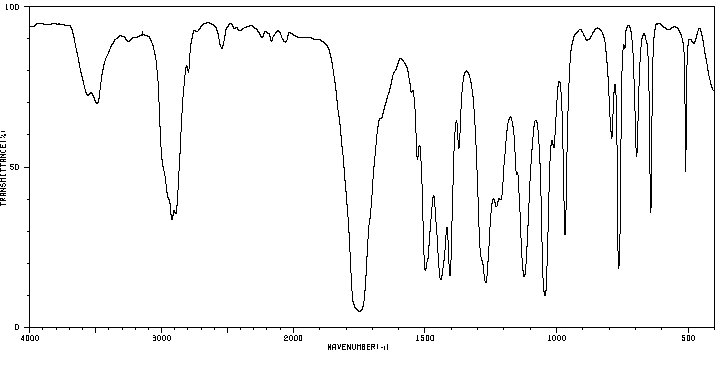
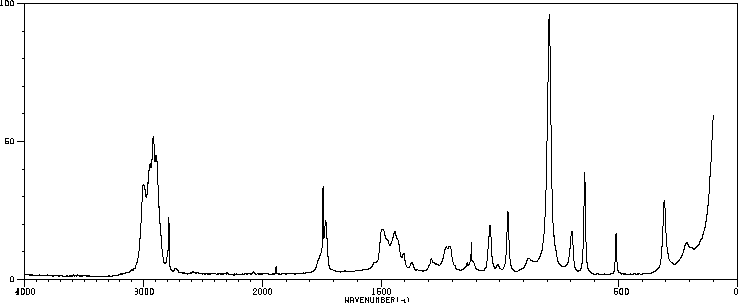
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息
同类化合物
(R)-4-异丙基-2-恶唑烷硫酮
麻黄恶碱
顺-八氢-2H-苯并咪唑-2-酮
顺-1-(4-氟苯基)-4-[1-(4-氟苯基)-4-羰基-1,3,8-三氮杂螺[4.5]癸-8-基]环己甲腈
非达司他
降冰片烯缩醛3-((1S,2S,4S)-双环[2.2.1]庚-5-烯-2-羰基)恶唑烷-2-酮
阿齐利特
阿那昔酮
阿洛双酮
阿帕鲁胺
阿帕他胺杂质2
铟烷-2-YL-甲基胺盐酸
钾3-{2-[3-氰基-3-(十二烷基磺酰基)-2-丙烯-1-亚基]-1,3-噻唑烷-3-基}-1-丙烷磺酸酯
钠2-{[4,5-二羟基-3-(羟基甲基)-2-氧代-1-咪唑烷基]甲氧基}乙烷磺酸酯
重氮烷基脲
詹氏催化剂
解草恶唑
解草噁唑
表告依春
螺莫司汀
螺立林
螺海因氮丙啶
螺[咪唑烷-4,3'-吲哚啉]-2,2',5-三酮
螺[1-氮杂双环[2.2.2]辛烷-8,5'-咪唑烷]-2',4'-二酮
苯甲酸,4-氟-,2-[5,7-二(三氟甲基)-1,8-二氮杂萘-2-基]-2-甲基酰肼
苯氰二硫酸,1-氰基-1-甲基-4-氧代-4-(2-硫代-3-噻唑烷基)丁酯
苯妥英钠杂质8
苯妥英钠
苯妥英-D10
苯妥英
苯基硫代海因半胱氨酸钠盐
苯基硫代乙内酰脲-谷氨酸
苯基硫代乙内酰脲-蛋氨酸
苯基硫代乙内酰脲-苯丙氨酸
苯基硫代乙内酰脲-色氨酸
苯基硫代乙内酰脲-脯氨酸
苯基硫代乙内酰脲-缬氨酸
苯基硫代乙内酰脲-异亮氨酸
苯基硫代乙内酰脲-天冬氨酸
苯基硫代乙内酰脲-亮氨酸
苯基硫代乙内酰脲-丙氨酸
苯基硫代乙内酰脲-D-苏氨酸
苯基硫代乙内酰脲-(NΕ-苯基硫代氨基甲酰)-赖氨酸
苯基乙内酰脲-甘氨酸
苏氨酸-1-(苯基硫基)-2,4-咪唑烷二酮(1:1)
色氨酸标准品002
膦酸,(2-羰基-1-咪唑烷基)-,二(1-甲基乙基)酯
脱氢-1,3-二甲基尿囊素
脱氢-1,3,8-三甲基尿囊素
聚(d(A-T)铯)