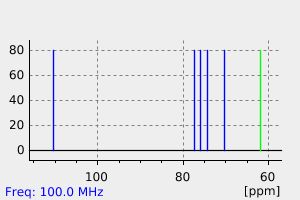
β-D-glucosyl fluoride
中文名称
——
中文别名
——
英文名称
β-D-glucosyl fluoride
英文别名
β-D-glucopyranosyl fluoride;b-D-Glucopyranosyl fluoride;(2S,3R,4S,5S,6R)-2-fluoro-6-(hydroxymethyl)oxane-3,4,5-triol
CAS
——
化学式
C6H11FO5
mdl
——
分子量
182.149
InChiKey
ATMYEINZLWEOQU-VFUOTHLCSA-N
BEILSTEIN
——
EINECS
——
-
物化性质
-
计算性质
-
ADMET
-
安全信息
-
SDS
-
制备方法与用途
-
上下游信息
-
文献信息
-
表征谱图
-
同类化合物
-
相关功能分类
-
相关结构分类
计算性质
-
辛醇/水分配系数(LogP):-1.6
-
重原子数:12
-
可旋转键数:1
-
环数:1.0
-
sp3杂化的碳原子比例:1.0
-
拓扑面积:90.2
-
氢给体数:4
-
氢受体数:6
上下游信息
-
上游原料
中文名称 英文名称 CAS号 化学式 分子量 氟代四乙酸 beta-d-吡喃葡萄糖酯 2,3,4,6-tetra-O-acetyl-β-D-glucopyranosyl fluoride 2823-46-3 C14H19FO9 350.298
反应信息
-
作为反应物:描述:参考文献:名称:单个葡糖苷酶水解α-和β-d-葡糖基氟化物:糖基化酶催化中分别控制“可塑性”和“保守”相的新证据摘要:摘要甜菜种子和未发芽大米中的α-葡萄糖苷酶催化β-d-吡喃葡萄糖基氟的水解形成α-d-葡萄糖。反应很慢,V / K = 11-15×10 -3或对-硝基苯基α-d-吡喃葡萄糖苷水解反应的V / K =的1-2%,但不是由于底物中的任何杂质或污染引起的β-葡糖苷酶或葡糖淀粉酶。此外,杏仁β-葡糖苷酶以极低的速率促进了α-d-葡糖基氟化物的水解以形成β-d-葡萄糖,V / K = 4×10 -4。这种弱反应不是由底物中的任何杂质引起的,也不是由α-葡糖苷酶或葡糖淀粉酶的污染引起的,而是部分(约20%)可归因于伴随的海藻糖酶的痕迹。所有三种葡糖苷酶均对α-和β-d-葡糖基氟化物都有作用,尽管不利的异构体效率低下,反映了先前证明的每种酶催化基团对不同类型底物进行灵活反应的能力。分别将不利的d-葡萄糖基氟化物转化为与烯醇或有利的d-葡萄糖基底物相同构型的产物,为葡萄糖苷酶化学机理的两步性质提供了进一DOI:10.1016/0008-6215(93)84153-w
-
作为产物:描述:参考文献:名称:以硫酰氟为脱氟试剂合成含氟碳水化合物摘要:碳水化合物的氟化一直是增加其酶促和化学稳定性并降低其亲水性的策略之一,使得这种修饰对于药物发现目的具有吸引力。单氟化碳水化合物的合成是在温和条件下通过使用SO 2 F 2作为脱氧氟化试剂在碱存在下没有额外的氟化物添加剂实现的。该方法具有低毒、易得、成本低、效率高、可适用于多种糖单元等特点。DOI:10.1021/acs.orglett.3c01305
文献信息
-
Rapid phenolic O-glycosylation of small molecules and complex unprotected peptides in aqueous solvent作者:Tyler J. Wadzinski、Angela Steinauer、Liana Hie、Guillaume Pelletier、Alanna Schepartz、Scott J. MillerDOI:10.1038/s41557-018-0041-8日期:2018.6Glycosylated natural products and synthetic glycopeptides represent a significant and growing source of biochemical probes and therapeutic agents. However, methods that enable the aqueous glycosylation of endogenous amino acid functionality in peptides without the use of protecting groups are scarce. Here, we report a transformation that facilitates the efficient aqueous O-glycosylation of phenolic糖基化的天然产物和合成的糖肽代表了生化探针和治疗剂的重要且不断增长的来源。然而,缺少能够在不使用保护基的情况下使肽中的内源氨基酸官能团进行水性糖基化的方法。在这里,我们报道了一种转化,该转化促进了在广泛的小分子,未保护的酪氨酸和嵌入一系列复杂,完全未保护的肽中的酪氨酸残基的酚官能团的有效O-糖基化水溶液。该转化使用糖基氟化物供体,并由Ca(OH)2促进,取决于糖基供体的立体化学,在室温下在水中迅速进行,并具有良好的收率和选择性形成独特的异头物产物。观察到高官能团耐受性,并且在几乎所有蛋白原性氨基酸的所有侧链均存在的情况下,Cys例外,酚糖基化选择性发生。该方法为水中的O-芳基糖苷和Tyr- O-糖基化肽的无保护基的合成提供了高度选择性,有效且操作简单的方法。
-
[EN] METHODS FOR GLYCOSYLATION<br/>[FR] PROCÉDÉS DE GLYCOSYLATION申请人:UNIV MICHIGAN REGENTS公开号:WO2020232194A1公开(公告)日:2020-11-19Provided herein are methods of glycosylation in the formation of disaccharides, trisaccharides, and oligosaccharides using fluoroglycosides, silyl ether glycosides and a triaryl borane catalyst.
-
Creation of an α-Mannosynthase from a Broad Glycosidase Scaffold作者:Keisuke Yamamoto、Benjamin G. DavisDOI:10.1002/anie.201201081日期:2012.7.23α‐Mannosides made easy: Mutation of a family‐GH31 α‐glucosidase that displays plasticity to alterations at the 2‐OH position of donor substrates created an efficient α‐mannoside‐synthesizing biocatalyst. A simple fluoride donor reagent was used for the synthesis of a range of mono‐α‐mannosylated conjugates using the α‐mannosynthase displaying low (unwanted) oligomerization activity.
-
Hydrolysis of β-d-glucopyranosyl fluoride to α-d-glucose catalyzed by Aspergillus niger α-d-glucosidase作者:Edward J. Hehre、Hirokazu Matsui、Curtis F. BrewerDOI:10.1016/0008-6215(90)84282-y日期:1990.4-glucosyl fluoride and not from a contaminating trace of α- d -glucosyl fluoride, and is catalyzed by the α- d -glucosidase and not by an accompanying trace of β- d -glucosidase or glucoamylase. Maltotriose competitively inhibits the hydrolysis, and β- d -glucosyl fluoride in turn competitively inhibits the hydrolysis of p-nitrophenyl α- d -glucopyranoside, indicating that β- d -glucosyl fluoride is bound摘要黑曲霉α-d-葡萄糖苷酶结晶且对β-d-葡萄糖苷没有可检测的活性,催化β-d-葡萄糖吡喃糖基氟的缓慢水解形成α-d-葡萄糖。β-d-葡萄糖基氟,对硝基苯基α-d-吡喃葡萄糖苷和α-d-吡喃葡萄糖基氟化物水解的最大初始速率V为0.27、0.75和78.5μmol.min-1.mg-1,分别具有0.0068、1.44和41.3的相应V / K常数。独立的证据表明,该反应源自β-d-葡萄糖基氟化物,而不是源自痕量的α-d-葡萄糖基氟化物,并且是由α-d-葡萄糖苷酶催化,而不是由伴随的β-痕量催化。 d-葡糖苷酶或葡糖淀粉酶。麦芽三糖竞争性地抑制水解,β-d-葡萄糖基氟又竞争性地抑制对硝基苯基α-d-葡萄糖吡喃糖苷的水解,表明β-d-葡萄糖基氟与已知的α-葡萄糖苷酶底物结合在同一位点。当前的发现提供了新的证据,即α-葡萄糖苷酶不限于α-d-葡萄糖基底物或提供保留构型的反应。他们强烈支持这样的概
-
Catalytic versatility of trehalase: Synthesis of α-d-glucopyranosyl α-d-xylopyranoside from β-d-glucosyl fluoride and α-d-xylose作者:Takafumi Kasumi、Curtis F. Brewer、Elwyn T. Reese、Edward J. HehreDOI:10.1016/0008-6215(86)85022-4日期:1986.1uniquely effective in enabling Trichoderma reesei trehalase to catalyze reactions with beta-D-glucosyl fluoride. As little as 0.2mM added alpha-D-glucose (0.4mM alpha-D-xylose) substantially increased the rate of enzymically catalyzed release of fluoride from 25mM beta-D-glucosyl fluoride at 0 degrees. Digests of beta-D-glucosyl fluoride plus alpha-D-xylose yielded the alpha, alpha-trehalose analog, alpha-D-glucopyranosyl先前显示海藻糖酶(参见参考文献5)水解α-D-葡萄糖基氟,形成β-D-葡萄糖,并由β-D-葡萄糖基氟加α-D-葡萄糖合成α,α-海藻糖。目前的观察结果进一步定义了在利用这些非糖苷底物时酶对单独的共底物的要求。发现α-D-葡糖醛糖和α-D-木吡喃糖在使里氏木霉海藻糖酶催化与β-D-葡糖基氟化物的反应方面具有独特的功效。添加低至0.2mM的α-D-葡萄糖(0.4mMα-D-木糖)在0度下大大提高了25mMβ-D-葡萄糖基氟化物的酶催化氟化物释放速率。β-D-葡萄糖基氟化物加α-D-木糖的消化物产生了α-α-海藻糖类似物,α-D-吡喃葡萄糖基α-D-木吡喃糖苷,作为一种短暂的(即随后水解的)转移产物。当β-D-葡糖基氟化物是供体时,需要具有轴向1-OH基的醛基吡喃糖受体,而当α-D-葡糖基氟化物是底物时需要水,这表明海藻糖的催化基团具有催化的灵活性。不同的立体化学反应。
表征谱图
-
氢谱1HNMR
-
质谱MS
-
碳谱13CNMR
-
红外IR
-
拉曼Raman
-
峰位数据
-
峰位匹配
-
表征信息
同类化合物
(反式)-4-壬烯醛
(s)-2,3-二羟基丙酸甲酯
([1-(甲氧基甲基)-1H-1,2,4-三唑-5-基](苯基)甲酮)
(Z)-4-辛烯醛
(S)-氨基甲酸酯β-D-O-葡糖醛酸
(S)-3-(((2,2-二氟-1-羟基-7-(甲基磺酰基)-2,3-二氢-1H-茚满-4-基)氧基)-5-氟苄腈
(R)-氨基甲酸酯β-D-O-葡糖醛酸
(5,5-二甲基-2-(哌啶-2-基)环己烷-1,3-二酮)
(2,5-二氟苯基)-4-哌啶基-甲酮
龙胆苦苷
龙胆二糖甲乙酮氰醇(P)
龙胆二糖丙酮氰醇(P)
龙胆三糖
龙涎酮
齐罗硅酮
齐留通beta-D-葡糖苷酸
鼠李糖
黑芥子苷单钾盐
黑海棉酸钠盐
黑木金合欢素
黑曲霉三糖
黑介子苷
黄尿酸8-O-葡糖苷
麻西那霉素II
麦迪霉素
麦芽糖脎
麦芽糖基海藻糖
麦芽糖1-磷酸酯
麦芽糖
麦芽四糖醇
麦芽四糖
麦芽十糖
麦芽六糖
麦芽五糖水合物
麦芽五糖
麦芽五糖
麦芽五糖
麦芽三糖醇
麦芽三糖
麦芽三糖
麦芽三塘水合
麦芽七糖水合物
麦芽七糖
麦法朵
麦可酚酸-酰基-Β-D-葡糖苷酸
麦利查咪
麝香酮
鹤草酚
鸢尾酚酮 3-C-beta-D-吡喃葡萄糖苷
鸡矢藤苷